หน้าหลักนี้ประกอบด้วยเอกสารฉบับแปลของบทความวิชาการต้นฉบับ
อย่างไรก็ตาม เรา ได้จัดทำสรุปเนื้อหาที่สำคัญแบบย่อยง่ายไว้ให้ผู้อ่านได้ศึกษาเป็นลำดับแรก เพื่อให้เข้าใจภาพรวมของงานวิจัยชิ้นนี้ได้อย่างรวดเร็ว หากท่านมีความสนใจในรายละเอียดเชิงลึกหรือข้อมูลทางสถิติเพิ่มเติม ท่านสามารถเลือกอ่านเอกสารฉบับเต็มได้ทั้งในรูปแบบภาษาอังกฤษ (Original) ได้ที่ลิงก์นี้: https://www.mdpi.com/1660-4601/14/3/329/htm หรือหากต้องการอ่านฉบับภาษาไทย (Translated) เราได้จัดทำบทแปลไว้ให้แล้วในหน้านี้ (ล่างสุด)
สรุปเนื้อหา
บทความเรื่อง Efficacy and Safety Evaluation of a Chlorine Dioxide Solution เป็นการศึกษาที่ประเมินทั้งประสิทธิภาพและความปลอดภัยของสารละลาย chlorine dioxide (ชื่อ UC-1) ที่ผลิตด้วยระบบไฟฟ้าและทำให้บริสุทธิ์ โดยผลการทดลองพบว่าสารดังกล่าวมีฤทธิ์ต้านจุลชีพสูง สามารถลดปริมาณแบคทีเรียและเชื้อราได้มากกว่า 98% ที่ความเข้มข้นต่ำ และยังมีฤทธิ์ยับยั้งไวรัสหลายชนิด เช่น influenza และ enterovirus ได้ในระดับที่มีนัยสำคัญ นอกจากนี้ การทดสอบความเป็นพิษทั้งในระดับเซลล์ สัตว์ทดลอง และการสัมผัสทางการหายใจ พบว่าในช่วงความเข้มข้นที่ใช้ทั่วไปไม่ก่อให้เกิดผลกระทบที่รุนแรง เช่น ไม่พบความเป็นพิษต่อเซลล์อย่างมีนัยสำคัญ และไม่พบความผิดปกติของอวัยวะในสัตว์ทดลอง จึงสรุปได้ว่า คลอรีน ไดอ็อกไซด์ ในรูปแบบที่เหมาะสมมีทั้งประสิทธิภาพในการฆ่าเชื้อและแนวโน้มความปลอดภัยที่ดี อย่างไรก็ตามยังคงต้องควบคุมปริมาณการใช้อย่างเคร่งครัดเพื่อหลีกเลี่ยงความเป็นพิษที่อาจเกิดขึ้น
เริ่มการแปลผลวิจัย
ข้อมูลการเผยแพร่
- ชื่อบทความ: Efficacy and Safety Evaluation of a Chlorine Dioxide Solution
- ผู้เขียน: Jui-Wen Ma และคณะ
- ปีที่ตีพิมพ์: 2017
- วารสารที่ตีพิมพ์: International Journal of Environmental Research and Public Health
บทคัดย่อ
ในการศึกษานี้ สารละลายคลอรีนไดออกไซด์ (UC-1) ที่ประกอบด้วยคลอรีนไดออกไซด์ถูกผลิตขึ้นโดยใช้วิธีการทางไฟฟ้าเคมี และต่อมาได้ทำการทำให้บริสุทธิ์โดยใช้เมมเบรน พบว่า UC-1 มีคลอรีนไดออกไซด์ในรูปก๊าซ 2000 ppm ในน้ำ ประสิทธิภาพและความปลอดภัยของ UC-1 ได้รับการประเมินแล้ว พบว่าฤทธิ์ต้านจุลชีพลดลงมากกว่า 98.2% เมื่อความเข้มข้นของ UC-1 อยู่ที่ 5 และ 20 ppm สำหรับแบคทีเรียและเชื้อรา ตามลำดับ ความเข้มข้นที่ยับยั้งได้ครึ่งหนึ่ง (IC50) ของ H1N1, ไวรัสไข้หวัดใหญ่ B/TW/71718/04 และ EV71 คือ 84.65 ± 0.64, 95.91 ± 11.61 และ 46.39 ± 1.97 ppm ตามลำดับ การทดสอบ 3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide (MTT) เผยให้เห็นว่าความสามารถในการอยู่รอดของเซลล์ไฟโบรบลาสต์ปอดของหนู L929 อยู่ที่ 93.7% ที่ความเข้มข้นของ UC-1 200 ppm ซึ่งสูงกว่าที่คาดการณ์ไว้ในการใช้งานปกติ นอกจากนี้ UC-1 ที่ความเข้มข้น 50 ppm ไม่แสดงอาการระคายเคืองตาอย่างมีนัยสำคัญในการทดสอบการระคายเคืองตาของกระต่าย
ในการทดสอบความเป็นพิษจากการสูดดม การรักษาด้วย UC-1 ที่ความเข้มข้น 20 ppm เป็นเวลา 24 ชั่วโมง ไม่แสดงความผิดปกติหรือการเสียชีวิตในอาการทางคลินิก และการทำงานของปอดและอวัยวะอื่นๆ เป็นปกติ ความเข้มข้นของ ClO2 สูงถึง 40 ppm ในน้ำดื่มไม่แสดงความเป็นพิษใดๆ ในการทดสอบความเป็นพิษทางปากแบบกึ่งเรื้อรัง ในที่นี้ UC-1 แสดงให้เห็นถึงกิจกรรมการฆ่าเชื้อที่ดีและมีแนวโน้มความปลอดภัยที่สูงกว่าในรายงานก่อนหน้านี้
คำสำคัญ: คลอรีนไดออกไซด์ (PubChem CID: 24870); ประสิทธิภาพในการต้านจุลชีพ; การทดสอบฤทธิ์ต้านไวรัส; ความเป็นพิษจากการสูดดม; ความเป็นพิษเรื้อรังจากการรับประทานทางปาก
บทนำ
คลอรีนไดออกไซด์ ซึ่งเป็นสารออกซิไดซ์ที่แรง สามารถยับยั้งหรือทำลายจุลินทรีย์ได้ มีการศึกษาค้นคว้าเกี่ยวกับการประยุกต์ใช้คลอรีนไดออกไซด์ในหลายสาขา เช่น การบำบัดน้ำหรือน้ำเสีย การฆ่าเชื้อในสิ่งแวดล้อมและอาหาร และการแพทย์ โดยทั่วไป คลอรีนไดออกไซด์จะผลิตโดยใช้วิธีการแบบใช้กรดหรือแบบอิเล็กโทรไลซิส ในวิธีการแบบใช้กรด คลอรีนไดออกไซด์จะผลิตโดยการผสมสารตั้งต้น เช่น โซเดียมคลอไรต์และกรดไฮโดรคลอริก โซเดียมคลอไรต์และเฟอร์ริกไตรคลอไรด์ หรือโซเดียมคลอไรต์และก๊าซคลอรีน ในวิธีการแบบอิเล็กโทรไลซิส สารตั้งต้นคือโซเดียมคลอไรด์ในน้ำหรือน้ำเกลืออิ่มตัวและโซเดียมไฮโปคลอไรต์
ตามกฎเกี่ยวกับสารฆ่าเชื้อและผลพลอยได้จากการฆ่าเชื้อ (DBPR) ของสำนักงานคุ้มครองสิ่งแวดล้อมแห่งสหรัฐอเมริกา คู่มือคำแนะนำการปฏิบัติตามกฎเกี่ยวกับจุลินทรีย์และผลพลอยได้จากการฆ่าเชื้อพร้อมกัน [14] เป้าหมายระดับสารฆ่าเชื้อตกค้างสูงสุด (MRDLG) และระดับสารฆ่าเชื้อตกค้างสูงสุด (MRDL) ของคลอรีนไดออกไซด์คือ 0.8 มก./ลิตร ขีดจำกัดการสัมผัสที่อนุญาต (PELs) สำหรับคลอรีนไดออกไซด์ที่กำหนดโดยสำนักงานความปลอดภัยและสุขภาพในการทำงานมีดังนี้: (ก) อุตสาหกรรมทั่วไป: 0.1 ppm และ 0.3 มก./ลบ.ม.; (ข) อุตสาหกรรมการก่อสร้าง: 0.1 ppm และ 0.3 มก./ลบ.ม. ค่าเฉลี่ยถ่วงน้ำหนักตามเวลา (TWA); (ค) ค่าขีดจำกัดเกณฑ์ของ American Conference of Governmental Industrial Hygienists: 0.1 ppm และ 0.28 มก./ลบ.ม. TWA; 0.3 ppm และ 0.83 mg/m3 ขีดจำกัดการสัมผัสระยะสั้น (STEL); (d) ขีดจำกัดการสัมผัสที่แนะนำโดยสถาบันแห่งชาติเพื่อความปลอดภัยและสุขภาพในการทำงาน: 0.1 ppm TWA; 0.3 ppm STEL
การใช้ผลิตภัณฑ์คลอรีนไดออกไซด์หรือการสัมผัสกับอาหารหรือร่างกายมนุษย์เป็นปัญหาที่ร้ายแรงหากผลิตภัณฑ์มีสิ่งเจือปนในระดับสูง สิ่งเจือปนส่วนใหญ่เกิดจากสารตั้งต้นที่ไม่บริสุทธิ์ เช่น H2SO4 10% และ NaClO2 15% หรือผลพลอยได้จากปฏิกิริยา เช่น Cl2 และคลอโรออกซีแอนไอออน ตัวอย่างเช่น H2SO4 10% และ NaClO2 15% มีสิ่งเจือปนที่ไม่ทราบชนิด 90% และ 85% ตามลำดับ ผลิตภัณฑ์คลอรีนไดออกไซด์ที่ได้จากส่วนผสมของ H2SO4 10% และ NaClO2 15% นั้น ไม่บริสุทธิ์อย่างมาก ผลิตภัณฑ์ Cl2 สามารถทำปฏิกิริยากับสารอินทรีย์เพื่อสร้างไตรฮาโลมีเทน ซึ่งเป็นสารก่อมะเร็งคลอโรออกซีแอนไอออน เช่น ClO2− หรือ ClO3− อาจเป็นอันตรายต่อสุขภาพของมนุษย์
การใช้คลอรีนไดออกไซด์ในครัวเรือนและอุตสาหกรรมควรได้รับการประเมินตามความบริสุทธิ์ของผลิตภัณฑ์ ซึ่งวิธีการเตรียมเป็นขั้นตอนที่สำคัญ วัตถุดิบเริ่มต้นที่มีความบริสุทธิ์ต่ำ (เช่น HCl 5% และ NaClO2 10%) มีปริมาณสิ่งเจือปนสูง หากผลิตภัณฑ์จากปฏิกิริยาเหล่านี้ไม่ได้รับการทำให้บริสุทธิ์เพิ่มเติมผลิตภัณฑ์คลอรีนไดออกไซด์ที่ผลิตได้ซึ่งมีสิ่งเจือปนในระดับสูงเช่นกัน จะมีประโยชน์เฉพาะสำหรับการบำบัดน้ำเสียเท่านั้น และไม่เหมาะสมสำหรับการสัมผัสกับมนุษย์หรืออาหารเนื่องจากสิ่งเจือปนที่เป็นอันตราย ดังนั้นจึงต้องได้รับโมเลกุลก๊าซคลอรีนไดออกไซด์ในเปอร์เซ็นต์ที่สูงขึ้นผ่านการทำให้โมเลกุลก๊าซคลอรีนไดออกไซด์บริสุทธิ์เพิ่มเติม
เพื่อเพิ่มความปลอดภัยของสารละลายคลอรีนไดออกไซด์ การกำจัดหรือลดสิ่งเจือปนและการเพิ่มความเข้มข้นของก๊าซคลอรีนไดออกไซด์ในสารละลายถือเป็นแนวทางที่เหมาะสม ในที่นี้ได้มีการออกแบบและดำเนินการกระบวนการผลิตก๊าซคลอรีนไดออกไซด์ที่สะอาดและเข้มข้น เราได้ผลิตสารละลายคลอรีนไดออกไซด์ (UC-1) ที่มีก๊าซคลอรีนไดออกไซด์ 2000 ppm ในน้ำโดยใช้วิธีการอิเล็กโทรไลซิส สารละลายดังกล่าวได้รับการทำให้บริสุทธิ์เพิ่มเติมด้วยเมมเบรนฟิล์ม และละลายในน้ำรีเวิร์สออสโมซิส (RO) ในภายหลัง UC-1 ได้รับการตรวจสอบเพื่อหาประสิทธิภาพและประเด็นด้านความปลอดภัย เช่น กิจกรรมต้านจุลชีพ ความเป็นพิษต่อเซลล์ในหลอดทดลอง การระคายเคืองตาของกระต่ายในร่างกาย ความเป็นพิษจากการสูดดมในร่างกาย และความเป็นพิษเรื้อรังจากการรับประทานในร่างกาย
เครื่องมือและวิธีการ
วิธีการผลิตก๊าซคลอรีนไดออกไซด์ด้วยกระบวนการอิเล็กโทรไลซิส
สารละลาย UC-1 ผลิตขึ้นในอุปกรณ์ ซึ่งรายละเอียดทางเทคนิคจะถูกเผยแพร่ในภายหลังในรูปแบบของคำขอสิทธิบัตร (PCT applied PCT/CN2016/080198; PCT applied PCT/CN2016/080199; PCT applied PCT/CN2015/099515; DE202016103175) โดยวิธีทางเคมีไฟฟ้า โดยสรุป สารละลายโซเดียมคลอไรด์ทำจากโซเดียมคลอไรด์ 99% (เกรดอาหาร) และน้ำ RO แล้วปั๊มเข้าไปในอุปกรณ์อ่างไฟฟ้า การอิเล็กโทรไลซิสทำงานโดยใช้แรงดันไฟฟ้า 6–12 V และกระแสไฟฟ้า 40–80 A หลังจากอิเล็กโทรไลซิสแล้ว ก๊าซ ClO2 จะถูกผสมกับน้ำโดยใช้เครื่องผสมน้ำ-ClO2 ซึ่งออกแบบโดยอาศัยผลของเวนทูริ การผสมน้ำกับก๊าซ ClO2 ดำเนินต่อไปตามวัฏจักรจนกระทั่งความเข้มข้นของ ClO2 ในน้ำสูงกว่า 2000 ppm (ภาพที่ 1) และค่า pH เท่ากับ 2.2 สารละลายคลอรีนไดออกไซด์ที่ผลิตได้จากกระบวนการนี้เรียกว่า UC-1
องค์ประกอบทางเคมีของสารละลาย UC1 ถูกกำหนดตามวิธีการมาตรฐาน ได้รับข้อมูลดังต่อไปนี้: ClO2: 2120 ppm, คลอรีนอิสระ (Cl2): 882 ppm, และคลอรีนทั้งหมด (Cl2 + HOCl + OCl−): 900 ppm ความเข้มข้นของคลอรีนทั้งหมดสูงกว่าในกรณีของเครื่องกำเนิด ClO2 อื่นๆ เล็กน้อย เนื่องจากอิเล็กโทรไลต์ที่เราใช้ไม่มี NaClO2 สารละลาย UC-1 ผลิตขึ้นโดยใช้สารละลาย NaCl 25% เท่านั้น โดยไม่มีสารเติมแต่งอื่นๆ
ซึ่งเป็นข้อได้เปรียบที่เห็นได้ชัด ในขณะเดียวกัน แม้จะมีปริมาณคลอรีนทั้งหมดสูงกว่า (ซึ่งมีอยู่ในสารละลาย UC-1 ที่เจือจางส่วนใหญ่ในรูปของ HOCl) ก็ไม่พบผลกระทบที่ไม่พึงประสงค์ที่ตรวจพบได้ในสัตว์ทดลองหรือเนื้อเยื่อสัตว์
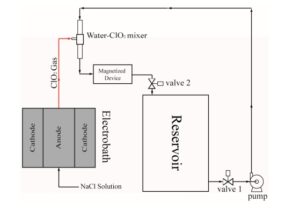
ภาพที่ 1 แผนผังแสดงขั้นตอนการผลิตสารละลายคลอรีนไดออกไซด์
การทดสอบประสิทธิภาพการต้านจุลชีพ
การทดสอบดำเนินการตาม U.S. Pharmacopeia 34 NF29 การทดสอบทางจุลชีววิทยา/<51> การทดสอบประสิทธิภาพต้านจุลชีพ จุลินทรีย์ที่ใช้ในการทดสอบมีดังนี้: Escherichia coli (BCRC 11634/ATCC 8739), Staphylococcus aureus (BCRC 10451/ATCC 6538P), Pseudomonas aeruginosa (BCRC 11633/ATCC 9027), S. aureus subsp. aureus (BCRC 15211/ATCC 33591), Bacillus subtilis subspecies (BCRC 10447/ATCC 6633), Listeria monocytogenes (BCRC 14848/ATCC 19114), Acinetobacter baumannii (BCRC 10591/ATCC 19606), Salmonella enterica subspecies (BCRC 12947/ATCC
13311), Klebsiella pneumoniae (BCRC 16082/ATCC 4352), Penicillium funiculosum (BCRC 30438/ATCC 11797) และ Candida albicans (BCRC 21538/ATCC10231)
การทดสอบต้านไวรัส
ไวรัสถูกขยายจำนวนในเซลล์ MDCK/RD เซลล์ MDCK/RD ถูกเพาะเลี้ยงในอาหารเลี้ยงเซลล์ Dulbecco’s modified Eagle’s medium (FBS DMEM) ที่มีซีรั่มจากลูกวัว 10% เมื่อเซลล์เจริญเติบโตจนเต็มพื้นที่ 90%
เซลล์จะถูกล้างด้วยสารละลายฟอสเฟตบัฟเฟอร์ (PBS) และติดเชื้อด้วยอัตราการติดเชื้อ 0.01 หลังจากติดเชื้อแล้ว จะเติม DMEM ที่มี FBS 0% และบ่มเซลล์ที่อุณหภูมิ 35 ◦C ในตู้บ่มที่มี CO2 5% เป็นเวลา 48 ชั่วโมง
นำเซลล์แขวนลอย 1 มล. (6 × 10⁵ เซลล์) ใส่ลงในแต่ละหลุมของจานเพาะเลี้ยง 6 หลุม จากนั้นบ่มที่อุณหภูมิ 37 ◦C เป็นเวลา 18–24 ชั่วโมง ใช้ PBS เจือจาง UC-1 ให้มีความเข้มข้นสุดท้ายที่ 0, 25, 50,
100 และ 200 ppm ในหลุมที่ทำปฏิกิริยากับเซลล์และไวรัสเป็นเวลา 2 นาทีที่อุณหภูมิ 37 ◦C หลังจากปฏิกิริยาเสร็จสิ้น เจือจางส่วนผสมปฏิกิริยาทั้งหมดให้มีความเข้มข้น 10⁻⁸ จากนั้นบ่มส่วนผสมที่เจือจาง 10⁻⁸ นี้ที่อุณหภูมิ 37 ◦C เป็นเวลา 48–64 ชั่วโมง ตรึงเซลล์ด้วยฟอร์มาลิน 10% เป็นเวลา 1 ชั่วโมง และย้อมด้วยคริสตัลไวโอเลต 0.1% เป็นเวลา 5 นาที นับจำนวนพลากที่เกิดขึ้นจากไวรัสและเปรียบเทียบระหว่างกลุ่มทดสอบและกลุ่มควบคุม กิจกรรมต้านไวรัสแสดงเป็นเปอร์เซ็นต์การควบคุมไวรัส = จำนวนคราบจุลินทรีย์ในกลุ่มทดสอบ/จำนวนคราบจุลินทรีย์ในกลุ่มควบคุม × 100 การควบคุมไวรัสหมายถึงไวรัสที่ติดเชื้อในเซลล์ที่ไม่มีสารทดสอบ และถือว่าเท่ากับ 100%
การทดสอบความเป็นพิษต่อเซลล์ในหลอดทดลอง (การทดสอบ MTT)
เซลล์ไฟโบรบลาสต์ปอดของหนู L929 ถูกเพาะเลี้ยงในอาหารเลี้ยงเซลล์ Eagle minimum essential medium (MEM) ที่สมบูรณ์ และบ่มที่อุณหภูมิ 37 ◦C ± 1 ◦C ในบรรยากาศ 5% ± 1% CO2 จากนั้น นำเซลล์ L929 จำนวน 100 µL (1 × 10⁵ เซลล์/มล.) ถ่ายลงในแต่ละหลุมของจานเพาะเลี้ยงเซลล์ 96 หลุม เซลล์ถูกบ่มต่อที่อุณหภูมิ 37 ◦C ± 1 ◦C เป็นเวลา 24 ชั่วโมง ± 2 ชั่วโมง เปลี่ยนอาหารเลี้ยงเซลล์ด้วยสารละลายทดสอบหรือสารละลายควบคุมว่างเปล่า สารละลายควบคุมเชิงบวก หรือสารละลายควบคุมเชิงลบ จำนวน 100 µL สารละลายทดสอบประกอบด้วย UC-1 ที่ความเข้มข้น 0 (ควบคุม), 200, 400, 600 และ 800 ppm ใน MEM สารละลายควบคุมว่างเปล่าประกอบด้วยซีรั่มม้า 10% เซลล์ถูกบ่มต่ออีก 24 ชั่วโมง เซลล์ได้รับการบำบัดด้วยสารละลายเหล่านี้ซ้ำกัน 3 ครั้ง
หลังจากเติมสารละลาย MTT ลงในแต่ละหลุมแล้ว นำเพลทไปบ่มเป็นเวลา 2 ชั่วโมง ± 10 นาที ที่อุณหภูมิ 37 ◦C ± 1 ◦C จากนั้นแทนที่สารละลาย MTT ด้วยไดเมทิลซัลฟอกไซด์ 100 µL และนำไปวิเคราะห์ด้วยเครื่องอ่านไมโครเพลทที่ติดตั้งตัวกรอง 570 นาโนเมตรสำหรับการวัดสี (ค่าอ้างอิง 650 นาโนเมตร) ผลการทดสอบ MTT สามครั้งจะแสดงเป็นค่าเฉลี่ย ± ส่วนเบี่ยงเบนมาตรฐาน (SD) ความมีชีวิตของเซลล์ (%) = ความหนาแน่นเชิงแสงของกลุ่มทดสอบ/ความหนาแน่นเชิงแสงของกลุ่มควบคุม × 100
การทดสอบการระคายเคืองตาของกระต่ายขาว
ซื้อกระต่ายขาวพันธุ์นิวซีแลนด์เพศเมียจำนวน 6 ตัว น้ำหนัก 2–3 กิโลกรัม จากสถาบันวิจัยปศุสัตว์ไต้หวัน (ซินหัว ไถหนาน ไต้หวัน) โดยนำกระต่ายไปกักกันและปรับตัวก่อนทำการทดลองสัตว์เหล่านี้ได้รับอาหารอย่างไม่จำกัด และเลี้ยงไว้ที่อุณหภูมิ 20–26 องศาเซลเซียส ภายใต้ความชื้น 30–70% นอกจากนี้หยอดสารละลาย UC-1 ความเข้มข้น 50 ppm (สารละลายทดสอบ) ปริมาณ 0.1 มิลลิลิตร ลงในตาซ้ายของกระต่าย และหยอดสารละลายเกลือปกติ 0.9% (สารละลายควบคุม) ปริมาณ 0.1 มิลลิลิตร ลงในตาขวา จากนั้นจับเปลือกตาทั้งสองข้างเข้าหากันเป็นเวลา 1 วินาที ก่อนหยอดสารละลาย การทดลองแต่ละครั้งทำซ้ำ 3 ครั้ง สังเกตอาการระคายเคืองตาในชั่วโมงที่ 1, 24, 48 และ 72 โดยใช้กล้องตรวจตา (Welch Allyn, Skaneateles Falls, NY, USA)
ในกรณีที่มีรอยโรคคงอยู่ จำเป็นต้องมีการสังเกตการณ์อย่างต่อเนื่องเพื่อตรวจสอบความคืบหน้าหรือการกลับคืนสู่สภาพเดิมของรอยโรค คะแนนการระคายเคืองตาจะอิงตามระบบการให้คะแนนรอยโรคที่ตา (ISO 10993-10) หากสัตว์มากกว่าหนึ่งตัวในกลุ่มทดสอบแสดงผลบวกในขั้นตอนใดๆ ของการสังเกตการณ์ ส่วนประกอบที่ทดสอบนั้นจะถือว่าเป็นสารระคายเคืองตา และไม่จำเป็นต้องทำการทดสอบเพิ่มเติม หากกลุ่มทดสอบเพียงกลุ่มเดียวแสดงปฏิกิริยาเล็กน้อยหรือปานกลางที่ไม่แน่ชัด ขั้นตอนนี้จะดำเนินการกับสัตว์เพิ่มเติมอีกสามตัว หากดวงตามากกว่าครึ่งหนึ่งแสดงผลบวกในขั้นตอนใดๆ ของการสังเกตการณ์ ส่วนประกอบที่ทดสอบนั้นจะถือว่าเป็นสารระคายเคืองตา ปฏิกิริยารุนแรงในสัตว์เพียงตัวเดียวก็ถือว่าเพียงพอที่จะระบุส่วนประกอบที่ทดสอบนั้นว่าเป็นสารระคายเคืองตา
การทดสอบความเป็นพิษจากการสูดดม
ซื้อหนู BALB/c เพศผู้ อายุ 4 สัปดาห์ จำนวน 15 ตัว จากศูนย์สัตว์ทดลองแห่งชาติ (ไทเป ไต้หวัน) กักกันและปรับตัวให้เข้ากับสภาพแวดล้อมก่อนทำการทดลองในห้องสัตว์ทดลองที่มหาวิทยาลัยการแพทย์จีน ไต้หวัน ให้อาหารอย่างอิสระและรักษาอุณหภูมิไว้ที่ 20–25 ◦C และความชื้น 65%–80% เลี้ยงหนู 5 ตัวในกรงเดียวกัน โดยให้กินสารละลาย 0 (PBS) และ 10 หรือ 20 ppm (สารละลายทดสอบ) โดยให้เป็นละอองโดยใช้เครื่องทำความชื้นในกล่องปิดสนิทเป็นเวลา 24 ชั่วโมง สังเกตอาการทางคลินิกและน้ำหนักตัวของสัตว์ทดลอง จากนั้นจึงทำการฆ่าสัตว์ทดลองเพื่อตรวจสอบส่วนปอดและน้ำหนักอวัยวะ สังเกตอาการของสัตว์ทดลองและบันทึกอาการทางคลินิกเป็นเปอร์เซ็นต์ความผิดปกติ (%) ซึ่งหมายถึงสัตว์ทดลองมีพฤติกรรมผิดปกติเมื่อเทียบกับสัตว์ทดลองปกติ และเปอร์เซ็นต์การตาย (%) ซึ่งหมายถึงสัตว์ทดลองตาย
การประเมินน้ำหนักอวัยวะ
ในระหว่างการทดลอง สัตว์ทดลองจะถูกผ่าพิสูจน์ทันทีหลังจากตาย และมีการบันทึกข้อมูลไว้ สัตว์ทดลองที่รอดชีวิตทั้งหมดจะถูกฆ่าและผ่าพิสูจน์เพื่อสังเกตลักษณะและอวัยวะทั้งหมดในช่องปาก ช่องอก กะโหลกศีรษะ และช่องท้อง จากนั้น อวัยวะต่างๆ รวมถึงตับ ต่อมหมวกไต ไต และอวัยวะสืบพันธุ์ จะถูกนำออกมาชั่งน้ำหนักและบันทึกข้อมูล
การย้อมสีฮีมาทอกซิลินและอีโอซินของชิ้นส่วนปอดหนู
ชิ้นส่วนเนื้อเยื่อที่แช่แข็งในสารประกอบอุณหภูมิการตัดที่เหมาะสมจะถูกตรึงด้วยอะซิโตนและคลอโรฟอร์ม ชิ้นส่วนจะถูกแช่ในแฮร์ริสฮีมาทอกซิลินที่กรองแล้ว (Leica Biosystems Richmond, Inc., Richmond, IL, USA) เป็นเวลา 1 นาที สไลด์จะถูกล้างอีกครั้งด้วยสารละลายบัฟเฟอร์ Tris และ Tween 20 (Biokit Biotechnology Inc., Miaoli, Taiwan) และชิ้นส่วนจะถูกย้อมสีเพิ่มเติมด้วยอีโอซิน (Leica Biosystems Richmond, Inc., Richmond, IL, USA) เป็นเวลา 1–2 นาที ชิ้นส่วนจะถูกทำให้แห้ง ในสารละลายแอลกอฮอล์ที่มีความเข้มข้นเพิ่มขึ้นและทำให้ใสด้วยไซลีน สไลด์ที่เตรียมไว้จะถูกตรวจสอบผ่านกล้องจุลทรรศน์แบบใช้แสง
การทดสอบความเป็นพิษเรื้อรังทางปาก
หนู BALB/c เพศผู้ อายุ 4 สัปดาห์ จำนวน 25 ตัว ถูกซื้อมาจากศูนย์สัตว์ทดลองแห่งชาติ โดยถูกกักกันและปรับตัวให้เข้ากับสภาพแวดล้อมก่อนการทดลองในห้องสัตว์ทดลองที่มหาวิทยาลัยการแพทย์จีน สัตว์ทดลองได้รับอาหารอย่างอิสระและถูกเลี้ยงไว้ที่อุณหภูมิ 20–25 ◦C ภายใต้ความชื้น 65%–80% หนู 5 ตัวถูกเลี้ยงไว้ในกรงเดียวกันและได้รับสารละลาย UC-1 ที่ความเข้มข้น 0 (PBS; กลุ่มควบคุม), 5, 10, 20 และ 40 ppm (สารละลายทดสอบ) อย่างต่อเนื่องเป็นเวลา 90 วัน สารละลาย PBS หรือสารละลายทดสอบที่ใช้เป็นน้ำดื่มนั้นถูกเตรียมใหม่ทุกวันก่อนการทดลอง
- การประเมินอาการทางคลินิก
สัตว์ทดลองได้รับการสังเกต และอาการทางคลินิกของพวกมันถูกบันทึกเป็นความผิดปกติ (%) ซึ่งหมายถึงสัตว์ที่มีพฤติกรรมผิดปกติเมื่อเทียบกับสัตว์ปกติ และอัตราการตาย (%) ซึ่งหมายถึงการตายของสัตว์
- น้ำหนักตัว
น้ำหนักตัวของสัตว์ทดลองถูกบันทึกไว้เมื่อเริ่มการรักษาและสัปดาห์ละครั้งตลอดระยะเวลาการทดลอง โดยใช้เครื่องชั่งอิเล็กทรอนิกส์ (AND, FX-2000i, โตเกียว, ญี่ปุ่น)
- การชันสูตรศพ การตรวจดูอวัยวะโดยละเอียด และการชั่งน้ำหนักอวัยวะ
ในระหว่างการทดลอง สัตว์ทดลองจะถูกผ่าทันทีหลังจากตาย และมีการบันทึกข้อมูลไว้ สัตว์ทดลองที่รอดชีวิตทั้งหมดจะถูกฆ่าและผ่าชันสูตรเพื่อสังเกตลักษณะภายนอก และอวัยวะทั้งหมดในปาก หน้าอก กะโหลกศีรษะ และช่องท้องจะถูกนำมาวิเคราะห์ ต่อมา อวัยวะต่างๆ รวมถึงตับ ต่อมหมวกไต ไต และอวัยวะสืบพันธุ์ จะถูกนำออกมาชั่งน้ำหนักและบันทึกข้อมูล
การวิเคราะห์ทางสถิติ
ผลลัพธ์ได้รับการวิเคราะห์โดยใช้ SPSS เวอร์ชัน 20.0 (IBM Corp., Armonk, NY, USA) ด้วยการวิเคราะห์ความแปรปรวนแบบทางเดียว (ANOVA), การทดสอบ F และการทดสอบช่วงหลายค่าใหม่ของดันแคน (Duncan’s new multiple range test) สำหรับการเปรียบเทียบค่าเฉลี่ยมากกว่าสองค่า ผลลัพธ์ที่มีค่า p < 0.05 แสดงถึงความแตกต่างอย่างมีนัยสำคัญ ผลลัพธ์แสดงถึงการทดลองอิสระอย่างน้อย 3 ครั้ง และแสดงเป็นค่าเฉลี่ย ± ส่วนเบี่ยงเบนมาตรฐาน (SD)
คำแถลงด้านจริยธรรม
งานวิจัยนี้ได้รับการอนุมัติจากศูนย์บริการสัตว์ทดลองของมหาวิทยาลัยการแพทย์จีน หมายเลขโครงการ: 10442699 (สำหรับการทดสอบการระคายเคืองตาของกระต่ายขาว) และ 10442686 (สำหรับการทดสอบความเป็นพิษจากการสูดดมและการทดสอบความเป็นพิษเรื้อรังจากการรับประทาน)
ผลลัพธ์
ในการศึกษานี้ สารละลาย UC-1 ที่มีคลอรีนไดออกไซด์ 2000 ppm ในน้ำ ถูกผลิตขึ้นโดยวิธีการอิเล็กโทรไลซิส โดยใช้เกลือเกรดอาหาร (NaCl 99%) และน้ำ RO เป็นสารตั้งต้น จากนั้น คลอรีนไดออกไซด์ถูกทำให้บริสุทธิ์ผ่านฟิล์มและละลายในน้ำ RO เนื่องจากสารละลายคลอรีนไดออกไซด์สามารถนำไปใช้โดยตรงกับอาหารหรือสุขอนามัยของมนุษย์ หรือมาตรการป้องกันสุขภาพได้ จึงได้ทำการตรวจสอบความปลอดภัยและประสิทธิภาพของสารละลายดังกล่าว
การทดสอบประสิทธิภาพการต้านจุลชีพ
ได้ทำการตรวจสอบฤทธิ์ต้านจุลชีพในหลอดทดลองของ UC-1 พบว่าฤทธิ์ต้านจุลชีพในหลอดทดลองลดลงมากกว่า 98.2% สำหรับแบคทีเรียและเชื้อรา (ตารางที่ 1) และพบฤทธิ์ต้านจุลชีพที่ดีเยี่ยมที่ความเข้มข้นต่ำ 5 และ 20 ppm ของ UC-1 สำหรับแบคทีเรียและเชื้อรา ตามลำดับ
ตารางที่ 1 ประสิทธิภาพในการต้านจุลชีพของ UC-1
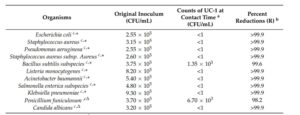
a ระยะเวลาสัมผัสคือ 10 นาที
b เปอร์เซ็นต์การลดลง <1% แสดงว่าไม่มีการยับยั้งแบคทีเรียหรือเชื้อราอย่างมีนัยสำคัญ
c ความเข้มข้นของ UC-1 คือ 5 และ 20 ppm สำหรับแบคทีเรียและเชื้อรา ตามลำดับ * แสดงผลเป็นแบคทีเรีย; ∆ แสดงผลเป็นเชื้อรา CFU: หน่วยสร้างโคโลนี
การทดสอบต้านไวรัส
ฤทธิ์ต้านไวรัสของ UC-1 ที่ความเข้มข้น 0, 25, 50, 100 และ 200 ppm หลังจากปฏิกิริยา 2 นาที แสดงในภาพที่ 2 สำหรับ H1N1 และไวรัสไข้หวัดใหญ่ B/TW/71718/04 พบว่า UC-1 ที่ความเข้มข้น 200 ppm มีผลยับยั้งการก่อตัวของคราบไวรัสได้อย่างมีนัยสำคัญที่สุด ความเข้มข้นที่ยับยั้งได้ครึ่งหนึ่ง (IC50) ของ H1N1 คือ 84.65 ± 0.64 ppm และของไวรัสไข้หวัดใหญ่ B/TW/71718/04 คือ 95.91 ± 11.61 ppm สำหรับ EV71
UC-1 ที่ความเข้มข้น 50 ppm แสดงฤทธิ์ยับยั้งอย่างมีนัยสำคัญ โดยมีค่า IC50 เท่ากับ 46.39 ± 1.97 ppm ที่ 2 นาที ผลลัพธ์ที่แสดงนัยสำคัญทางสถิติ (p < 0.05) ได้ถูกนำเสนอไว้แล้ว แท่งกราฟแสดงค่าเฉลี่ย ± ส่วนเบี่ยงเบนมาตรฐาน
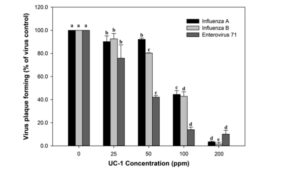
ภาพที่ 2 ประสิทธิภาพการต้านไวรัสไข้หวัดใหญ่สายพันธุ์ A/WSN/33, สายพันธุ์ B/TW/71718/04 และสายพันธุ์เอนเทอโรไวรัส 71 แท่งกราฟแสดงค่าเฉลี่ย ± ส่วนเบี่ยงเบนมาตรฐาน (SD) ค่าเฉลี่ยที่มีตัวอักษรเดียวกัน
ไม่แตกต่างกันอย่างมีนัยสำคัญที่ p < 0.05 ตามการทดสอบ F ของ ANOVA (การวิเคราะห์ความแปรปรวน) และการทดสอบช่วงหลายค่าใหม่ของดันแคน
การทดสอบความเป็นพิษต่อเซลล์ในหลอดทดลอง (การทดสอบ MTT)
ได้ทำการวิเคราะห์ผลกระทบที่เป็นพิษต่อเซลล์ของ UC-1 ที่ความเข้มข้น 0, 200, 400, 600 และ 800 ppm ต่อเซลล์ไฟโบรบลาสต์ปอด L929 พบว่าอัตราการรอดชีวิตของเซลล์อยู่ที่ 74.0%–100.0% ที่ความเข้มข้นของ UC-1 ต่ำกว่า 600 ppm และอัตราการรอดชีวิตของเซลล์ L929 ลดลงเหลือ 40.3% ที่ความเข้มข้น 800 ppm ของ UC-1 (ภาพที่ 3)
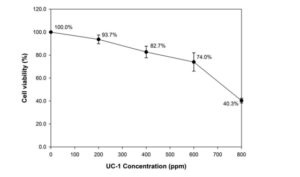
ภาพที่ 3 ผลกระทบที่เป็นพิษต่อเซลล์ของ UC-1 ในความเข้มข้นต่างๆ ต่อเซลล์ L929
การทดสอบการระคายเคืองตา
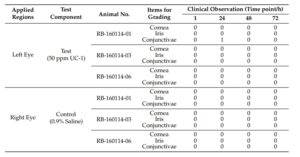
กระจกตา ม่านตา และเยื่อบุตาถูกประเมินในการทดสอบการระคายเคืองตาในกระต่าย สารละลาย UC-1 ความเข้มข้น 50 ppm ไม่ก่อให้เกิดอาการทางคลินิกที่สำคัญหรือการเปลี่ยนแปลงทางสายตาอย่างเห็นได้ชัดในกระต่ายในแต่ละช่วงเวลา (ตารางที่ 2) ดังนั้น การหยอดตาเพียงครั้งเดียวด้วยสารละลาย UC-1 ความเข้มข้น 50 ppm ปริมาณ 0.1 มล. จึงไม่ก่อให้เกิดการระคายเคืองตาในกระต่าย
ตารางที่ 2 ระดับคะแนนจากการสังเกตอาการระคายเคืองตาของกระต่ายแต่ละตัว
การทดสอบความเป็นพิษจากการสูดดม
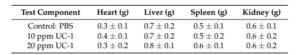
ในการทดสอบความเป็นพิษจากการสูดดม เราใช้ UC-1 ที่ความเข้มข้น 0, 10 และ 20 ppm ซึ่งให้โดยการพ่นเป็นละออง โดยใช้เครื่องทำความชื้นในกล่องปิดสนิทที่มีหนูทดลอง 5 ตัว การทดสอบแสดงให้เห็นว่าไม่มีความผิดปกติและไม่มีอัตราการตายในกลุ่มควบคุมและกลุ่มทดสอบภายใน 24 ชั่วโมง (ตารางที่ 3) น้ำหนักของหัวใจ ตับ ม้าม และไตของกลุ่มทดสอบไม่แตกต่างกันอย่างมีนัยสำคัญจากกลุ่มควบคุม (ตารางที่ 4) การย้อมสีฮีมาทอกซิลินและอีโอซินของส่วนตัดปอดของหนู (ภาพที่ 4) แสดงให้เห็นว่า UC-1 ที่ความเข้มข้น 10 และ 20 ppm ไม่ก่อให้เกิดสัญญาณทางคลินิกที่สำคัญของการเปลี่ยนแปลงในเซลล์ปอดของหนูภายใน 24 ชั่วโมง ดังนั้น การสูดดม UC-1 ที่ความเข้มข้น 10 และ 20 ppm จึงไม่ก่อให้เกิดการระคายเคืองในหนู
ตารางที่ 3 การประเมินอาการทางคลินิกในการทดสอบความเป็นพิษจากการสูดดม

PBS: สารละลายบัฟเฟอร์ฟอสเฟต
ตารางที่ 4 การประเมินน้ำหนักอวัยวะสำหรับการทดสอบความเป็นพิษจากการสูดดม
การวิเคราะห์ทางสถิติของข้อมูลที่นำเสนอได้ดำเนินการที่ระดับนัยสำคัญ 95% (p < 0.05)
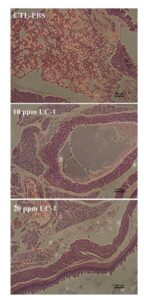
ภาพที่ 4 การย้อมสีฮีมาทอกซิลินและอีโอซินของส่วนตัดปอดของหนูในการทดสอบความเป็นพิษจากการสูดดม แถบมาตราส่วนที่ระบุในรูปนี้คือ 100 ไมโครเมตร
การทดสอบความเป็นพิษเรื้อรังทางปาก
ในการทดสอบความเป็นพิษเรื้อรังทางปาก ได้เตรียม UC-1 ที่ความเข้มข้น 0, 5, 10, 20 และ 40 ppm เพื่อให้หนูทดลองกิน จากการสังเกตทางคลินิกพบว่าไม่มีความผิดปกติและไม่มีหนูตายหลังจาก 90 วัน ทั้งในกลุ่มควบคุมและกลุ่มทดลอง (ตารางที่ 5) น้ำหนักของหนูไม่เปลี่ยนแปลง (รูปที่ 5) นอกจากนี้ การชันสูตรศพและการตรวจร่างกายโดยรวมไม่พบอาการผิดปกติใดๆ (ภาพที่ 6) น้ำหนักของหัวใจ ตับ ม้าม และไตของกลุ่มทดลองไม่แตกต่างกันอย่างมีนัยสำคัญเมื่อเทียบกับกลุ่มควบคุม (ตารางที่ 6) ดังนั้น การให้ UC-1 แก่หนูทดลองในปริมาณสูงถึง 40 ppm เป็นเวลา 90 วันจึงไม่เป็นพิษ
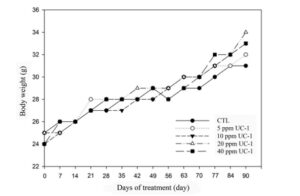
ภาพที่ 5 แผนภูมิแสดงแนวโน้มการเปลี่ยนแปลงน้ำหนักของหนูในการทดสอบความเป็นพิษเรื้อรังจากการให้ยาทางปาก CTL: กลุ่มควบคุม
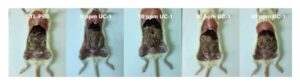
ภาพที่ 6 การสังเกตปอดและอวัยวะของหนูในการทดสอบความเป็นพิษเรื้อรังจากการให้ทางปาก
ตารางที่ 5 การประเมินอาการทางคลินิกในการทดสอบความเป็นพิษเรื้อรังจากการรับประทานยา

ตารางที่ 6 การประเมินน้ำหนักอวัยวะในการทดสอบความเป็นพิษเรื้อรังจากการรับประทาน
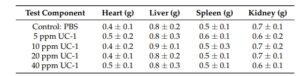
การวิเคราะห์ทางสถิติของข้อมูลที่นำเสนอได้ดำเนินการที่ระดับนัยสำคัญ 95% (p < 0.05)
การอภิปราย
UC-1 ที่มีก๊าซคลอรีนไดออกไซด์และสิ่งเจือปนน้อยลงถูกเตรียมขึ้นโดยใช้กระบวนการออกแบบที่เป็นมิตรต่อสิ่งแวดล้อมซึ่งได้รับการจดสิทธิบัตร และได้มีการประเมินประสิทธิภาพและความปลอดภัยของ UC-1 แล้ว งานวิจัยหลายชิ้นได้รายงานถึงฤทธิ์ออกซิแดนต์และฤทธิ์ต้านจุลชีพที่รุนแรงของคลอรีนไดออกไซด์ในหลอดทดลอง รายงานล่าสุดได้กล่าวถึงข้อกังวลที่เกี่ยวข้องกับการฆ่าเชื้อจุลินทรีย์ในอาหารด้วยคลอรีนไดออกไซด์ [6,9,18–21] ในการศึกษาเหล่านี้ คลอรีนไดออกไซด์ถูกผลิตขึ้นโดยใช้วิธีการต่างๆ (เช่น 2% NaClO2 กับ H3PO4, 4% Cl2 กับ 80% NaClO2 และโดยการใช้เครื่องกำเนิดไฟฟ้า) ฤทธิ์ต้านจุลชีพมากกว่า 2% สำหรับ
5–75 มก./ลิตร ClO2 ภายใน 5–30 นาที ในที่นี้ ฤทธิ์ต้านจุลชีพลดลงมากกว่า 98.2% ที่ความเข้มข้นของ UC-1 ที่ 5 และ 20 ppm สำหรับแบคทีเรียและเชื้อรา ตามลำดับ ในการทดสอบ MTT พบว่าเซลล์ L929 มีชีวิตรอดได้ 93.7% ที่ความเข้มข้น UC-1 200 ppm ซึ่งเป็นความเข้มข้นที่สูงกว่าการใช้งานตามปกติ
ไม่พบอาการสำคัญใดๆ ในการทดสอบการระคายเคืองตาด้วย UC-1 ที่ความเข้มข้น 50 ppm ไม่พบความผิดปกติหรือการเสียชีวิตในอาการทางคลินิก ปอด และอวัยวะอื่นๆ ที่ความเข้มข้น 10 ppm หรือ 20 ppm UC-1 ในการทดสอบความเป็นพิษจากการสูดดม Paulet และ Desbrousses [22] ได้ให้คลอรีนไดออกไซด์ที่ความเข้มข้น 2.5, 5, และ 10 ppm แก่หนูและกระต่ายในปี 1970 พวกเขารายงานว่าคลอรีนไดออกไซด์ที่ความเข้มข้น 2.5 ppm มีระดับผลกระทบที่ไม่พึงประสงค์ที่สังเกตได้ต่ำที่สุด (LOAEL) ทำให้เกิดผลกระทบต่อทรวงอกในหนูที่ 7 ชั่วโมงต่อวันเป็นเวลา 30 วัน และผลกระทบต่อปอดในกระต่ายที่ 4 ชั่วโมงต่อวันเป็นเวลา 45 วัน Paulet และ Desbrousses [23] เพิ่มความเข้มข้นของการทดสอบเป็น 5, 10 และ 15 ppm คลอรีนไดออกไซด์ และลดระยะเวลาการให้ยาเป็น 15 นาทีต่อครั้ง วันละ 2-4 ครั้ง เป็นเวลา 4 สัปดาห์ในหนูทดลอง ผลการทดลองแสดงให้เห็นระดับที่ไม่พบผลกระทบที่ไม่พึงประสงค์ (NOAEL) ที่ 5 ppm และระดับที่ไม่พบผลกระทบที่ไม่พึงประสงค์ (LOAEL) ที่ 10 ppm สำหรับความเสียหายของปอด
หนูทดลองได้รับน้ำดื่มที่มี UC-1 สูงถึง 40 ppm เป็นเวลา 90 วัน ความเข้มข้นดังกล่าวไม่แสดงความเป็นพิษในการทดสอบความเป็นพิษทางปากแบบกึ่งเรื้อรัง Daniel et al. [24] รายงานความเป็นพิษของคลอรีนไดออกไซด์ในน้ำดื่มที่ให้แก่หนู Sprague–Dawley เป็นเวลา 90 วัน โดยพวกเขาใช้ความเข้มข้นของคลอรีนไดออกไซด์ที่แตกต่างกัน (0, 25, 50, 100 และ 200 มก./ลิตร ซึ่งสอดคล้องกับปริมาณ 0, 2, 5, 8 และ 15 มก./กก.·วัน) น้ำหนักของม้ามและตับลดลงอย่างมีนัยสำคัญที่ 25 และ 50 มก./ลิตร ตามลำดับ พวกเขาพบรอยโรคในจมูกที่เกิดจากไอระเหยของคลอรีนไดออกไซด์ 25 มก./ลิตร ในน้ำดื่ม ในการศึกษาครั้งนั้น LOAEL คือ 25 มก./ลิตร Bercz et al. [25] ได้ทำการทดสอบที่คล้ายกันในลิงเขียวแอฟริกัน (Cercopithecus aethiops) โดยใช้คลอรีนไดออกไซด์ 0, 30, 100 และ 200 มก./ลิตร เป็นเวลา 4–6 สัปดาห์
นอกจากนี้ คลอรีนไดออกไซด์ 200 มก./ลิตร ทำให้เกิดผื่นแดงและแผลในช่องปาก หลังจาก 1 สัปดาห์ และคลอรีนไดออกไซด์ 100 มก./ลิตร ลดระดับไทรอกซิน (T4) ในซีรั่มหลังจาก 6 สัปดาห์ ในการศึกษานั้น NOAEL คือ 30 มก./ลิตร และ LOAEL คือ 100 มก./ลิตร สำหรับการสัมผัสทางปากของลิง
บทสรุป
UC-1 ผลิตขึ้นด้วยกระบวนการที่เป็นมิตรต่อสิ่งแวดล้อม โดยใช้วัตถุดิบและขั้นตอนการผลิตที่สะอาด สารละลาย UC-1 แสดงให้เห็นถึงฤทธิ์ต้านแบคทีเรีย เชื้อรา และไวรัสที่น่าพอใจ มีความเป็นพิษต่ำ ซึ่งแสดงให้เห็นได้จากการทดสอบความเป็นพิษต่อเซลล์ในหลอดทดลอง (ค่า IC50 สูง 765 ± 18 ppm) ClO2 50 ppm ไม่ทำให้เกิดการระคายเคืองตาในการทดสอบการระคายเคืองตา หนูไม่แสดงอาการผิดปกติและไม่ตายใน
การทดสอบความเป็นพิษจากการสูดดม ClO2 20 ppm และความเข้มข้นของ UC-1 สูงถึง 40 ppm ไม่เป็นพิษต่อหนูเป็นเวลา 90 วันในการทดสอบความเป็นพิษทางปากแบบเรื้อรัง ดังนั้น จึงแสดงให้เห็นถึงความปลอดภัยที่สูงกว่าของ UC-1 เมื่อเทียบกับผลการศึกษาในอดีต
กิตติกรรมประกาศ
เราขอขอบคุณบริษัท Unique Biotech Co. Ltd. ที่ให้การสนับสนุนโซลูชัน UC-1 งานวิจัยนี้ไม่ได้รับการสนับสนุนทางการเงินใดๆ จากหน่วยงานภาครัฐ ภาคเอกชน หรือภาคไม่แสวงหาผลกำไร
การมีส่วนร่วมของผู้เขียน: Hao-Chang Yin และ Shan-Shue Wang มีส่วนร่วมในการออกแบบการวิจัย การอภิปราย การวิเคราะห์ การตัดสินใจ การแก้ไข และการจัดหาเงินทุน Jui-Wen Ma และ Bin-Syuan Huang ประมวลผลข้อมูล ดำเนินการทดลองส่วนใหญ่ และเขียนต้นฉบับ Chu-Wei Hsu, Chun-Wei Peng และ Ming-Long Cheng ช่วยดำเนินการทดลองโดยละเอียด รวมถึงการรวบรวมและจัดการข้อมูล Jung-Yie Kao และ Tzong-Der Way เป็นที่ปรึกษาทางเทคนิคและผู้ประสานงานการศึกษา และให้คำแนะนำที่เป็นประโยชน์สำหรับการออกแบบการทดลอง ความคิดเห็นใหม่ๆ สำหรับการศึกษา และการทำงานร่วมกับห้องปฏิบัติการอื่นๆ
ความขัดแย้งทางผลประโยชน์: ผู้เขียนขอประกาศว่าไม่มีความขัดแย้งทางผลประโยชน์ใดๆ
เอกสารอ้างอิง
1. Sanekata, T.; Fukuda, T.; Miura, T.; Morino, H.; Lee, C.; Maeda, K.; Araki, K.; Otake, T.; Kawahata, T.; Shibata, T. การประเมินฤทธิ์ต้านไวรัสของคลอรีนไดออกไซด์และโซเดียมไฮโปคลอไรต์ต่อไวรัส
calicivirus ในแมว, ไวรัสไข้หวัดใหญ่ในมนุษย์, ไวรัสโรคหัด, ไวรัสไข้หัดสุนัข, ไวรัสเริมในมนุษย์, ไวรัสอะดีโนในมนุษย์, ไวรัสอะดีโนในสุนัข และไวรัสพาร์โวในสุนัข Biocontrol Sci. 2010, 15, 45–49. [CrossRef] [PubMed]
2. Ogata, N.; Shibata, T. ผลการป้องกันของก๊าซคลอรีนไดออกไซด์ความเข้มข้นต่ำต่อการติดเชื้อไวรัสไข้หวัดใหญ่ชนิดเอ J. Gen. Virol. 2008, 89, 60–67. [CrossRef] [PubMed]
3. Morino, H.; Fukuda, T.; Miura, T.; Lee, C.; Shibata, T.; Sanekata, T. การทำให้ไวรัส feline calicivirus ซึ่งเป็นตัวแทนของ norovirus ไม่ทำงานโดยก๊าซคลอรีนไดออกไซด์ Biocontrol Sci. 2009, 14, 147–153. [CrossRef] [PubMed]
4. Tanner, R.S. การทดสอบเปรียบเทียบและการประเมินสารฆ่าเชื้อบนพื้นผิวแข็ง J. Ind. Microbiol. 1989, 4, 145–154. [CrossRef]
5. Junli, H.; Li, W.; Nenqi, R.; Li, L.X.; Fun, S.R.; Guanle, Y. ผลการฆ่าเชื้อของคลอรีนไดออกไซด์ต่อไวรัสสาหร่าย และแพลงก์ตอนสัตว์ในน้ำ Water Res. 1997, 31, 455–460. [CrossRef]
6. Kim, J.; Marshall, M.R.; Du, W.X.; Otwell, W.S.; Wei, C.I. การหาปริมาณคลอเรตและคลอไรต์และการกลายพันธุ์ของอาหารทะเลที่ผ่านการบำบัดด้วยคลอรีนไดออกไซด์ในน้ำ J. Agric. Food Chem. 1999, 47, 3586–3591. [CrossRef] [PubMed]
7. Hubbard, H.; Poppendieck, D.; Corsi, R.L. ปฏิกิริยาของคลอรีนไดออกไซด์กับวัสดุภายในอาคารระหว่างการฆ่าเชื้ออาคาร: การดูดซึมบนพื้นผิว Environ. Sci. Technol. 2009, 43, 1329–1335. [CrossRef] [PubMed]
8. Yu, C.H.; Huang, T.C.; Chung, C.C.; Huang, H.H.; Chen, H.H. การประยุกต์ใช้คลอรีนไดออกไซด์ที่บริสุทธิ์สูงด้วยกระบวนการอิเล็กโทรไลซิสสำหรับการฆ่าเชื้อเนื้อปลานิล Sci. World J. 2014. [CrossRef] [PubMed]
9. Choi, S.; Park, S.; Kim, Y.; Kim, B.S.; Beuchat, L.R.; Hoikyung, K.; Ryu, J.H. การลดจำนวน Salmonella enterica บนผิวเปลือกไข่ด้วยการบำบัดด้วยคลอรีนไดออกไซด์ในน้ำและการทำให้แห้งตามลำดับ Int. J. Food Microbiol. 2015, 210, 84–87. [CrossRef] [PubMed]
10. Smith, D.J.; Ernst, W.; Herges, G.R. สารตกค้างของคลอรอกซีแอนไอออนในแคนตาลูปและมะเขือเทศหลังจากการฆ่าเชื้อด้วยก๊าซคลอรีนไดออกไซด์ J. Agric. Food Chem. 2015, 63, 9640–9649. [CrossRef] [PubMed]
11. Hsu, C.S.; Chen, I.M.; Liang, C.K.; Shih, C.H. การประเมินประสิทธิภาพการฆ่าเชื้อในโรงพยาบาลสัตว์โดยใช้คลอรีนไดออกไซด์ Sustain. Environ. Res. 2016, 26, 191–195. [CrossRef]
12. Hsu, M.S.; Wu, M.Y.; Huang, Y.T.; Liao, C.H. ประสิทธิภาพของการฆ่าเชื้อด้วยคลอรีนไดออกไซด์ต่อแบคทีเรียแกรมลบที่ไม่หมัก และไมโคแบคทีเรียที่ไม่ใช่วัณโรคในระบบน้ำของโรงพยาบาล J. Hosp. Infect. 2016, 93, 22–28. [CrossRef] [PubMed]
13. Yeturu, S.K.; Acharya, S.; Urala, A.S.; Pentapati, K.C. ผลของว่านหางจระเข้ คลอรีนไดออกไซด์ และคลอร์เฮกซิดีนน้ำยาบ้วนปากต่อคราบจุลินทรีย์และโรคเหงือกอักเสบ: การทดลองแบบสุ่มควบคุม J. Oral Biol. Craniofac. Res. 2016, 6, 54–58. [CrossRef] [PubMed]
14. สำนักงานคุ้มครองสิ่งแวดล้อมแห่งสหรัฐอเมริกา กฎระเบียบเกี่ยวกับจุลินทรีย์และผลพลอยได้จากการฆ่าเชื้อ การปฏิบัติตามพร้อมกัน คู่มือแนะนำ; สำนักงานคุ้มครองสิ่งแวดล้อมแห่งสหรัฐอเมริกา: วอชิงตัน ดี.ซี. สหรัฐอเมริกา, 1999.
15. Couri, D.; Abdel-Rahman, M.S.; Bull, R.J. ผลกระทบทางพิษวิทยาของคลอรีนไดออกไซด์ คลอไรต์ และคลอเรต Environ. Health Perspect. 1982, 46, 13–17. [CrossRef] [PubMed]
16. วิธีมาตรฐานสำหรับการตรวจสอบน้ำและน้ำเสีย ฉบับที่ 19; สมาคมสาธารณสุขแห่งอเมริกา: วอชิงตัน ดี.ซี. สหรัฐอเมริกา; สมาคมการประปาแห่งอเมริกา: วอชิงตัน ดี.ซี. สหรัฐอเมริกา; สหพันธ์สิ่งแวดล้อมทางน้ำ: อเล็กซานเดรีย เวอร์จิเนีย สหรัฐอเมริกา 1995
17. ตำราเภสัชกรรมสหรัฐอเมริกา 34 NF29 การทดสอบทางจุลชีววิทยา/<51> การทดสอบประสิทธิภาพยาต้านจุลชีพ; การประชุมตำราเภสัชกรรมสหรัฐอเมริกา: ร็อกวิลล์ แมริแลนด์ สหรัฐอเมริกา
18. Trinetta, V.; Morgan, M.; Linton, R.; Dermirci, A.; Ngadi, M.O. คลอรีนไดออกไซด์สำหรับการฆ่าเชื้อจุลินทรีย์ในอาหาร ในการฆ่าเชื้อจุลินทรีย์ในอุตสาหกรรมอาหาร; Demirci, A., Ngadi, M.O., บรรณาธิการ; สำนักพิมพ์ Woodhead: เคมบริดจ์ สหราชอาณาจักร 2012; หน้า 533–562
19. Sorlini, S.; Gialdini, F.; Biasibetti, M.; Collivignarelli, C. อิทธิพลของการบำบัดน้ำดื่มต่อการบริโภคคลอรีนไดออกไซด์และการก่อตัวของคลอไรต์/คลอเรต Water Res. 2014, 54, 44–52. [CrossRef] [PubMed]
20. Park, S.H.; Kang, D.H. ผลต้านจุลชีพของก๊าซคลอรีนไดออกไซด์ต่อเชื้อก่อโรคในอาหารภายใต้สภาวะความชื้นสัมพัทธ์ที่แตกต่างกัน LWT- Food Sci. Technol. 2015, 60, 186–191. [CrossRef]
21. Arango, J.; Rubino, M.; Auras, R.; Gillett, J.; Schilder, A.; Grzesiak, A.L. การประเมินคลอรีนไดออกไซด์ในฐานะสารต้านจุลชีพต่อ Botrytis cinerea ในสตรอว์เบอร์รีแคลิฟอร์เนีย Food Packag. Shelf Life 2016, 9, 45–54. [CrossRef]
22. Paulet, G.D.; Desbrousses, S. ผลกระทบของ ClO2 ที่ความเข้มข้นต่ำต่อสัตว์ทดลอง Arch. Mal. Prof. 1970, 31, 97–106. [PubMed]
23. Paulet, G.D.; Desbrousses, S. ผลกระทบของการสัมผัสคลอรีนไดออกไซด์ (ClO2) แบบไม่ต่อเนื่องต่อหนู Arch. Mal. Prof. 1974, 35, 797–804.
24. Daniel, F.B.; Condie, L.W.; Robinson, M.; Stober, J.A.; York, R.G.; Olson, G.R.; Wang, S.R. การศึกษาเปรียบเทียบความเป็นพิษเรื้อรังของสารฆ่าเชื้อสามชนิด J. Am. Water Works Assn. 1990, 82, 61–69.
25. Bercz, J.P.; Jones, L.; Garner, L.; Murray, D.; Ludwig, D.A.; Boston, J. ความเป็นพิษเรื้อรังของคลอรีนไดออกไซด์ และสารประกอบที่เกี่ยวข้องในน้ำดื่มในลิงที่ไม่ใช่มนุษย์ Environ. Health Perspect. 1982, 46, 47–55. [CrossRef] [PubMed]