หน้าหลักนี้ประกอบด้วยเอกสารฉบับแปลของบทความวิชาการต้นฉบับ อย่างไรก็ตาม เรา ได้จัดทำสรุปเนื้อหาที่สำคัญแบบย่อยง่ายไว้ให้ผู้อ่านได้ศึกษาเป็นลำดับแรก เพื่อให้เข้าใจภาพรวมของงานวิจัยชิ้นนี้ได้อย่างรวดเร็ว หากท่านมีความสนใจในรายละเอียดเชิงลึกหรือข้อมูลทางสถิติเพิ่มเติม ท่านสามารถเลือกอ่านเอกสารฉบับเต็มได้ทั้งในรูปแบบภาษาอังกฤษ (Original) ได้ที่ลิงก์นี้: https://akjournals.com/view/journals/2060/107/1/article-p1.xml หรือหากต้องการอ่านฉบับภาษาไทย (Translated) เราได้จัดทำบทแปลไว้ให้แล้วในหน้านี้ (ล่างสุด)
บทความเรื่อง Can chlorine dioxide prevent the spreading of coronavirus or other viral infections? เป็นบทความเชิงสมมติฐานทางการแพทย์ (medical hypothesis) ที่นำเสนอแนวคิดเกี่ยวกับศักยภาพของ chlorine dioxide ในการยับยั้งหรือป้องกันการติดเชื้อไวรัส เช่น coronavirus โดยผู้เขียนอภิปรายจากหลักฐานทางชีวเคมีและจุลชีววิทยาที่มีอยู่ ซึ่งชี้ว่า chlorine dioxide เป็นสารออกซิไดซ์ที่สามารถทำลายโปรตีนของเชื้อโรค รวมถึงโปรตีนของไวรัสที่จำเป็นต่อการเข้าสู่เซลล์และการเพิ่มจำนวน จึงอาจมีบทบาทในการลดการแพร่กระจายของไวรัสได้ อย่างไรก็ตาม บทความนี้ไม่ได้เป็นการทดลองทางคลินิกโดยตรง และยังขาดหลักฐานเชิงประจักษ์ในมนุษย์ที่เพียงพอ ผู้เขียนจึงเน้นว่าข้อเสนอเหล่านี้ยังคงเป็นเพียงสมมติฐานที่ต้องได้รับการศึกษาวิจัยเพิ่มเติมเพื่อยืนยันทั้งประสิทธิภาพและความปลอดภัยก่อนนำไปใช้จริง
ข้อมูลการเผยแพร่
- ชื่อบทความ: Can chlorine dioxide prevent the spreading of coronavirus or other viral infections?
- ผู้เขียน: K. Kály-Kullai และคณะ
- ปีที่ตีพิมพ์: 2020
- วารสารที่ตีพิมพ์: Physiology International
บทนำ
แรงจูงใจ
ไวรัสได้ก่อให้เกิดโรคระบาดมากมายตลอดประวัติศาสตร์ของมนุษย์ ไวรัสโคโรนาสายพันธุ์ใหม่ เป็นเพียงตัวอย่างล่าสุด การระบาดของไวรัสสายพันธุ์ใหม่นั้นคาดเดาไม่ได้ และการพัฒนาเครื่องมือป้องกันและมาตรการตอบโต้เฉพาะเจาะจงต่อไวรัสสายพันธุ์ใหม่ยังคงต้องใช้เวลานานแม้ในยุคปัจจุบันของวิทยาศาสตร์และเทคโนโลยีทางการแพทย์ที่ทันสมัย ในกรณีที่ไม่มีตัวยาหรือวัคซีนที่มีประสิทธิภาพและเฉพาะเจาะจง การมีโปรโตคอลหรือสารที่ไม่เฉพาะเจาะจงเพื่อทำให้ไวรัสไม่ทำงาน ซึ่งเป็นสาร/โปรโตคอลที่สามารถนำมาใช้ได้ทุกครั้งที่เกิดการระบาดของไวรัสสายพันธุ์ใหม่ จะเป็นที่พึงปรารถนา สิ่งนี้มีความสำคัญอย่างยิ่งในกรณีที่ไวรัสสายพันธุ์ใหม่ที่เกิดขึ้นนั้นแพร่เชื้อได้ง่ายเช่นเดียวกับ SARS-CoV-2
วัตถุประสงค์และโครงสร้างของเอกสารฉบับนี้
ในบทบรรณาธิการนี้ เราเสนอให้พิจารณาความเป็นไปได้ในการพัฒนาและนำโปรโตคอลต้านไวรัสมาใช้โดยใช้สารละลายคลอรีนไดออกไซด์ (ClO2) ที่มีความบริสุทธิ์สูง จุดมุ่งหมายของข้อเสนอนี้คือการเริ่มต้นการวิจัยที่อาจนำไปสู่การนำโปรโตคอลต้านไวรัสที่ใช้งานได้จริงและมีประสิทธิภาพมาใช้ เพื่อบรรลุเป้าหมายนี้ เราจะกล่าวถึงคุณสมบัติที่สำคัญบางประการของโมเลกุล ClO2 ซึ่งทำให้มันเป็นสารต้านไวรัสที่มีประโยชน์ จากนั้นจะทบทวนผลลัพธ์ก่อนหน้านี้ของการประยุกต์ใช้ก๊าซ ClO2 กับไวรัส สุดท้าย เราตั้งสมมติฐานเกี่ยวกับวิธีการควบคุมการแพร่กระจายของการติดเชื้อไวรัสโดยใช้สารละลาย ClO2 ในน้ำ
ประสบการณ์และภูมิหลังในการใช้ ClO2 เป็นสารต้านไวรัส
การทำให้ไวรัสไม่ทำงานด้วย ClO2 ในเฟสของเหลว
จากความรู้ในปัจจุบัน สารละลาย ClO2 ในน้ำสามารถยับยั้งไวรัสได้ทุกประเภทสารฆ่าเชื้อ (ในเฟสน้ำ) จะถูกเปรียบเทียบโดยค่า CT ซึ่งเป็นความเข้มข้น (วัดเป็น mg/L) คูณด้วยเวลาสัมผัส (วัดเป็นนาที) ในตาราง CT ClO2 จะถูกระบุสำหรับไวรัสโดยทั่วไป โดยไม่กล่าวถึงข้อยกเว้นใดๆ ตัวอย่างเช่น ตาม ต้องใช้ค่า CT 8.4 mg 3 min/L เพื่อให้ได้การยับยั้งไวรัสสี่ลำดับความแรง (“4 log” หรือ “99.99%”) ในตัวกลางที่เป็นน้ำที่อุณหภูมิ 25 8C
กลไกทางเคมีในการยับยั้งการทำงานของไวรัส: ปฏิกิริยาของ ClO2 กับกรดอะมิโนตกค้าง
ในปี พ.ศ. 2529 Noss และคณะ พิสูจน์ว่าการทำให้ไวรัสแบคทีเรีย f2 ไม่ทำงานโดย ClO2 เกิดจากปฏิกิริยาของมันกับโปรตีนแคปซิดของไวรัส และแทบไม่มีการทำให้ RNA ของไวรัสที่ก่อให้เกิดการติดเชื้อไม่ทำงาน [8] เมื่อ RNA นั้นได้รับการบำบัดด้วย ClO2 แยกต่างหาก อย่างไรก็ตาม พวกเขาพบว่าส่วนประกอบทางเคมีที่แยกจากกันสามส่วนในโปรตีนของไวรัส ได้แก่ ซิสเทอีน ไทโรซีน และทริปโตแฟน
กรดอะมิโน สามารถทำปฏิกิริยากับ ClO2 ได้อย่างรวดเร็ว ในปี พ.ศ. 2530 Tan และคณะ ทดสอบปฏิกิริยาของ ClO2 กับกรดอะมิโนอิสระ 21 ชนิด ClO2 ทำปฏิกิริยากับกรดอะมิโนเพียงหกชนิดที่ละลายในบัฟเฟอร์โซเดียมฟอสเฟต 0.1 M ที่ pH 6.0 ปฏิกิริยากับซิสเทอีน ทริปโตแฟน และไทโรซีนนั้น เร็วเกินกว่าที่จะติดตามได้ด้วยเทคนิคของพวกเขา กรดอะมิโนอีกสามชนิด (ฮิสติดีน ไฮดรอกซีโพรลีน และโพรลีน) ทำปฏิกิริยากับ ClO2 ช้ากว่ามาก แต่ในอัตราที่สามารถวัดได้
ปฏิกิริยาของกรดอะมิโนที่มีปฏิกิริยาเร็ว 3 ชนิด (ซิสเทอีน ไทโรซีน และทริปโตแฟน) ได้รับการศึกษาในห้องปฏิบัติการของ Margerum ระหว่างปี 2005 ถึง 2008 พวกเขาพบว่าซิสเทอีนมีปฏิกิริยาสูงที่สุดในบรรดากรดอะมิโนเหล่านี้ จากข้อมูลการทดลองของพวกเขา พวกเขาคำนวณค่าคงที่อัตราอันดับสอง (ที่ pH 7.0, 25 8C และความแรงไอออน 1 M) และได้ลำดับดังต่อไปนี้:
![]()
ในปี 2550 Ogata พบว่าฤทธิ์ต้านจุลชีพของ ClO2 ขึ้นอยู่กับการทำให้โปรตีนบางชนิดเสียสภาพ ซึ่งส่วนใหญ่เกิดจากการดัดแปลงออกซิเดชันของกรดอะมิโนทริปโตเฟนและไทโรซีนของโปรตีนต้นแบบสองชนิด (อัลบูมินในซีรั่มวัวและกลูโคส-6-ฟอสเฟตดีไฮโดรจีเนส) ที่ใช้ในการทดลองของเขา ในปี 2555 Ogata ก็ได้แสดงให้เห็นอีกครั้ง ว่าการทำให้ไวรัสไข้หวัดใหญ่ไม่ทำงานโดย ClO2 เกิดจากการออกซิเดชันของกรดอะมิโนทริปโตเฟน (W153) ในเฮมากลูตินิน (โปรตีนหนามของไวรัส) ซึ่งทำให้ความสามารถในการจับกับตัวรับของไวรัสหายไป
เฮมากลูตินิน (โปรตีนหนามของไวรัส) จึงทำให้ความสามารถในการจับกับตัวรับของไวรัสหมดไป ในบริบทนี้ เป็นที่น่าสนใจที่จะสังเกตว่าโปรตีนหนามของไวรัสโคโรนาสายพันธุ์ใหม่ SARS_CoV-2 ประกอบด้วยไทโรซีน 54 ตัว ทริปโตแฟน 12 ตัว และซิสเทอีน 40 ตัว หากเราสมมติว่าในสารละลายในน้ำ กรดอะมิโนเหล่านี้ทั้งหมดสามารถทำปฏิกิริยากับ ClO2 ได้เช่นเดียวกับกรดอะมิโนอิสระ แล้วการยับยั้งไวรัสจะเกิดขึ้นอย่างรวดเร็วมากแม้ในสารละลาย ClO2 ที่เจือจางมาก (เช่น ในสารละลาย ClO2 0.1 มก./ลิตร)
ClO2 เป็นก๊าซที่ละลายน้ำได้
แม้ว่าคลอรีนไดออกไซด์จะเป็นก๊าซ แต่ก็ละลายได้ดีในน้ำ เมื่อมีทั้งอากาศและน้ำอยู่ด้วยกัน ClO2 จะกระจายตัวระหว่างสองเฟสในอัตราส่วนสมดุลที่กำหนดโดยอุณหภูมิ ค่าสัมประสิทธิ์การกระจายตัวของ ClO2 นี้ถูกกำหนดโดย Ishi ในปี 1958 ค่าสัมประสิทธิ์การกระจายตัว g = [ClO2]G/[ClO2]L แสดงถึงอัตราส่วนของความเข้มข้นที่แสดงในหน่วยเดียวกันในเฟสก๊าซและเฟสของเหลว (เช่น g/L) และเปลี่ยนแปลงไปตามอุณหภูมิ ตัวอย่างเช่น ที่ 20 8C g = 0.0316 ซึ่งแสดงว่าในสภาวะสมดุล เฟสของเหลว 1 cm3 จะมีโมเลกุล ClO2 มากกว่าเฟสก๊าซ 1 cm3 ถึง (0.0316) 1 5 31.6 เท่า
ในทางปฏิบัติ ความเข้มข้นในสองเฟสมักจะระบุเป็น ppm อย่างไรก็ตาม ตัวเลขไร้มิติเหล่านี้ถูกกำหนดในเฟสแก๊สและของเหลวแตกต่างกัน โดยเป็น ppm (V/V) และ ppm (m/m) ตามลำดับ ดังนั้น เพื่อประโยชน์ในทางปฏิบัติ เราจึงต้องการสัมประสิทธิ์การกระจาย ซึ่งแสดงอัตราส่วนระหว่างความเข้มข้นเหล่านี้ การคำนวณอย่างตรงไปตรงมาพบว่า สัมประสิทธิ์การกระจายในหน่วย ppm มีค่าเป็น 357 เท่าของสัมประสิทธิ์การกระจายในหน่วย g/L ดังนั้นที่ 20 8C gppm 5 11.3 ดังนั้น สูตรต่อไปนี้สามารถใช้คำนวณความเข้มข้นของ ClO2 ในเฟสแก๊สที่อยู่ในสมดุลกับสารละลาย ClO2 ที่ 20 8C ได้:
![]()
การทำให้ไวรัสไม่ทำงานด้วย ClO2 ในสถานะก๊าซ
ปฏิกิริยาที่ทำให้ไวรัสไม่ทำงาน (ปฏิกิริยาของ ClO2 กับกรดอะมิโนทั้งสามชนิด) เกิดขึ้นในตัวกลางที่เป็นน้ำ ดังนั้น ClO2 จึงสามารถทำให้จุลินทรีย์ไม่ทำงานได้เฉพาะในสภาวะเปียกเท่านั้น ด้วยเหตุนี้ ก๊าซ ClO2 ที่มีความชื้นจึงเป็นสารที่เหมาะสมในการต่อต้านไวรัสทั้งในสภาวะเปียก และแห้ง ไวรัสที่ถูกพาไปกับหยดน้ำสามารถถูกทำให้ไม่ทำงานได้ง่ายแม้กระทั่งโดยก๊าซ ClO2 เนื่องจาก ClO2 ละลายน้ำได้สูง ก๊าซ ClO2 ที่แห้งจะไม่เหมาะสม เนื่องจากปริมาณน้ำในหยดน้ำอาจระเหยไป และในกรณีที่ไม่มีตัวกลางที่เป็นน้ำ ปฏิกิริยาของ ClO2 จะช้าลงอย่างมาก อันที่จริง Morino et al. รายงานว่าเมื่อใช้ ClO2 ความเข้มข้นต่ำในเฟสแก๊สต่อต้าน FCV ในสภาวะแห้งความชื้นในบรรยากาศ – อย่างน้อย 75–85% ความชื้นสัมพัทธ์ – เป็นสิ่งจำเป็นในการทำให้ไวรัสไม่ทำงาน ข้อดีของการใช้ก๊าซ ClO2 ที่มีความชื้นคือ ปริมาณน้ำในก๊าซนั้นสามารถทำให้ไวรัสเปียกได้ในสภาพแวดล้อมที่แห้ง
ไวรัสส่วนใหญ่พบอยู่บนพื้นผิวแข็งภายในอาคาร แต่ไวรัสส่วนน้อยจะ “ลอยอยู่ในอากาศ” เกาะติดกับอนุภาคฝุ่น ซึ่งอาจมีจุลินทรีย์เดี่ยวๆ หรือกลุ่มของจุลินทรีย์อยู่ด้วย ดังนั้น การทำให้จุลินทรีย์ทั้งหมดในทุกส่วนของห้องเปียกและสัมผัสกับ ClO2 จึงเป็นสิ่งจำเป็นสำหรับการฆ่าเชื้อที่มีประสิทธิภาพ หากฉีดพ่นสารละลาย ClO2 ในน้ำเข้าไปในห้องมากพอ หยดน้ำจะทำให้บรรยากาศอิ่มตัวด้วยไอน้ำไปทั่วทุกหนแห่ง นอกจากนี้ บรรยากาศยังจะมีก๊าซ ClO2 อยู่ทั่วทุกหนแห่งด้วย ข้อดีอย่างมากของวิธีนี้คือ โมเลกุลของ H2O และ ClO2 ในสถานะก๊าซสามารถเข้าถึงจุลินทรีย์ในทุกซอกทุกมุมของห้องได้ หยดน้ำที่กระจายตัวอย่างละเอียดซึ่งมี ClO2 ละลายอยู่ สามารถสร้างสภาพแวดล้อมที่เอื้ออำนวยต่อการรักษาสภาพเช่นนี้ได้นานขึ้น
วิธีนี้ใช้ความเข้มข้นของ ClO2 สูง ช่วยให้สามารถฆ่าเชื้อในห้องได้อย่างรวดเร็วเมื่อไม่มีคนอยู่ เช่น ห้องผู้ป่วยหนัก อาคารที่ใช้เป็นสถานที่กักกัน หรือยานพาหนะขนส่งสาธารณะ อย่างไรก็ตาม การใช้ก๊าซ ClO2 มีข้อจำกัดเมื่อมีคนอยู่ เนื่องจากเป็นอันตรายต่อมนุษย์และสัตว์ที่ความเข้มข้นสูงกว่าระดับหนึ่ง สำนักงานความปลอดภัยและอาชีวอนามัยแห่งสหรัฐอเมริกา (OSHA) จำกัดความเข้มข้นของก๊าซ ClO2 ที่อนุญาตในอากาศในที่ทำงานไว้ที่ 0.1 ppm (V/V) ค่าเฉลี่ยถ่วงน้ำหนักตามเวลา (TWA) สำหรับการสัมผัส 8 ชั่วโมง และที่ขีดจำกัดการสัมผัสระยะสั้น (STEL) ที่สูงขึ้นชั่วคราวที่ 0.3 ppm เฉพาะในช่วงเวลา 15 นาทีเท่านั้น
งานวิจัยก่อนหน้านี้เกี่ยวกับการป้องกันการติดเชื้อไวรัสด้วยก๊าซ ClO2
Ogata ตระหนักเป็นครั้งแรกว่า ClO2 สามารถทำให้ไวรัสไม่ทำงานได้แม้ภายใต้ขีดจำกัด 0.1 ppm (OSHATWA) ซึ่งเป็นความเข้มข้นที่ไม่เป็นอันตรายต่อมนุษย์ ในปี 2551 Ogata และ Shibata ได้แสดงให้เห็นว่าการติดเชื้อไวรัสไข้หวัดใหญ่ A ในหนูทดลองที่ใช้ในรูปแบบละอองลอย สามารถป้องกันได้ด้วยก๊าซ ClO2 ที่มีความเข้มข้น 0.03 ppm ในอากาศ ซึ่งเป็นเพียง 30% ของระดับการสัมผัส TWA ที่อนุญาตสำหรับมนุษย์ในสถานที่ทำงาน พวกเขาสรุปว่า “ก๊าซ ClO2 จึงอาจมีประโยชน์ในฐานะเครื่องมือป้องกันไข้หวัดใหญ่ในสถานที่ที่มีกิจกรรมของมนุษย์ โดยไม่จำเป็นต้องอพยพ” พวกเขายังได้พยายามลดอุบัติการณ์ของการติดเชื้อไข้หวัดใหญ่ในหมู่นักเรียนโดยการใช้ก๊าซ ClO2 ที่มีความเข้มข้นต่ำในห้องเรียน
แม้ว่าผลลัพธ์เบื้องต้นเหล่านี้จะดูดี แต่เราไม่ทราบว่ามีการนำวิธีการนี้ไปใช้ในวงกว้างในช่วงทศวรรษที่ผ่านมาหรือไม่ มีปัญหาอยู่สองประการที่อาจขัดขวางการนำวิธีการนี้ไปใช้อย่างแพร่หลาย:
1. ด้วยเทคนิคที่ผู้เขียนที่กล่าวถึงข้างต้นนำมาใช้ การบรรลุและคงระดับความเข้มข้นของ ClO2 ที่ต่ำมากในพื้นที่ขนาดใหญ่และเป็นเวลานานนั้นไม่ใช่เรื่องง่าย ซึ่งเป็นเงื่อนไขเบื้องต้นในการบรรลุระดับการยับยั้งไวรัสที่น่าพอใจ
2. ยังไม่เป็นที่เข้าใจว่าเหตุใดระดับ ClO2 ที่ต่ำจึงไม่เป็นอันตรายต่อมนุษย์หรือสัตว์ แต่ยังคงมีประสิทธิภาพในการต่อต้านไวรัส
ผลกระทบการเลือกขนาดของ
แม้ว่าสารตกค้างของซิสเทอีน ไทโรซีน และทริปโตแฟนจะพบได้ในเนื้อเยื่อของมนุษย์เช่นกัน แต่ ClO2 มีความเป็นพิษต่อมนุษย์หรือสัตว์น้อยกว่าจุลินทรีย์ (แบคทีเรีย เชื้อรา และไวรัส) มาก Noszticzius et al. พบว่าเหตุผลหลักสำหรับการเลือกสรรระหว่างมนุษย์และจุลินทรีย์นั้นไม่ได้ขึ้นอยู่กับชีวเคมีที่แตกต่างกัน แต่ขึ้นอยู่กับขนาดที่แตกต่างกัน จากการทดลองและการคำนวณโดยใช้แบบจำลองปฏิกิริยา-การแพร่กระจาย Noszticzius et al. พบว่าเวลาในการฆ่าสิ่งมีชีวิตเป็นสัดส่วนกับกำลังสองของขนาดลักษณะเฉพาะ (เช่น เส้นผ่านศูนย์กลาง) ดังนั้นสิ่งมีชีวิตขนาดเล็กจะถูกฆ่าอย่างรวดเร็วมาก การคำนวณของพวกเขาแสดงให้เห็นว่าแบคทีเรียขนาดเส้นผ่านศูนย์กลาง 1 มิลลิเมตรจะถูกฆ่าในสารละลาย ClO2 ความเข้มข้น 300 มิลลิกรัม/ลิตร ภายใน 3 มิลลิวินาที และแม้แต่ในสารละลาย ClO2 ที่เจือจางกว่ามาก คือ 0.25 มิลลิกรัม/ลิตร ก็จะถูกกำจัดได้ภายในเวลาเพียง 3.6 วินาที ในช่วงเวลานี้ ClO2 จะเข้าถึงทุกส่วนของเซลล์และฆ่าเซลล์โดยการทำลายโปรตีนที่มีซิสเทอีน ไทโรซีน และทริปโตเฟน ซึ่งจำเป็นต่อกระบวนการดำรงชีวิต
บทบาทในการปกป้องเซลล์สิ่งมีชีวิตจากการเกิดออกซิเดชันของ ClO2 โดยกลูตาไธโอน
ตามที่ Ison et al. ระบุไว้ กลูตาไธโอนทำปฏิกิริยากับ ClO2 ในอัตราที่สูงกว่าอัตราของปฏิกิริยา ClO2 – ซิสเทอีนที่เกิดขึ้นอย่างรวดเร็วมาก เมื่อ ClO2 สัมผัสกับเซลล์ที่มีชีวิตซึ่งมีกลูตาไธโอนอยู่ ในตอนแรกความเข้มข้นของ ClO2 จะยังคงต่ำมากแม้กระทั่ง ณ จุดที่เข้าสู่เซลล์เนื่องจากปฏิกิริยาที่รวดเร็วนี้ เนื่องจากเป็นโมเลกุลขนาดเล็ก กลูตาไธโอนจึงสามารถแพร่กระจายไปยังจุดที่เข้าจากส่วนอื่นๆ ของเซลล์ได้อย่างรวดเร็ว โดยบริโภค ClO2 ส่วนใหญ่ที่นั่น และป้องกันไม่ให้ ClO2 ไปถึงซิสเทอีน ไทโรซีน และทริปโตแฟนของโปรตีนในไซโตพลาซึมส่วนใหญ่ ดังนั้น ความเข้มข้นของ ClO2 ที่ต่ำในตอนแรกจึงไม่ก่อให้เกิดอันตรายมากนัก
อย่างไรก็ตาม การที่ ClO2 เข้าสู่เซลล์อย่างต่อเนื่องอาจทำให้เซลล์สูญเสียกลูตาไธโอน (และสารต้านอนุมูลอิสระอื่นๆ) ในที่สุด แม้ว่าเซลล์จะผลิตสารต้านอนุมูลอิสระเหล่านั้นอย่างต่อเนื่องก็ตาม ณ จุดนี้ ClO2 สามารถ
เข้าสู่บริเวณที่เคยได้รับการปกป้องของเซลล์และทำปฏิกิริยากับกรดอะมิโนที่ไวต่อปฏิกิริยาทำให้โปรตีนที่ได้รับผลกระทบเสียสภาพและในที่สุดก็ทำให้เซลล์ตาย
ผลของกลูตาไธโอนและโมเลกุลต้านอนุมูลอิสระขนาดเล็กอื่นๆ ที่มีอยู่ในเซลล์ที่มีชีวิตไม่ได้ถูกนำมาพิจารณาในการคำนวณทางทฤษฎีของ Noszticzius et al. การทดลองของพวกเขาทำบนเยื่อหุ้มเซลล์สัตว์ที่ไม่มีชีวิตและถูกล้าง ซึ่งมีโปรตีนที่ทำปฏิกิริยากับเยื่อหุ้มเซลล์อยู่ แต่ไม่มีกลูตาไธโอนและโมเลกุลขนาดเล็กอื่นๆ อย่างไรก็ตาม เซลล์ที่มีชีวิตจะผลิตสารต้านอนุมูลอิสระเหล่านี้อย่างต่อเนื่อง ดังนั้นบทบาทของพวกมันจึงไม่สามารถละเลยได้ อันที่จริง เมื่อพิจารณาจากพลวัตการฆ่าเชื้อที่วัดได้จากการทดลองของสารละลาย ClO2 0.25 มก./ลิตร ต่อแบคทีเรีย Escherichia coli เราจะเห็นอัตราการฆ่าเชื้อซึ่งเร็วอย่างน่าประหลาดใจ แต่ยังคงช้ากว่าการประมาณทางทฤษฎีประมาณหนึ่งลำดับขนาด เป็นเรื่องสมเหตุสมผลที่จะสันนิษฐานว่าผลหน่วงเวลาของโมเลกุลรีดิวซ์ขนาดเล็กเหล่านี้เป็นสาเหตุของความเบี่ยงเบนนั้น
การปกป้องเนื้อเยื่อของมนุษย์จากผลกระทบออกซิเดชันของ ClO2
เซลล์ของมนุษย์ยังมีกลูตาไธโอนในความเข้มข้นระดับมิลลิโมลาร์ รวมถึงสารต้านอนุมูลอิสระอื่นๆ เช่น วิตามินซีและอี ซึ่งทำงานร่วมกับกลูตาไธโอนเพื่อลด ClO2 เนื่องจากเซลล์ของมนุษย์มีขนาดใหญ่กว่าแบคทีเรียมาก ดังนั้นปริมาณกลูตาไธโอนสำรองและศักยภาพในการผลิตกลูตาไธโอนจึงมากกว่า แม้แต่เซลล์ของมนุษย์ที่แยกออกมาก็สามารถอยู่รอดได้นานกว่าในสภาพแวดล้อมที่มี ClO2 มากกว่าแบคทีเรียที่ลอยอยู่ในน้ำ เมื่อพิจารณาว่าเซลล์ของมนุษย์ไม่ได้แยกออกมาแต่รวมตัวกันเป็นเนื้อเยื่อ ปริมาณกลูตาไธโอนของเซลล์มนุษย์อาจมากกว่าแบคทีเรียที่ลอยอยู่ในน้ำหลายเท่า
นอกจากนี้ ในสิ่งมีชีวิตหลายเซลล์ การไหลเวียนโลหิตจะขนส่งสารต้านอนุมูลอิสระไปยังเซลล์ของเนื้อเยื่อที่ได้รับผลกระทบจากการโจมตีของ ClO2 อย่างต่อเนื่อง ช่วยให้เซลล์เหล่านั้นอยู่รอดได้ สิ่งนี้ช่วยเสริมผลของการเลือกขนาด และอธิบายการสังเกตที่น่าประหลาดใจ ที่ว่าสารละลาย ClO2 ที่สามารถฆ่าแบคทีเรียแพลงก์ตอนได้ในเวลาเพียงเสี้ยววินาที สามารถบริโภคได้ เนื่องจากปลอดภัยสำหรับมนุษย์ที่จะดื่มในปริมาณเล็กน้อย (เช่น การดื่มสารละลาย ClO2 24 มก./ล. ปริมาณ 1 ลิตร แบ่งเป็นสองส่วนในวันเดียว ไม่ก่อให้เกิดผลกระทบที่สังเกตได้ในมนุษย์)
ผลกระทบของ ClO2 ต่อปอด
แม้ว่าโดยทั่วไปเนื้อเยื่อของมนุษย์จะไม่ไวต่อ ClO2 มากนัก แต่ปอดควรได้รับการพิจารณาแตกต่างออกไป เนื่องจากเยื่อกั้นระหว่างถุงลมที่แยกช่องว่างอากาศของถุงลมออกจากกระแสเลือดของหลอดเลือดฝอยนั้นบางมาก อุปสรรคการแพร่กระจายในปอดของมนุษย์นั้นมีความหนาเพียง 2 มม. เพื่ออำนวยความสะดวกในการแลกเปลี่ยนออกซิเจนและคาร์บอนไดออกไซด์ระหว่างอากาศและเลือดอย่างมีประสิทธิภาพ ถุงลมถูกปกคลุมด้วยของเหลวบุผิวบาง ๆ ที่เรียกว่าของเหลวบุผิวปอด (ELF) หรือไฮโปเฟส ELF มีความหนาเพียง 0.2 มม. ในถุงลมของหนู ประกอบด้วยกลูตาไธโอน และสารต้านอนุมูลอิสระอื่น ๆ เช่น กรดแอสคอร์บิกและกรดยูริก เป็นที่น่าสังเกตว่าความเข้มข้นของกรดแอสคอร์บิกสูงกว่าในของเหลวในปอด (ELF) ถึง 2.5 เท่า และความเข้มข้นของกลูตาไธโอนสูงกว่าในพลาสมาถึง 100 เท่า หน้าที่ปกติของสารต้านอนุมูลอิสระที่ไม่ใช่เอนไซม์เหล่านี้ใน ELF คือการปกป้องเซลล์เยื่อบุผิวจากอนุมูลอิสระออกซิเจน (ROS) เช่น ซูเปอร์ออกไซด์หรือไฮโดรเจนเปอร์ออกไซด์ ซึ่งเป็นสารพิษที่เกิดจากกระบวนการเผาผลาญ นอกจากนี้ยังสามารถปกป้องปอดจากก๊าซพิษอื่นๆ เช่น โอโซน (O3) ไนโตรเจนไดออกไซด์ (NO2) หรือ ClO2
อย่างไรก็ตาม ClO2 ในปริมาณมากสามารถใช้สารรีดิวซ์ทั้งหมดใน ELF ได้ ซึ่งในจุดนี้ ClO2 จะเริ่มทำปฏิกิริยากับเซลล์เยื่อบุผิว ทำให้เกิดความเสียหายต่อเซลล์เหล่านี้อย่างต่อเนื่อง เป็นที่ทราบกันดีว่าก๊าซ ClO2 ในความเข้มข้นสูงอาจเป็นอันตรายถึงชีวิตได้ อย่างไรก็ตาม เป็นที่สมเหตุสมผลที่จะสันนิษฐานว่าผลกระทบของ ClO2 ต่อปอดนั้นขึ้นอยู่กับไม่เพียงแต่ความเข้มข้นในเฟสของก๊าซเท่านั้น แต่ยังขึ้นอยู่กับระยะเวลาการสัมผัสด้วย ดังนั้น เมื่อพิจารณาถึงผลกระทบของ ClO2 ต่อปอด จึงเป็นเรื่องสมเหตุสมผลที่จะพิจารณาผลคูณ CT (ความเข้มข้น) 3 (เวลาสัมผัส) ในลักษณะเดียวกับกรณีของจุลินทรีย์
การประมาณเวลาที่ไวรัสถูกทำลาย
ในกรณีของไวรัส กลไกการทำให้ไม่ทำงานจะแตกต่างจากแบคทีเรียหรือเซลล์อื่นๆ เป็นไปได้ที่จะสันนิษฐานว่าเวลาในการทำให้ไวรัสไม่ทำงานนั้นน่าจะสั้นกว่าเวลาในการทำให้แบคทีเรียไม่ทำงานภายใต้เงื่อนไขเดียวกัน (ความเข้มข้นของ ClO2 อุณหภูมิ ฯลฯ) มาก ข้อโต้แย้งต่อไปนี้สนับสนุนสมมติฐานนี้:
1. ไวรัสมีขนาดเล็กกว่าแบคทีเรียประมาณหนึ่งลำดับ เช่น เส้นผ่านศูนย์กลางของ SARS_CoV-2 อยู่ที่ประมาณ 120 นาโนเมตร เวลาในการฆ่าไวรัสตามที่แนะนำใน จะสั้นกว่าแบคทีเรีย 1-2 ลำดับ นั่นคือ ปฏิกิริยาที่ควบคุมโดยการแพร่กระจายกับ ClO2 จะเกิดขึ้นในช่วงเวลาที่สั้นกว่าในปริมาตรทั้งหมดของไวรัส
2. ไม่จำเป็นที่ก๊าซ ClO2 จะต้องแทรกซึมเข้าไปในไวรัสเพื่อทำให้ไวรัสไม่ทำงาน เพียงแค่ ClO2 ทำปฏิกิริยากับกรดอะมิโนซิสทีน ไทโรซีน และทริปโตเฟนหนึ่งตัวหรือบางส่วนของสไปค์ ซึ่งอยู่บนพื้นผิวของไวรัส ก็เพียงพอแล้ว ซึ่งหมายความว่าแนวทางเชิงทฤษฎีของเอกสารอ้างอิง ประเมินเวลาในการทำให้ไวรัสไม่ทำงานสูงเกินไป ในด้านหนึ่ง เนื่องจากการแพร่กระจายเกิดขึ้นเร็วมากในช่วงความยาว 0.1 มม. ดังนั้นจึงอาจไม่ได้เป็นปัจจัยจำกัดอัตราของปฏิกิริยา ในอีกด้านหนึ่ง ClO2 สามารถเข้าถึงกรดอะมิโนที่ทำปฏิกิริยาได้เป็นจำนวนมาก ส่วนที่เหลือของหนามแหลมโดยไม่ต้องซึมผ่านเปลือกโปรตีนของไวรัส
3. ไวรัสไม่มีไทออลโมเลกุลขนาดเล็กที่ป้องกัน เช่น กลูตาไธโอน หรือผลิตภัณฑ์เมตาบอลิซึมป้องกันโมเลกุลขนาดเล็กอื่นๆ เนื่องจากไวรัสไม่มีกระบวนการเมตาบอลิซึม ในแง่นี้ ไวรัสจึงควรมีความเปราะบางต่อการโจมตีของ ClO2 มากกว่าแบคทีเรีย
ข้อเท็จจริงเหล่านี้ทั้งหมดชี้ให้เห็นว่า เมื่อ ClO2 สัมผัสกับพื้นผิวของไวรัส การทำลายไวรัสจะเกิดขึ้นอย่างรวดเร็ว อย่างไรก็ตาม ไวรัสที่พร้อมจะติดเชื้อเซลล์มักจะอยู่ในเฟสของเหลว เช่น ในหยดของเหลว หรือในของเหลวที่บุผิวของเยื่อเมือก ขนาดของเฟสของเหลวเหล่านี้มีขนาดใหญ่กว่าไวรัสมาก ดังนั้นในกรณีเช่นนี้ ขั้นตอนที่จำกัดอัตราน่าจะเป็นการแพร่ของ ClO2 ในน้ำและการทำปฏิกิริยากับสารอื่นๆ เวลาที่ใช้ในการทำลาย ไวรัสเองจะสั้นกว่าเวลาที่ใช้ในการขนส่งโมเลกุล ClO2 ไปยังไวรัสให้เพียงพอ
ข้อเสนอแนะในการป้องกันการแพร่กระจายของการติดเชื้อไวรัสโดยใช้ ClO2
จากข้อโต้แย้งก่อนหน้านี้ ต่อไปนี้จะนำเสนอข้อเสนอแนะบางประการเกี่ยวกับวิธีการนำสารละลาย ClO2 ในน้ำมาใช้เพื่อวัตถุประสงค์ในการฆ่าเชื้อโรคทั้งในระดับโลกและระดับท้องถิ่น (ส่วนบุคคล) ข้อเสนอแนะเหล่านี้ส่วนใหญ่ตั้งอยู่บนสมมติฐาน ดังนั้นจึงสามารถนำไปใช้ได้ก็ต่อเมื่อมีการวิจัยอย่างรอบคอบแล้วเท่านั้น เป้าหมายของงานวิจัยนี้คือการเริ่มต้นการวิจัยเพื่อตรวจสอบสมมติฐานและข้อเสนอแนะเหล่านี้ในเชิงทดลอง ซึ่งอาจนำไปสู่การประยุกต์ใช้สารละลาย ClO2 ที่มีความบริสุทธิ์สูงเพื่อต่อต้านการติดเชื้อไวรัสหรือการติดเชื้ออื่นๆ แนวคิดเหล่านี้อาจได้รับการพัฒนาเพิ่มเติมในอนาคต แต่เนื่องจากภัยคุกคามจากการระบาดใหญ่ทั่วโลก เราจึงเลือกที่จะดำเนินการอย่างรวดเร็ว
การป้องกันทั่วโลก
การฆ่าเชื้อในอากาศ พื้นผิวแข็ง และบุคคลพร้อมกันด้วยสารละลาย ClO2 ในน้ำ สิ่งที่เราเสนอในที่นี้โดยพื้นฐานแล้วเป็นแนวคิดเดียวกันกับที่ Ogata และคณะ ได้เสนอไว้แล้ว นั่นคือ เป็นไปได้ที่จะสร้างบรรยากาศ ClO2 ที่ปลอดภัยสำหรับมนุษย์ แต่ในขณะเดียวกันก็เป็นอันตรายต่อจุลินทรีย์ อย่างไรก็ตาม มีความแตกต่างระหว่างข้อเสนอของพวกเขาและของเรา กลุ่มของ Ogata ถือว่าความเข้มข้นของ ClO2 (C) ในบรรยากาศเป็นพารามิเตอร์สำคัญเพียงอย่างเดียวของการบำบัด พวกเขาเสนอให้ใช้ความเข้มข้นของ ClO2 ต่ำกว่าขีดจำกัด OSHA 0.1 ppm (V/V) เป็นระยะเวลาที่จำเป็นในการทำให้จุลินทรีย์ไม่ทำงาน
อย่างไรก็ตาม ด้วยวิธีดังกล่าว เวลาสัมผัสที่จำเป็น (T) อาจยาวนานมาก ในที่นี้เราเสนอให้พิจารณาผลิตภัณฑ์ CT เป็นพารามิเตอร์ของการฆ่าเชื้อ ด้วยวิธีนี้จึงสามารถใช้ความเข้มข้นของ ClO2 ที่สูงกว่าขีดจำกัดของ OSHA ได้ แต่ใช้ได้เพียงช่วงเวลาจำกัดเท่านั้น ข้อดีของวิธีนี้คือ เมื่อใช้ค่า C ที่สูงขึ้น เวลาสัมผัสที่จำเป็นก็จะสั้นลงมาก แนวคิดนี้จะได้รับการอธิบายด้วยตัวอย่างเชิงตัวเลขด้านล่าง
ความแตกต่างที่สำคัญอีกประการหนึ่งคือ วิธีการของ Ogata เน้นไปที่บทบาทของก๊าซ ClO2 เป็นหลัก ในขณะที่เราเน้นความสำคัญของการใช้ก๊าซ ClO2 และ H2O พร้อมกัน ดังที่ได้รับการยืนยันจากการสังเกตของ Morino et al. ด้วยเหตุนี้ เราจึงเสนอวิธีการใหม่ในการสร้างบรรยากาศ ClO2: การใช้สารละลาย ClO2 ในน้ำ ซึ่งสามารถสร้างสมดุลความเข้มข้นของ ClO2 และ H2O ในบรรยากาศได้ เมื่อฉีดพ่นเข้าไปในอากาศ สารละลายในน้ำยังจัดการได้ง่ายกว่าการรักษาระดับ ClO2 ที่คงที่และต่ำมากในกระแสแก๊สอย่างต่อเนื่อง
ขอแนะนำให้ใช้สารละลาย ClO2 ที่มีความบริสุทธิ์สูงในการฉีดพ่น เพื่อหลีกเลี่ยงผลข้างเคียงที่ไม่พึงประสงค์ต่อบุคคลหรือพื้นผิวที่ได้รับการบำบัด สารละลาย ClO2 ที่มีความบริสุทธิ์สูงจะระเหยไปโดยไม่ทิ้งสารตกค้างหรือร่องรอยใดๆ
ตัวอย่างเชิงตัวเลขประกอบการอธิบาย สมมติว่าเราต้องการฆ่าเชื้อในพื้นที่ปิดโดยพ่นสารละลาย ClO2 เข้มข้นในน้ำเข้าไป ความเข้มข้นของ ClO2 ที่สมดุล cair ในเฟสแก๊สและ cw,e ในเฟสของเหลวสามารถคำนวณได้จากการกระจายสมดุลไอ-ของเหลวที่วัดโดย Ishi:
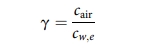
และจากสมดุลของส่วนประกอบสำหรับ ClO2:
![]()
โดยที่ Vair คือปริมาตรที่จะทำการฆ่าเชื้อ, Vw คือปริมาตรของสารละลาย ClO2 เข้มข้น และ cw0 คือความเข้มข้นของ ClO2 ในสารละลายนั้น
ด้วยความช่วยเหลือของสมการทั้ง 2 ข้างต้น เราสามารถคำนวณค่า cw;e ได้ดังนี้
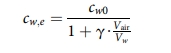
สมมติว่าเราใช้สารละลาย ClO2 เข้มข้น 40 ppm (m/m) ปริมาตร Vw 5 20 mL ในพื้นที่ปิดปริมาตร Vair 5 1 m3
ที่อุณหภูมิ 20°C ค่าสัมประสิทธิ์การกระจายตัวคือ g = 0.0316 (ข้อมูลของ Ishi) เมื่อความเข้มข้นทั้งหมดอยู่ในหน่วยเดียวกัน (เช่น ใน mg/L) และคือ gppm = 11.3 (ดูส่วนที่ ClO2 เป็นก๊าซที่ละลายน้ำได้) เมื่อใช้ ppm (m/m) และ ppm (V/V) ในเฟสของเหลวและเฟสก๊าซ ตามลำดับ เมื่อแทนค่าข้อมูลของเรา ผลลัพธ์ที่ได้คือ
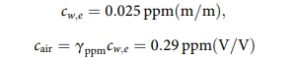
ผลลัพธ์นี้ต่ำกว่าค่า OSHA STEL (Short Term Exposition Limit) เล็กน้อย ซึ่งคือ 0.30 ppm (V/V) สำหรับ 15 นาที ตามที่ OSHA กำหนด STEL คือค่าเฉลี่ยการสัมผัสที่ยอมรับได้ในช่วงเวลาสั้นๆ – โดยปกติคือ 15 นาที – ตราบใดที่ค่าเฉลี่ยถ่วงน้ำหนักตามเวลา (TWA) ไม่เกิน หากบุคคลสัมผัสกับ 0.30 ppm เป็นเวลา 15 นาที และหลังจากนั้นเขาหรือเธออยู่ในบรรยากาศที่ปราศจาก ClO2 เป็นเวลา 30 นาที ค่า TWA สำหรับช่วงเวลา 45 นาทีทั้งหมดนี้จะอยู่ที่ 0.10 ppm ซึ่งถือว่ายอมรับได้ ทั้งหมดนี้หมายความว่าการสัมผัสของบุคคลกับบรรยากาศ ClO2 0.30 ppm เป็นเวลา 15 นาทีในครั้งเดียว หรือแม้แต่การใช้การรักษาดังกล่าวเป็นระยะๆ โดยมีช่วงพัก 30 นาทีภายในช่วงเวลา 8 ชั่วโมง ก็ไม่น่าจะก่อให้เกิดปัญหาสุขภาพใดๆ
คำถามและข้อคิดเห็น
1. เป็นคำถามสำคัญว่า การอยู่ในบรรยากาศ ClO2 0.29 ppm (V/V) เป็นเวลา 15 นาทีนั้นเพียงพอที่จะทำให้ไวรัสที่มีอยู่ไม่ทำงานหรือไม่? เกี่ยวกับบรรยากาศที่ชื้น เราสามารถสันนิษฐานได้ว่าไวรัสก็ชื้นด้วย หรือแม้กระทั่งอาจพบไวรัสในหยดน้ำขนาดเล็กที่มี ClO2 0.025 ppm (m/m) เราไม่มีข้อมูลโดยตรงเกี่ยวกับเวลาในการทำให้ไวรัสไม่ทำงานในสารละลายดังกล่าว แต่เรามีค่าประมาณเวลาในการฆ่าเชื้อแบคทีเรีย E. coli ในสารละลาย ClO2 0.25 ppm (m/m) อยู่ที่ 15 ± 5 วินาที เป็นเรื่องสมเหตุสมผลที่จะสันนิษฐานว่าเวลาในการฆ่าเชื้อจะนานขึ้น 10 เท่าในสารละลายที่เจือจางกว่า 10 เท่า นั่นคือ 150 วินาที 5 2.5 นาที เนื่องจากไวรัสมีแนวโน้มที่จะถูกทำลายเร็วกว่าแบคทีเรีย และ 15 นาทีนั้นนานกว่าเวลาที่คาดการณ์ไว้สำหรับ E. coli ถึงหกเท่า (2.5 นาที) ดังนั้นวิธีการดังกล่าวจึงน่าจะประสบความสำเร็จ อย่างน้อยก็ในทางทฤษฎี
2. เพื่อทดสอบวิธีการดังกล่าว เราขอแนะนำให้สร้างห้องฆ่าเชื้อพิเศษที่มีปริมาตรมากขึ้น การเริ่มต้นการทดลองดังกล่าวเป็นสิ่งที่พึงปรารถนาอย่างยิ่ง เพราะวิธีการนี้อาจเป็นการป้องกันแบบไม่จำเพาะเจาะจงที่มีประสิทธิภาพต่อไวรัสทุกชนิด และอาจช่วยควบคุมการระบาดของไวรัสได้
การป้องกันในระดับท้องถิ่น เทคนิคการฆ่าเชื้อส่วนบุคคลเพื่อป้องกันการติดเชื้อไวรัส
การฆ่าเชื้อในช่องปากและทางเดินหายใจส่วนบนด้วยการกลั้วคอ ไวรัสโคโรนาสายพันธุ์ใหม่ที่ระบาดในปัจจุบันเป็นที่ทราบกันดีว่ามีอยู่ในช่องปากและทั้งในทางเดินหายใจส่วนบนและส่วนล่าง แต่จะทำให้เกิดการติดเชื้อรุนแรงเฉพาะในทางเดินหายใจส่วนล่าง โดยเฉพาะในปอด ระยะฟักตัวของโรคคือหลายวัน แต่สามารถตรวจพบไวรัสได้ในตัวอย่างที่เก็บจากทางเดินหายใจส่วนบนไม่กี่วันก่อนที่อาการจะปรากฏ ดังที่ได้กล่าวไว้ในบทก่อนหน้า คลอรีนไดออกไซด์จะทำให้ไวรัสไม่ทำงานอย่างแน่นอน ด้วยการกลั้วคอ ทางเดินหายใจส่วนบนสามารถเข้าถึงได้ ยกเว้นโพรงจมูก แต่ก็สามารถเข้าถึงได้โดยใช้ยาหยอดจมูกหรือผ้าอนามัยแบบสอดที่ชุบสารฆ่าเชื้อ ส่วนต่างๆ เหล่านี้สามารถฆ่าเชื้อได้โดยการล้างเป็นประจำด้วยสารละลายคลอรีนไดออกไซด์ที่มีความบริสุทธิ์สูงที่มีจำหน่ายทั่วไป
ดังนั้นจำนวนไวรัสจึงสามารถลดลงได้อย่างมีนัยสำคัญในช่องปากและในทางเดินหายใจส่วนบน เราไม่สามารถแน่ใจได้ว่าการรักษาดังกล่าวจะเพียงพอที่จะป้องกันการเกิดโรคได้ เนื่องจากไวรัสที่อาศัยอยู่ในส่วนอื่นๆ ของร่างกายสามารถอยู่รอดได้ อย่างไรก็ตาม การทำให้ไวรัสบางส่วนไม่ทำงานด้วยการรักษาดังกล่าวจะช่วยให้ระบบภูมิคุ้มกันต่อสู้กับโรคได้อย่างแน่นอน ในส่วนนี้ เป็นที่น่าสนใจที่จะสังเกตว่านักวิจัยชาวญี่ปุ่นได้พิสูจน์แล้ว ว่าการกลั้วคอด้วยน้ำดื่มเป็นประจำช่วยลดอุบัติการณ์ของการติดเชื้อทางเดินหายใจส่วนบนได้อย่างมีนัยสำคัญทางสถิติ ผลกระทบดังกล่าวได้รับการอธิบายโดยข้อเท็จจริงที่ว่าน้ำดื่มที่ใช้ในการทดลองมีคลอรีน 0.5 มก./ลิตร ซึ่งใช้ในการฆ่าเชื้อน้ำ เราขอตั้งข้อสังเกตในที่นี้ว่าในบางสถานที่ใช้คลอรีนไดออกไซด์ในการฆ่าเชื้อน้ำดื่มแทนคลอรีน
การฆ่าเชื้อโรคในระบบทางเดินหายใจส่วนล่าง
ปัญหาแรกคือจะนำ ClO2 เข้าสู่ทางเดินหายใจส่วนล่างได้อย่างปลอดภัยได้อย่างไร เพื่อจุดประสงค์นี้ สามารถใช้เทคนิคการสูดดมใดๆ ก็ได้โดยใช้ละอองน้ำที่มี ClO2
ปัญหาที่สองและสำคัญกว่าคือ ปริมาณ ClO2 ที่สามารถสูดดมเข้าไปได้โดยไม่ทำให้ปอดเสียหายมีปริมาณเท่าใด การทราบปริมาณ ClO2 ที่ยังไม่เป็นอันตรายต่อปอดจะเป็นประโยชน์มาก เท่าที่เราทราบ ข้อมูลโดยตรงดังกล่าวไม่มีอยู่ในเอกสาร แต่สามารถคำนวณได้จากข้อมูลอื่นๆ จุดเริ่มต้นสำหรับการคำนวณดังกล่าวคือค่า OSHA STEL ซึ่งระบุว่า ClO2 0.30 ppm ในบรรยากาศสถานที่ทำงานสามารถทนได้เป็นเวลา 15 นาทีโดยไม่เกิดความเสียหายใดๆ ปริมาณอากาศที่คนงานสูดดมเข้าไปในช่วง 15 นาทีคือ 15 เท่าของสิ่งที่เรียกว่า “ปริมาณการระบายอากาศต่อนาที”
ตามตารางที่ 3 ของเอกสารอ้างอิง ในระหว่างกิจกรรมเบาๆ เช่น ขณะนั่งอยู่ในรถ ปริมาตรต่อนาทีจะอยู่ที่ประมาณ 12 ลิตร ดังนั้นปริมาณอากาศที่สูดดมเข้าไปทั้งหมดจะอยู่ที่ประมาณ 180 ลิตร ในกรณีที่มีความเข้มข้น 0.30 ppm ปริมาณ ClO2 ที่สูดดมเข้าไปทั้งหมดคือ 54 มิลลิลิตร ซึ่ง (ที่ 20 8C) เท่ากับ 2.25 มิลลิโมล ≈ 0.15 มิลลิกรัม ClO2 หากสมมติว่าทำกิจกรรมที่หนักขึ้น ปริมาณอาจเพิ่มขึ้นเป็นสองเท่า คือ 0.30 มิลลิกรัม
การคำนวณอย่างคร่าวๆ นี้แสดงให้เห็นว่าปริมาณ ClO2 โดยประมาณนี้เป็นปริมาณที่ปอดสามารถทนได้ ขีดจำกัดของ OSHA อาจใช้ปัจจัยด้านความปลอดภัยที่สูง ดังนั้นขีดจำกัดที่แท้จริงจึงควรสูงกว่านี้
เราขอแนะนำให้ทำการทดลองในสัตว์เพื่อหาค่าทดลองเกี่ยวกับความเป็นพิษต่อปอดของ ClO2 นอกจากนี้ การตรวจสอบเพิ่มเติมในการทดลองในสัตว์ว่า ClO2 ที่ใช้ในปริมาณที่ไม่เป็นพิษสามารถรักษาการติดเชื้อในปอดที่เกิดจากแบคทีเรียหรือไวรัสได้หรือไม่นั้น ก็มีความสำคัญเช่นกัน
บทสรุป
ในบทบรรณาธิการนี้ เราได้สรุปคุณสมบัติเฉพาะของคลอรีนไดออกไซด์ ซึ่งทำให้มันเป็นสารต้านจุลชีพที่เหมาะสมและไม่จำเพาะเจาะจงในความเข้มข้นที่ไม่เป็นอันตรายต่อมนุษย์ และเราได้ทบทวนงานวิจัยก่อนหน้านี้เกี่ยวกับการป้องกันการติดเชื้อไวรัสด้วยก๊าซ ClO2 จากพื้นฐานนี้ เราได้เสนอวิธีการสมมติฐานใหม่บางวิธีโดยใช้คลอรีนไดออกไซด์ในการฆ่าเชื้อในห้อง ป้องกันการติดเชื้อในมนุษย์ และชะลอการแพร่กระจายของไวรัส วิธีเหล่านี้เป็นวิธีการที่ไม่จำเพาะเจาะจง ซึ่งสามารถใช้ต่อต้านไวรัสที่ค้นพบใหม่ใด ๆ ก็ได้เป็นแนวป้องกันเบื้องต้นจนกว่าจะมีการพัฒนามาตรการรับมือที่เฉพาะเจาะจงและมีประสิทธิภาพ
ความขัดแย้งทางผลประโยชน์: Zoltan Noszticzius, Maria Wittmann และ Krist of K aly-Kullai เป็นผู้ร่วมคิดค้นสิทธิบัตรยุโรปหมายเลข 2069232 “วิธีการซึมผ่านและอุปกรณ์สำหรับการเตรียมของเหลว
ที่มีคลอรีนไดออกไซด์ความบริสุทธิ์สูง” Zoltan Noszticzius เป็นผู้ก่อตั้งและเจ้าของบริษัท Solumium Ltd (บริษัทผู้ผลิตคลอรีนไดออกไซด์) ในขณะที่ Krist of K aly-Kullai เป็นพนักงานที่ได้รับค่าจ้างของบริษัทดังกล่าว
เอกสารอ้างอิง
1. Bastacky J, Lee CY, Goerke J, Koushafar H, Yager D, Kenaga L และคณะ ชั้นเยื่อบุถุงลมบางและต่อเนื่อง: กล้องจุลทรรศน์อิเล็กตรอนแบบสแกนที่อุณหภูมิต่ำของปอดหนู J Appl Physiol 1995; 79(5): 1615–28, https://doi.org/10.1152/jappl.1995.79.5.1615.
2. Benarde MA, Snow WB, Oliveri VP, Davidson B. จลนศาสตร์และกลไกการฆ่าเชื้อแบคทีเรียโดยคลอรีนไดออกไซด์ Appl Microbiol 1967; 15(2): 257–65.
3. Cantin AM, North SL, Hubbard RC, Crystal RG. ของเหลวบุผิวถุงลมปกติมีระดับกลูตาไธโอนสูง J Appl Physiol 1987; 63(1): 152–7, https://doi.org/10.1152/jappl.1987.63.1.152.
4. Cao Z, Zhang Q, Lu X, Pfeiffer D, Jia Z, Song H, et al. การประมาณค่าจำนวนการแพร่พันธุ์ที่มีประสิทธิภาพของ 2019-nCoV ในประเทศจีน มีให้ดูออนไลน์ที่ http.medxriv.org; 29 ม.ค. 2020; https://doi.org/10.1101/2020.01.27.20018952.
5. Cross CE, van der Vliet A, O’Neill CA, Louie S, Halliwell B. สารออกซิแดนต์ สารต้านอนุมูลอิสระ และของเหลวที่บุทางเดินหายใจ Environ Health Perspect 1994; 102(ฉบับเพิ่มเติม 10): 185–91, https://doi.org/10.1289/ehp.94102s10185.
6. คู่มือแนวทางปฏิบัติของ EPA สำหรับการปฏิบัติตามข้อกำหนดการกรองและการฆ่าเชื้อสำหรับแหล่งน้ำสาธารณะ (AWWA; 1991) ตาราง C-9: ค่า CT สำหรับการยับยั้งไวรัสโดยคลอรีนไดออกไซด์ มีให้ที่ http://www.opssys.com/InstantKB/article.aspx?id514495.
7. Forman HJ, Zhang H, Rinna A. กลูตาไธโอน: ภาพรวมของบทบาทการป้องกัน การวัด และการสังเคราะห์ทางชีวภาพ Mol Aspects Med 2009; 30(1–2): 1–12, https://doi.org/10.1016/j.mam.2008.08.006.
8. Hauchman FS, Noss CI, Olivieri VP. ปฏิกิริยาของคลอรีนไดออกไซด์กับกรดนิวคลีอิก Water Res 1986; 20(3):357–61, https://doi.org/10.1016/0043-1354(86)90083-7.
9. https://www.britannica.com/science/coronavirus-virus-group.
10. Hui DS, Azhar EI, Madani TA, Ntoumi F, Kock R, Dar O, et al. ภัยคุกคามจากการระบาดของไวรัสโคโรนาสายพันธุ์ใหม่ 2019 อย่างต่อเนื่องต่อสุขภาพทั่วโลก – การระบาดของไวรัสโคโรนาสายพันธุ์ใหม่ 2019 ครั้งล่าสุดในเมืองอู่ฮั่น ประเทศจีน Int J Infect Dis 2020; 91: 264–6, https://doi.org/10.1016/j.ijid.2020.01.009.
11. Ishi G. ความสามารถในการละลายของคลอรีนไดออกไซด์ Chem Eng Japan 1958; 22(3): 153–4, https://doi.org/10.1252/kakoronbunshu1953.22.153.
12. Ison A, Odeh IN, Margerum DW. จลนศาสตร์และกลไกของการออกซิเดชันของคลอรีนไดออกไซด์และคลอไรต์ของซิสเตอีนและกลูตาไธโอน Inorg Chem 2006; 45: 8768–75, https://doi.org/10.1021/ic0609554.
13. Knudsen L, Ochs M. กลไกจุลภาคของถุงลมปอด: โครงสร้างและหน้าที่ของสารลดแรงตึงผิวและส่วนประกอบของเนื้อเยื่อวารสาร Histochem Cell Biol 2018; 150: 661–76, https://doi.org/10.1007/s00418-018-1747-9.
14. Koren E. ข้อเสนอแนะ ข้อมูลส่วนบุคคล; 2020.
15. Lubbers JR, Chauan SR, Bianchine JR. การประเมินทางคลินิกแบบควบคุมของคลอรีนไดออกไซด์ คลอไรต์ และคลอเรตในมนุษย์ วารสาร Environ Health Perspect 1982; 46: 57–62, https://doi.org/10.1289/ehp.824657.
16. Morino H, Fukuda T, Miura T, Lee C, Shibata T, Sanekata T. การทำให้ไวรัส feline calicivirus ซึ่งเป็นตัวแทนของ Norovirus ไม่ทำงานโดยก๊าซคลอรีนไดออกไซด์ Biocontrol Sci 2009; 14: 147–53, https://doi.org/10.4265/bio.14.147.
17. Napolitano MJ, Green BJ, Nicoson JS, Margerum DW. การออกซิเดชันของไทโรซีน, N-acetyltyrosine และ Dopa โดยคลอรีนไดออกไซด์ Chem Res Toxicol 2005; 18: 501–8, https://doi.org/10.1021/tx049697i.
18. Napolitano MJ, Stewart DJ, Margerum DW. การออกซิเดชันของกัวโนซีน 50-โมโนฟอสเฟตด้วยคลอรีนไดออกไซด์ Chem Res Toxicol 2006; 19: 1451–8, https://doi.org/10.1021/tx060124a.
19. Noss CI, Hauchman FS, Olivieri VP. ปฏิกิริยาของคลอรีนไดออกไซด์กับโปรตีน Water Res. 1986; 20(3): 351–6, https://doi.org/10.1016/0043-1354(86)90083-7.
20. Noszticzius Z, Wittmann M, K aly-Kullai K, Beregv ari Z, Kiss I, Rosivall L, et al. คลอรีนไดออกไซด์เป็นสารต้านจุลชีพที่เลือกขนาด PloS One 2013; 8(11): e79157, https://doi.org/10.1371/journal.pone.0079157
21. Ogata N. ก๊าซคลอรีนไดออกไซด์สำหรับใช้ในการรักษาการติดเชื้อไวรัสทางเดินหายใจ ข้อกำหนดสิทธิบัตรยุโรป EP 1955719 B1. ลำดับความสำคัญของ JP 2005342503; 2005
22. Ogata N. การทำให้โปรตีนเสียสภาพโดยคลอรีนไดออกไซด์: การดัดแปลงออกซิเดชันของทริปโตเฟนและไทโรซีนสารตกค้าง ชีวเคมี 2007; 46: 4898–911, https://doi.org/10.1021/bi061827u
23. Ogata N. การทำให้ฮีแมกกลูตินินของไวรัสไข้หวัดใหญ่ไม่ทำงานโดยคลอรีนไดออกไซด์: การออกซิเดชันของสารตกค้างทริปโตเฟน 153 ที่อนุรักษ์ไว้ในตำแหน่งการจับตัวรับ J Gen Virol 2012; 93: 2558–63, https://doi.org/10.1099/vir.0.044263-0.
24. Ogata N, Shibata T. ผลของก๊าซคลอรีนไดออกไซด์ที่มีความเข้มข้นต่ำมากต่อการขาดเรียนของเด็กนักเรียน Int J Med Med Sci 2009; 1(7): 288–9.
25. Ogata N, Shibata T. ผลการป้องกันของก๊าซคลอรีนไดออกไซด์ความเข้มข้นต่ำต่อการติดเชื้อไวรัสไข้หวัดใหญ่ A J Gen Virol 2008; 89: 60–7, https://doi.org/10.1099/vir.0.83393-0.
26. Satomura K, Kitamura T, Kawamura T, Shimbo T, Watanabe M, Kamei M, et al. นักวิจัยโรคหวัดใหญ่: การป้องกันการติดเชื้อทางเดินหายใจส่วนบนโดยการกลั้วคอ การทดลองแบบสุ่ม Am J PrevMed 2005; 29:302–7, https://doi.org/10.1016/j.amepre.2005.06.013.
27. Stewart DJ, Napolitano MJ, Bakhmutova-Albert EV, Margerum DW. จลนศาสตร์และกลไกของการออกซิเดชันของทริปโตเฟนด้วยคลอรีนไดออกไซด์ Inorg Chem 2008; 47: 1639–47, https://doi.org/10.1021/ic701761p.
28. Tan H, Wheeler BW, Wei C. ปฏิกิริยาของคลอรีนไดออกไซด์กับกรดอะมิโนและเปปไทด์: จลนศาสตร์และการศึกษาการกลายพันธุ์ Mutat Res 1987; 188(4): 259–66, https://doi.org/10.1016/0165-1218(87)90002-4.
29. Tao Y, Queen K, Paden CR, Zhang J, Li Y, Uehara A และคณะ ไวรัสโคโรนาสายพันธุ์ 2 ที่ก่อให้เกิดโรคทางเดินหายใจเฉียบพลันรุนแรงแยกได้ 2019-nCoV/USA-IL1/2020 จีโนมสมบูรณ์ NCBI GenBank; 2020. เข้าถึงได้ที่ https://www.ncbi.nlm.nih.gov/nucleotide/MN988713.1?report5genbank&log$5nuclalign&blast_rank51&RID5304U21XH016.
30. สำนักงานบริหารความปลอดภัยและสุขภาพในการทำงานแห่งสหรัฐอเมริกา การกำหนดปริมาณคลอรีนไดออกไซด์ในบรรยากาศสถานที่ทำงาน; 1991. เข้าถึงได้ที่ https://www.osha.gov/dts/sltc/methods/inorganic/id202/id202.html
31. www.solumium.com
32. Zuurbier M, Hoek G, van den Hazel P, Brunekreef B. การระบายอากาศต่อนาทีของนักปั่นจักรยาน ผู้โดยสารรถยนต์และรถโดยสาร: การศึกษาเชิงทดลอง Environ Health 2009; 8: 48, https://doi.org/10.1186/1476-069X-8-48