หน้าหลักนี้ประกอบด้วยเอกสารฉบับแปลของบทความวิชาการต้นฉบับ อย่างไรก็ตาม เรา ได้จัดทำสรุปเนื้อหาที่สำคัญแบบย่อยง่ายไว้ให้ผู้อ่านได้ศึกษาเป็นลำดับแรก เพื่อให้เข้าใจภาพรวมของงานวิจัยชิ้นนี้ได้อย่างรวดเร็ว หากท่านมีความสนใจในรายละเอียดเชิงลึกหรือข้อมูลทางสถิติเพิ่มเติม ท่านสามารถเลือกอ่านเอกสารฉบับเต็มได้ทั้งในรูปแบบภาษาอังกฤษ (Original) ได้ที่ลิงก์นี้: https://www.microbiologyresearch.org/content/journal/jgv/10.1099/vir.0.044263-0 หรือหากต้องการอ่านฉบับภาษาไทย (Translated) เราได้จัดทำบทแปลไว้ให้แล้วในหน้านี้ (ล่างสุด)
บทความเรื่อง Inactivation of influenza virus haemagglutinin by chlorine dioxide: oxidation of the conserved tryptophan 153 residue in the receptor-binding site เป็นการศึกษากลไกระดับโมเลกุลของการที่ chlorine dioxide ทำลายไวรัสไข้หวัดใหญ่ โดยมุ่งเน้นที่โปรตีน haemagglutinin (HA) ซึ่งเป็นส่วนสำคัญที่ไวรัสใช้ยึดเกาะและเข้าสู่เซลล์เจ้าบ้าน ผลการวิจัยพบว่า chlorine dioxide สามารถออกซิไดซ์กรดอะมิโน tryptophan ตำแหน่งที่ 153 ในบริเวณ receptor-binding site ของ HA ทำให้โครงสร้างและหน้าที่ของโปรตีนเสียไป ส่งผลให้ไวรัสไม่สามารถติดเชื้อได้ กลไกนี้แสดงให้เห็นว่า chlorine dioxide มีฤทธิ์ต้านไวรัสผ่านการทำลายโปรตีนสำคัญของไวรัสโดยตรง และสนับสนุนบทบาทของสารนี้ในฐานะสารฆ่าเชื้อที่มีประสิทธิภาพต่อไวรัส
ข้อมูลการเผยแพร่
- ชื่อบทความ: Inactivation of influenza virus haemagglutinin by chlorine dioxide: oxidation of the conserved tryptophan 153 residue in the receptor-binding site
- ผู้เขียน: Nobuyuki Ogata
- ปีที่ตีพิมพ์: 2012
- วารสารที่ตีพิมพ์: Journal of General Virology
บทคัดย่อ
การติดเชื้อไวรัสไข้หวัดใหญ่ในอากาศในหนูสามารถป้องกันได้ด้วยก๊าซคลอรีนไดออกไซด์ (ClO2) การศึกษานี้แสดงให้เห็นว่า ClO2 ยับยั้งการทำงานของฮีแมกกลูตินิน (HA) ของไวรัสไข้หวัดใหญ่สายพันธุ์ A (H1N1) ในลักษณะที่ขึ้นอยู่กับความเข้มข้น เวลา และอุณหภูมิ ค่า IC50 ในระหว่างปฏิกิริยา 2 นาทีกับ ClO2 ที่ 25°C คือ 13.7 mM และครึ่งชีวิตของ HA กับ ClO2 100 mM ที่ 25°C คือ 19.5 วินาที เปปไทด์ที่สร้างขึ้นจากการย่อยด้วยเอนไซม์ทริปซินของไวรัสที่ได้รับการบำบัดด้วย ClO2 ได้รับการวิเคราะห์โดยแมสสเปกโทรเมตรี พบชิ้นส่วน HA 150NLLWLTGK157 ซึ่งมีกรดอะมิโนทริปโตแฟน (W153) ที่มีมวลมากกว่าที่คาดไว้ 32 หน่วย หมู่ W153 ของเปปไทด์นี้ ซึ่งได้มาจากบริเวณตรงกลางของตำแหน่งจับกับตัวรับของ HA มีการอนุรักษ์ไว้อย่างสูง มีการแสดงให้เห็นว่า W153 ถูกออกซิไดซ์เป็น N-ฟอร์มิลคีนูเรนีนในไวรัสที่ได้รับการบำบัดด้วย ClO2
จึงสรุปได้ว่าการทำให้ไวรัสไข้หวัดใหญ่ไม่ทำงานโดย ClO2 เกิดจากการออกซิเดชันของ W153 ใน HA ซึ่งทำให้ความสามารถในการจับกับตัวรับของมันหายไป
บทนำ
ไวรัสไข้หวัดใหญ่เป็นไวรัส RNA สายเดี่ยวที่มีเปลือกหุ้มและมีทิศทางลบ มีโปรตีนที่ทะลุผ่านเยื่อหุ้มเซลล์ 3 ชนิด โดย 2 ชนิดเป็นที่รู้จักกันในชื่อโปรตีนหนาม ได้แก่ ฮีแมกกลูตินิน (HA) (Gamblin & Skehel, 2010; Skehel & Wiley, 2000) และนิวรามินิเดส (NA) (Xie et al., 2011) หน้าที่ของ HA นั้นจำเป็นอย่างยิ่งสำหรับการเริ่มต้นการติดเชื้อในเซลล์เป้าหมาย (Skehel & Wiley, 2000) ตัวรับ HA บนเซลล์เป้าหมายจะจับกับตำแหน่งจับตัวรับของ HA บริเวณดังกล่าวเป็นร่องตื้นๆ ที่ประกอบด้วยองค์ประกอบสามส่วน ได้แก่ เกลียว 190 (เกลียวอัลฟาของกรดอะมิโน 188–190) วง 130 (กรดอะมิโน 134–138) และวง 220 (กรดอะมิโน 221–228)
(Yang et al., 2007) กรดอะมิโนที่อนุรักษ์ไว้มีอยู่ในบริเวณที่จับกับตัวรับ ได้แก่ Y98, S136, W153, H183, E190 และ Y195 (Gamblin & Skehel, 2010; Stevens et al., 2004, 2006) ในบรรดาสารตกค้างที่ได้รับการอนุรักษ์เหล่านี้ W153 ตั้งอยู่ที่ด้านล่างของบริเวณการจับ ซึ่งอยู่ใต้หมู่แอซีทาไมด์ของกรดไซอะลิก (กรด N-อะซีทิลนิวรามินิก) ของตัวรับ (Lin et al., 2009)
คลอรีนไดออกไซด์ (ClO2) เป็นอนุมูลอิสระที่มีความเสถียรค่อนข้างสูง ClO2 สามารถยับยั้งแบคทีเรียหลายชนิด (Morino et al., 2011) เชื้อรา (Morino et al., 2007) และไวรัส (Morino et al., 2009; Sanekata et al., 2010) Ogata & Shibata (2008) ได้แสดงให้เห็นเมื่อเร็วๆ นี้ว่าก๊าซ ClO2 ความเข้มข้นต่ำ (0.03 ppm, v/v) ช่วยลดอัตราการตายของหนูที่สัมผัสกับละอองลอยของไวรัสไข้หวัดใหญ่สายพันธุ์ A (H1N1) ในขณะที่ Akamatsu et al (2012) ได้รายงานการทดลองสูดดมอย่างต่อเนื่องเป็นเวลา 6 เดือนในหนูทดลอง ซึ่งแสดงให้เห็นว่าระดับ ClO2 ที่ 0.05 ppm ไม่มีผลเสียใดๆ ประสิทธิภาพ (Ogata & Shibata, 2008) ของก๊าซ ClO2 ความเข้มข้นต่ำ บ่งชี้ว่าอาจมีประโยชน์ในการป้องกันการแพร่กระจายของไวรัสไข้หวัดใหญ่ (Ogata & Shibata, 2009) แม้ว่า Ogata & Shibata (2008) จะแสดงให้เห็นว่า ClO2 ทำให้ไวรัสไข้หวัดใหญ่ไม่ทำงาน แต่รายละเอียดระดับโมเลกุลของกลไกการทำให้ไม่ทำงานนี้ยังไม่ชัดเจน ผลลัพธ์ที่นำเสนอในเอกสารนี้แสดงให้เห็นอย่างชัดเจนว่าการทำให้ไวรัสไข้หวัดใหญ่ไม่ทำงานโดย ClO2 เกิดจากการออกซิเดชันและการกำจัดหน้าที่ของโมเลกุล HA
ผลลัพธ์
การยับยั้งการจับกลุ่มของเม็ดเลือดแดงโดย ClO2
ความสามารถของอนุภาคไวรัสไข้หวัดใหญ่ในการจับกลุ่มเม็ดเลือดแดงของไก่ลดลงเมื่ออนุภาคไวรัสได้รับการบำบัดด้วย ClO2 (ภาพที่ 1a) โดยมีค่า IC50 เท่ากับ 13.7 mM ที่ 25 uC เป็นเวลา 2 นาที และมีครึ่งชีวิตของ HA เท่ากับ 19.5 วินาที ที่ 25 uC ด้วย ClO2 100 mM (ภาพที่ 1b) กระบวนการยับยั้งนี้ขึ้นอยู่กับอุณหภูมิ (ภาพที่ 1c) ซึ่งบ่งชี้ว่าพื้นฐานของการยับยั้งเกี่ยวข้องกับปฏิกิริยาเคมี พลังงานกระตุ้นของกระบวนการยับยั้งนี้ถูกกำหนดโดยกราฟ Arrhenius (ภาพที่ 1d) จากเส้นที่เหมาะสม y521970x+9.31 (r2 50.93) พบว่าพลังงานกระตุ้นคือ 16.4 kJ·mol⁻¹·K⁻¹. เซลล์เม็ดเลือดแดงที่ได้รับการบำบัดล่วงหน้าด้วยแบคทีเรีย NA ไม่แสดงการจับกลุ่มกัน (ภาพที่ 1a) ซึ่งบ่งชี้ว่าการจับกลุ่มกันเกิดขึ้นผ่านทางสารตกค้างของกรดไซอะลิกในไกลโคโปรตีนของเซลล์เม็ดเลือดแดง
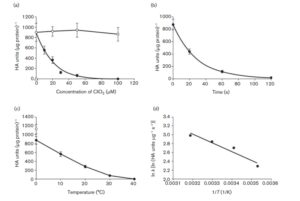
ภาพที่ 1 การยับยั้งการทำงานของ HA ของไวรัสไข้หวัดใหญ่โดยการสัมผัสกับ ClO2 (a) อนุภาคไวรัสไข้หวัดใหญ่ได้รับการบำบัดด้วย ClO2 ที่ความเข้มข้นต่างๆ ที่อุณหภูมิ 25°C เป็นเวลา 2 นาที จากนั้นจึงทำการทดสอบการจับกลุ่มของเม็ดเลือดแดงโดยใช้เม็ดเลือดแดงไก่ที่ไม่ได้รับการบำบัด ($) หรือเม็ดเลือดแดงไก่ที่ได้รับการบำบัดด้วย NA จากแบคทีเรีย (g) เพื่อเป็นตัวควบคุม ClO2 ที่ได้รับการบำบัดล่วงหน้าด้วย Na2S2O3 ในปริมาณที่มากเกินไปถูกเติมลงในการทดสอบ HA (#) (b) การเปลี่ยนแปลงตามเวลาของการยับยั้งการจับกลุ่มของเม็ดเลือดแดงโดยการสัมผัสกับ ClO2 100 mM ที่อุณหภูมิ 25°C (c) ความสัมพันธ์ระหว่างอุณหภูมิกับการยับยั้งการจับกลุ่มของเม็ดเลือดแดงโดยการสัมผัสกับ ClO2 100 mM เป็นเวลา 2 นาที (d) แผนภาพ Arrhenius แสดงความสัมพันธ์ระหว่างอุณหภูมิกับการยับยั้งการจับกลุ่มของเม็ดเลือดแดงเมื่อสัมผัสกับ ClO2 ความเข้มข้น 100 mM เป็นเวลา 2 นาที k คือค่าคงที่อัตรา T คืออุณหภูมิสัมบูรณ์ (K) ข้อมูลแสดงเป็นค่าเฉลี่ย ± ค่าเบี่ยงเบนมาตรฐาน จากการทดลองอิสระ 4 ครั้ง แถบแสดงข้อผิดพลาดถูกละเว้นใน (d)
การยับยั้งการจับตัวของตัวรับ HA โดย ClO2
การยับยั้งการทำงานของ HA ในการจับกับตัวรับจำเพาะโดย ClO2 ได้รับการตรวจสอบโดยการจับโดยตรงของสารประกอบอัลบูมินในซีรั่มของมนุษย์ที่ดัดแปลงด้วยไซอะลิล-α(2,6)-แลคโตส-เอ็น-อะเซทิลเลต พี-ฟีนิลีนไดอะมีน (ต่อไปนี้จะเรียกว่าสารประกอบไซอะลิล-อัลบูมิน) กับแผ่นไมโครไทเทรตที่เคลือบด้วย HA ไว้ล่วงหน้า ความสามารถของสารประกอบในการจับกับ HA บนแผ่นลดลงอย่างเห็นได้ชัดเมื่อ HA ถูกบำบัดด้วย ClO2 (รูปที่ S1 มีอยู่ใน JGV ออนไลน์) โดยสรุปแล้ว ผลลัพธ์เหล่านี้ชี้ให้เห็นว่า ClO2 ทำให้ความสามารถของ HA ในการจับกับตัวรับจำเพาะของมันหมดไป
การดัดแปลง HA โดย ClO2 ที่ตรวจพบโดยแมสสเปกโทรเมตรี (MS)
ต่อไปได้ทำการตรวจสอบลักษณะที่แท้จริงของการดัดแปลง HA ที่เกิดจาก ClO2 โดยทำการย่อยอนุภาคไวรัสที่ได้รับการบำบัดด้วย ClO2 ด้วยเอนไซม์ทริปซิน และแยกเปปไทด์ที่ได้ด้วย HPLC จากนั้นนำเศษส่วนไปวิเคราะห์ด้วยเทคนิค MALDI-TOF MS (matrix-assisted laser desorption/ionization time-of-flight MS) เศษส่วนที่มีเวลาการคงตัว 25.0225.5 นาที (รูปที่ S2 เศษส่วนที่ 45) แสดงค่าอัตราส่วนมวลต่อประจุ (m/z) เท่ากับ 976.55 (รูปที่ 2a) ชิ้นส่วนทริปซิน ที่มีค่า m/z 5976.55 สอดคล้องกับเปปไทด์ที่ประกอบด้วย 150NLLWLTGK157 ของ HA (การกำหนดหมายเลข H3) ซึ่งมีทริปโตแฟนเพียงตัวเดียวคือ W153 อย่างไรก็ตาม ค่า m/z 976.55 นั้นมากกว่าที่คาดการณ์ไว้จากลำดับกรดอะมิโนถึง 32 หน่วยมวล
นอกจากนี้ พีคนี้ยังไม่ปรากฏในอนุภาคไวรัสที่ไม่ได้รับการบำบัดด้วย ClO2 (ข้อมูลไม่ได้แสดงไว้) ลำดับกรดอะมิโนของเปปไทด์ที่ได้จากการวิเคราะห์ด้วย MS/MS คือ 150NLLWLTGK157 ยกเว้น W153 ที่มีมวลมากกว่าที่คาดไว้ 32 หน่วยมวล (ภาพที่ 2b) สารตกค้างนี้ถูกกำหนดเบื้องต้นให้เป็น N-formylkynurenine (FK) (รูปที่ 2a, ภาพแทรก) โดยอิงจากรายงานก่อนหน้านี้ (Ogata, 2007; Stewart et al., 2008) พีค MS อื่นๆ ของเศษส่วน HPLC แสดงอยู่ในตาราง S1
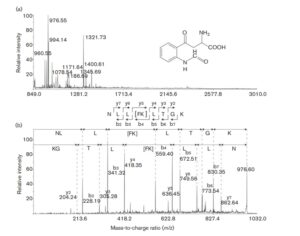
ภาพที่ 2 การวิเคราะห์ MALDI-TOF MS ของเศษส่วน HPLC (a) เปปไทด์ที่ปลดปล่อยออกมาจากอนุภาคไวรัสที่ได้รับการบำบัดด้วย ClO2 หลังจากการย่อยสลายด้วย trypsin ถูกนำไปวิเคราะห์ด้วย HPLC เศษส่วนที่ 45 (รูปที่ S2) ถูกนำไปวิเคราะห์ด้วย MALDI-TOF MS ภาพแทรกแสดงโครงสร้างของ N-formylkynurenine (b) พีคที่มี m/z 5976.55 ใน (a) ถูกนำไปวิเคราะห์ด้วย MS/MS ลำดับกรดอะมิโนที่ได้จากสเปกตรัม MS/MS แสดงอยู่ด้านบน (b) การกำหนดหมายเลขของไอออนชิ้นส่วน b และ y อ้างอิงจากระบบการตั้งชื่อของ Biemann (1988)
การดัดแปลงเปปไทด์สังเคราะห์ด้วย ClO2
เปปไทด์สังเคราะห์ที่มีลำดับ NLLWLTGK ที่ได้รับการบำบัดด้วย ClO2 แสดงพีคใหม่ที่มีเวลาการคงตัว 26.3 นาที ต่อไปนี้จะเรียกว่า ‘เปปไทด์ที่ถูกดัดแปลงด้วย ClO2’ (ข้อมูลไม่ได้แสดงไว้) เพื่อเป็นการควบคุม เปปไทด์อีกตัวหนึ่ง NLLGLTGK ซึ่งมีการแทนที่ G ด้วย W (ตัวหนา) ก็ได้รับการบำบัดด้วย ClO2 เช่นกัน เปปไทด์ที่แทนที่ด้วย G นี้ไม่แสดงการเปลี่ยนแปลงของมวลที่ตรวจพบได้หลังจากได้รับการบำบัดด้วย ClO2 (ข้อมูล
ไม่ได้แสดงไว้) ผลลัพธ์เหล่านี้ชี้ให้เห็นว่าการดัดแปลงที่เกิดจาก ClO2 นั้นเกิดจากการมีอยู่ของกรดอะมิโนทริปโตแฟนในเปปไทด์ NLLWLTGK เพื่อตรวจสอบความถูกต้องของการตีความนี้เพิ่มเติม สเปกตรัมการดูดกลืนแสงและการปล่อยแสงฟลูออเรสเซนต์ของเปปไทด์ที่ถูกดัดแปลงด้วย ClO2 ถูกนำมาเปรียบเทียบกับสเปกตรัมของเปปไทด์ NLLWLTGK ดั้งเดิม การเปลี่ยนแปลงสเปกตรัมการดูดกลืนแสงและการเรืองแสงของเปปไทด์ที่ดัดแปลงด้วย ClO2 บ่งชี้ว่าหมู่ทริปโตแฟนของเปปไทด์นั้นได้รับการดัดแปลงด้วยพันธะโควาเลนต์ (ข้อมูลไม่ได้แสดงไว้)
การวิเคราะห์ MS ของเปปไทด์ที่ดัดแปลงด้วย ClO2
พีค MALDI-TOF MS ของเปปไทด์ที่ถูกดัดแปลงด้วย ClO2 (m/z5976.79) (ภาพที่ S3a) เกือบจะเหมือนกับพีคที่ปลดปล่อยออกมาหลังจากการย่อยด้วยทริปซินจากอนุภาคไวรัสที่ได้รับการบำบัดด้วย ClO2
(ภาพที่ 2a) สเปกตรัมที่ได้จาก MS/MS โดยใช้พีค m/z5976.79 เป็นไอออนตั้งต้นยังให้พีคที่เกือบจะเหมือนกัน (ภาพที่ S3b) กับพีคที่สร้างขึ้นจากชิ้นส่วน HA ที่ปลดปล่อยออกมาจากอนุภาคไวรัสที่ได้รับการบำบัดด้วย ClO2 หลังจากการย่อยด้วยทริปซิน (ภาพที่ 2b) ยิ่งไปกว่านั้น องค์ประกอบของกรดอะมิโนของเปปไทด์ที่ถูกดัดแปลงด้วย ClO2 ไม่พบทริปโตแฟน แม้ว่าจะตรวจพบคีนูเรนีน (ข้อมูลไม่ได้แสดงไว้) (โปรดทราบว่าหมู่ฟอร์มิลของ FK จะถูกกำจัดออกไป ภายใต้สภาวะการไฮโดรไลซิสด้วยกรดที่ใช้สำหรับการวิเคราะห์กรดอะมิโน) ผลลัพธ์เหล่านี้บ่งชี้ว่าเปปไทด์สังเคราะห์ NLLWLTGK ก็ถูกออกซิไดซ์เป็น NLL[FK]LTGK โดย ClO2 เช่นกัน
การอภิปราย
ClO2 ทำปฏิกิริยาแบบไม่จำเพาะกับกรดอะมิโนทริปโตเฟนและไทโรซีนในโปรตีน (Napolitano et al., 2005; Ogata, 2007; Stewart et al., 2008) อย่างไรก็ตาม ควรสังเกตว่า ClO2 ไม่จำเป็นต้องทำปฏิกิริยากับกรดอะมิโนทริปโตเฟนและไทโรซีนทั้งหมดในโปรตีนที่กำหนด (Ogata, 2007) ความสามารถในการทำปฏิกิริยาที่แตกต่างกันของ ClO2 กับกรดอะมิโนในโปรตีนใดๆ อาจขึ้นอยู่กับว่ากรดอะมิโนเหล่านั้นเข้าถึงได้ง่ายสำหรับ ClO2 หรือไม่ การศึกษานี้แสดงให้เห็นว่า ClO2 ทำปฏิกิริยากับ W153 เป็นหลัก หากไม่ใช่แบบจำเพาะ ใน HA (รูปที่ 2) W153 ตั้งอยู่บนพื้นผิวของ HA (รูปที่ 3a) และคาดว่าเข้าถึงได้ง่ายสำหรับ ClO2
นอกจากนี้ ยังเป็นไปได้ว่ารูปทรงเรขาคณิตของ W153 ใน HA ช่วยอำนวยความสะดวกในการเกิดปฏิกิริยากับ ClO2 ความสามารถในการจับของ HA กับตัวรับจำเพาะบนเซลล์เป้าหมายมีความสำคัญอย่างยิ่งต่อ
การก่อให้เกิดการติดเชื้อ (Skehel & Wiley, 2000) เนื่องจาก W153 ใน HA มีการอนุรักษ์ไว้อย่างสูงในเกือบทุกสายพันธุ์ย่อยของไวรัสไข้หวัดใหญ่ (Knossow & Skehel, 2006; Martı´n et al., 1998)
จึงเชื่อกันว่ามันมีบทบาทสำคัญอย่างยิ่งต่อการทำงานของ HA (Meisner et al., 2008) ดังแสดงในรูปที่ 3(a, b) W153 ตั้งอยู่ที่ด้านล่างของบริเวณจับกับตัวรับอยู่ใต้กรดไซอะลิกของตัวรับ (Lin et al., 2009)
ในความเป็นจริง หมู่แอซีทาไมด์ (ภาพที่ 3b) ของกรดไซอะลิกนั้น อยู่ในสัมผัสแบบแวนเดอร์วาลส์กับวงแหวนอินโดลของ W153 (Lin et al., 2009; Martı´n et al., 1998) มีการคาดการณ์ว่า W153 ร่วมกับ Y195 ซึ่งสร้างพันธะไฮโดรเจนกับไนโตรเจนไพร์โรลของ W153 นั้น ให้โครงสร้างทางเรขาคณิตที่เหมาะสมที่สุด ซึ่งช่วยให้การจับกันอย่างมั่นคงของสารตกค้างกรดไซอะลิกของตัวรับกับ HA ปฏิสัมพันธ์ที่เสนอขึ้นนี้อธิบายว่าทำไมการออกซิเดชันของ W153 โดย ClO2 จึงมีแนวโน้มที่จะทำลายการทำงานของ HA (ภาพที่ 1)
ภาพที่ 3 ตำแหน่งการจับตัวรับของ HA และการเคลื่อนที่ที่เป็นไปได้ของกรดอะมิโน W153 ที่คงสภาพ หลังจากการออกซิเดชันเป็น FK โดย ClO2 (a) แสดงตำแหน่งการจับตัวรับของ HA ที่ตกผลึกร่วม กับตัวรับที่ถูกตัดทอน (Lin et al., 2009) แสดงเฉพาะกรดอะมิโนไซอะลิกที่ปลายสุดของตัวรับเท่านั้น (เส้นทึบ) กรดอะมิโนที่คงสภาพสูง ในตำแหน่งการจับตัวรับใน HA ก็แสดงไว้ด้วยพันธะไฮโดรเจนที่คาดว่ายึดกรดอะมิโนไซอะลิก
ของตัวรับกับ HA แสดงด้วยเส้นประ มุมมองนี้แสดงตำแหน่งการจับตัวรับของ HA เมื่อมองจากตัวรับ ลงไปยังปลายของ HA (b) มุมมองที่ขยายใหญ่ขึ้นของจุดศูนย์กลางของตำแหน่งการจับตัวรับของ HA (สเตอริโอแกรม) (c) การเคลื่อนที่ที่เป็นไปได้ของหมู่ W153 (เส้นประ, มองจากด้านหน้าของวงแหวนอินโดล) หลังจากถูกออกซิไดซ์เป็น FK (เส้นทึบ) โดย ClO2 ลูกศรแสดงการเคลื่อนที่ที่เป็นไปได้ของ W153 เมื่อถูกออกซิไดซ์เป็น FK พันธะคู่ของหมู่ฟอร์มิลไม่ได้อยู่ในสเกลที่ถูกต้อง เนื่องจากพันธะนี้อาจเอียงขึ้นด้านบน
ก่อนหน้านี้มีการแสดงให้เห็นโดยการทดลองติดฉลากไอโซโทปว่า ClO2 ออกซิไดซ์ทริปโตแฟนเป็น FK โดยการถ่ายโอนอะตอมออกซิเจนสองอะตอมจาก ClO2 (Ogata, 2007) ในปฏิกิริยานี้ วงแหวนไพร์โรลของทริปโตแฟนจะแยกออก และวงแหวนเบนซีนของ W153 จะเลื่อนไปดังแสดงในรูปที่ 3(c, ลูกศรล่าง) นอกจากนี้ เนื่องจากพันธะ N-ฟอร์มิลใน FK เป็นพันธะ s ที่หมุนได้อย่างอิสระ อะตอมออกซิเจนของหมู่ฟอร์มิลอาจหมุนขึ้นด้านบน (ในทิศทางของหมู่กรดไซอะลิก; ภาพที่ 3c, ลูกศรบน) เพื่อรองรับหมู่ CO ที่มีขนาดใหญ่
การเปลี่ยนแปลงโครงสร้างที่อาจเกิดขึ้นในบริเวณจับยึดของ HA มีแนวโน้มที่จะรบกวนการโต้ตอบกับหมู่กรดไซอะลิก นอกจากนี้ การเปลี่ยนแปลงโครงสร้างดังกล่าวในบริเวณจับยึดตัวรับของ HA จะไม่สามารถทำให้เกิดพันธะไฮโดรเจนที่จำเป็นซึ่งเกี่ยวข้องกับ Y95, Y195, E190 และ Q226 (รูปที่ 3a เส้นประ) เพื่อยึดหมู่กรดไซอะลิก ไว้ในตำแหน่งเดิมได้อีกต่อไป (Sauter et al., 1992) ดังนั้น การเปลี่ยนแปลงโครงสร้างในบริเวณจับยึดที่เกิดจาก W153 ที่ถูกออกซิไดซ์ จึงจะขัดขวางการทำงานของโมเลกุล HA
วิธีการ
ไวรัสและสารเคมี ไวรัสไข้หวัดใหญ่สายพันธุ์ A [A/New Caledonia/20/99 (H1N1)] ได้รับจาก ดร. Y. Okuno จากภาควิชาโรคติดเชื้อ สถาบันสาธารณสุขจังหวัดโอซาก้า ประเทศญี่ปุ่น แอนติบอดีซื้อจาก MyBiosource เปปไทด์ (ความบริสุทธิ์ 0.98%) ซื้อจาก Pi Proteomics โปรตีน HA รีคอมบิแนนท์ของ A/New Caledonia/20/99 (H1N1) ซื้อจาก Protein Sciences ClO2 เตรียมโดยใช้ NaClO2 และ HCl ตามที่อธิบายไว้ก่อนหน้านี้ (Ogata, 2007) สารประกอบไซอะลิล-อัลบูมินได้จาก IsoSep AB (Kallin et al., 1986) สารประกอบนี้มีโมเลกุลโอลิโกแซ็กคาไรด์ 15 โมลต่อโปรตีน 1 โมล ทริปซินได้จาก Promega สารเคมีอื่นๆ ทั้งหมดเป็นเกรดวิเคราะห์และได้มาจาก Nacalai Tesque อนุภาคไวรัสไข้หวัดใหญ่ถูกเตรียมในไข่ไก่ที่กำลังฟักตัวตามวิธีการที่อธิบายโดย Herrmann (1978) ได้โปรตีนไวรัสประมาณ 3.5 มิลลิกรัมใน 1 มิลลิลิตรจากไข่ 100 ฟอง โดยใช้วิธีนี้
การบำบัดอนุภาคไวรัสและ HA ด้วย ClO2 เว้นแต่จะระบุไว้เป็นอย่างอื่น ปฏิกิริยามาตรฐานสำหรับการบำบัดอนุภาคไวรัสหรือโปรตีน HA ด้วย ClO2 ดำเนินการในส่วนผสมปฏิกิริยา 1 มล. ซึ่งประกอบด้วยบัฟเฟอร์โซเดียมฟอสเฟต 10 mM (pH 7.0), NaCl 130 mM, ClO2 300 mM และอนุภาคไวรัส (100 มก. โปรตีน/มล.) หรือโปรตีน HA (100 มก./มล.) เริ่มปฏิกิริยาโดยการเติม ClO2 และดำเนินการต่อที่ 25 uC เป็นเวลา 2 นาที ยุติปฏิกิริยาโดยการเติม Na2S2O3 ในปริมาณโมลที่มากกว่าสองเท่า (Ogata, 2007) สำหรับการทดลองควบคุมโดยไม่ใช้ ClO2 บำบัด จะเติม ClO2 ที่ผสมไว้ล่วงหน้ากับ Na2S2O3 ในปริมาณโมลที่มากกว่าสองเท่าลงใน
ส่วนผสมปฏิกิริยา
สำหรับการทำปฏิกิริยากับอนุภาคไวรัส สารละลายปฏิกิริยาถูกนำไปให้ความร้อนที่ 100 องศาเซลเซียส เป็นเวลา 3 นาที จากนั้นจึงเติมสารละลายทริปซิน 38 มิลลิลิตร (1 มิลลิกรัมต่อมิลลิลิตร) สารละลายถูกบ่มที่ 37 องศาเซลเซียส เป็นเวลา 5 ชั่วโมง จากนั้นนำไปปั่นเหวี่ยงที่ 20,000 g ที่ 4 องศาเซลเซียส เป็นเวลา 1 ชั่วโมง ส่วนของเหลวใสถูกแยกออกมา และนำไปวิเคราะห์ด้วย HPLC ปริมาณ 100 มิลลิลิตร
การทดสอบการจับกลุ่มของเม็ดเลือดแดง ใช้แผ่นไมโครไทเทรตแบบก้นกลม 96 หลุม ทำจากโพลีสไตรีน (Biotec) ในการวัดความสามารถในการจับกลุ่มของเม็ดเลือดแดงของอนุภาคไวรัส อนุภาคไวรัสที่ได้รับการบำบัดหรือไม่ได้รับการบำบัดด้วย ClO2 ถูกแขวนลอยใน PBS จากนั้นอนุภาคไวรัสถูกเจือจางด้วยการเจือจางแบบอนุกรมสองเท่าและใส่ลงในแต่ละหลุมของแผ่น (50 มล. ต่อหลุม) เม็ดเลือดแดงไก่สดที่ได้รับการบำบัดหรือไม่ได้รับการบำบัดด้วย Clostridium perfringens NA (0.39 U ml21, 37 uC เป็นเวลา 10 นาทีใน PBS) ถูกแขวนลอยใน PBS ที่ความเข้มข้น 46107 เซลล์ ml21 และเติมลงในแต่ละหลุม (50 มล. ต่อหลุม) เก็บแผ่นไว้ที่ 4 uC เป็นเวลา 1 ชั่วโมง สังเกตการจับกลุ่มของเม็ดเลือดแดงด้วยตาเปล่า: จะเกิดแผ่นของเม็ดเลือดแดงที่ก้นหลุมหากเกิดการจับกลุ่ม มิฉะนั้น เม็ดเลือดแดงจะก่อตัวเป็น ‘จุด’ สีแดงที่ด้านล่าง ตรงกลางของหลุม หนึ่งหน่วยฮีแมกกลูตินินถูกกำหนดให้เป็นปริมาณไวรัสขั้นต่ำที่ทำให้เม็ดเลือดแดงจับตัวกันภายใต้เงื่อนไขการทดสอบที่อธิบายไว้ข้างต้น
การทดสอบการจับตัวรับของ HA โปรตีน HA รีคอมบิแนนท์ ที่ได้รับการบำบัดหรือไม่ได้รับการบำบัดด้วย ClO2 ตามที่อธิบายไว้ข้างต้น ถูกเจือจางด้วย PBS จนมีความเข้มข้น 20 มก./มล. จากนั้น นำสารละลายนี้ 100 ไมโครลิตร ใส่ลงในแต่ละหลุมของแผ่นไมโครไทเทรตแบบก้นแบน 96 หลุม (MaxiSorp; Nunc) ที่อุณหภูมิ 25 องศาเซลเซียส เป็นเวลา 30 นาที ล้างแต่ละหลุมของแผ่นสามครั้งด้วย PBS 100 มล.
ที่มี Tween 20 0.01% (v/v) และหนึ่งครั้งด้วยน้ำกลั่น 100 มล. จากนั้น นำสารละลายไมโอโกลบินจากกล้ามเนื้อโครงร่างม้า (Sigma-Aldrich) ใน PBS (1 มก./มล.) ใส่ลงในแต่ละหลุม (100 มล. ต่อหลุม) ที่อุณหภูมิ 25 องศาเซลเซียส เป็นเวลา 5 นาที เพื่อปิดกั้นบริเวณที่ไม่มีโปรตีนเคลือบในหลุม หลุมทดลองถูกล้างตามที่อธิบายไว้ข้างต้น ผึ่งลมให้แห้ง และเก็บไว้ที่อุณหภูมิห้อง ป้องกันแสง จนกว่าจะใช้งาน สำหรับการทดสอบการจับกับตัวรับ ใส่ไซอะลิล-อัลบูมิน 100 มล. (1.5 มก./มล.) ซึ่งเป็นแบบจำลองของตัวรับ HA ที่ถูกตัดทอน ลงในแต่ละหลุมที่อุณหภูมิ 25 องศาเซลเซียส เป็นเวลา 5 นาที จ
ากนั้นหลุมทดลองถูกล้างตามที่อธิบายไว้ข้างต้น และใส่แอนติบอดีต่อต้านอัลบูมินในซีรั่มของมนุษย์ที่ติดฉลาก HRP 100 มล. (เจือจางเป็น 0.8 มก./มล.) ลงในแต่ละหลุมที่อุณหภูมิ 25 องศาเซลเซียส เป็นเวลา 5 นาที จากนั้นหลุมทดลองถูกล้างตามที่อธิบายไว้ข้างต้น ก่อนที่จะเติมสารละลายซับสเตรตเพอร์ออกซิเดส (Bio-Rad) ปฏิกิริยาดำเนินต่อไปที่อุณหภูมิ 37 องศาเซลเซียส เป็นเวลา 10 นาที ก่อนที่จะหยุดปฏิกิริยาโดยการเติม HCl 20 มิลลิโมลาร์ (100 มล. ต่อหลุม)
แผ่นเพลทถูกสแกนโดยใช้เครื่องอ่านไมโครเพลท (รุ่น MPR-A4; Toyosoda) เพื่อวัดค่าการดูดกลืนแสงที่ 415 นาโนเมตร ความสามารถของแผ่นเพลท 96 หลุมในการจับกับ HA ถูกวัดในการทดลองแยกต่างหาก ในที่นี้ หลังจากขั้นตอนการจับ การล้าง และการทำให้แห้งตามที่อธิบายไว้ข้างต้น แอนติบอดีต่อไวรัสไข้หวัดใหญ่สายพันธุ์ A (H1N1) HA ที่ติดฉลาก HRP จำนวน 100 มล. (เจือจางเป็น 0.5 มก./มล.21) ถูกใส่ลงในแต่ละหลุม ปฏิกิริยาการพัฒนาสีถูกดำเนินการตามที่อธิบายไว้ข้างต้นเพื่อหาปริมาณของ HA ที่จับกับแต่ละหลุมของแผ่นเพลท
การแยกเปปไทด์ด้วย HPLC เปปไทด์ (5–20 นาโนโมล ใน 100 มิลลิลิตร) ถูกแยกด้วยคอลัมน์ Cosmosil 5C18-AR-300 (4.66250 มม.; Nacalai Tesque) ที่ติดตั้งบนระบบ HPLC หลังจากฉีดตัวอย่างเปปไทด์แล้ว
คอลัมน์จะถูกชะล้างด้วยกรดไตรฟลูออโรอะซิติก 0.1% (v/v) ที่มีอะซีโตไนไตรล์แบบไล่ระดับเชิงเส้นสองระดับต่อเนื่องกัน (0–12% v/v จาก 0 ถึง 1 นาที และจากนั้น 12–60% v/v จาก 1 ถึง 60 นาที) โดยใช้อัตราการไหล 1 มิลลิลิตรต่อนาที ได้โปรไฟล์การชะล้างของเปปไทด์โดยตรวจสอบการดูดกลืนแสงของสารที่ถูกชะล้างที่ 230 หรือ 280 นาโนเมตร เศษส่วนของสารที่ได้จากการชะล้างถูกทำให้แห้งด้วยวิธีแช่แข็งและละลายในน้ำกลั่นเพื่อการวิเคราะห์เพิ่มเติม
การวิเคราะห์มวลสารของเปปไทด์ ตัวอย่างเปปไทด์ (10–500 พิโคโมล) ถูกนำไปวิเคราะห์ด้วย MALDI-TOF MS เพื่อวัดมวลสารที่สมบูรณ์ ซึ่งก็คืออัตราส่วน m/z (Biemann, 1988) หรือ MS/MS หลังจากไอออนไนเซชันแบบอิเล็กตรอนสเปรย์ของไอออนตั้งต้น เพื่อวิเคราะห์ลำดับกรดอะมิโนของเปปไทด์ ตามที่ได้อธิบายไว้ก่อนหน้านี้ (Ogata, 2007)
การวิเคราะห์กรดอะมิโนของเปปไทด์ องค์ประกอบของกรดอะมิโนของเปปไทด์ (~200 พิโคโมล) ถูกวิเคราะห์โดยใช้เครื่องวิเคราะห์กรดอะมิโน (รุ่น L-8500; ฮิตาชิ) หลังจากการไฮโดรไลซิสด้วยกรด (ใน HCl 6 M ที่ 110 uC เป็นเวลา 22 ชั่วโมง) ภายใต้ความดันลดลงและในที่ที่มีไนโตรเจน มีการเติมกรดไทโอไกลโคลิก (4% v/v) ลงใน HCl เพื่อป้องกันการสลายตัวของทริปโตเฟนระหว่างการไฮโดรไลซิส
เอกสารอ้างอิง
Akamatsu, A., Lee, C., Morino, H., Miura, T., Ogata, N. & Shibata, T. (2012). การศึกษาความเป็นพิษจากการสูดดมก๊าซคลอรีนไดออกไซด์ระดับต่ำเป็นเวลาหกเดือน โดยมีระยะเวลาพักฟื้นสองสัปดาห์ในหนู J Occup Med Toxicol 7, 2.
Biemann, K. (1988). การมีส่วนร่วมของแมสสเปกโทรเมตรีต่อโครงสร้างของเปปไทด์ และโปรตีน Biomed Environ Mass Spectrom 16, 99–111.
Gamblin, S. J. & Skehel, J. J. (2010). โปรตีนเมมเบรนเฮมากลูตินินและนิวรามินิเดสของไวรัสไข้หวัดใหญ่ J Biol Chem 285, 28403–28409. Herrmann, B. (1978). [การผลิตการรวมตัวใหม่ของไวรัสไข้หวัดใหญ่]. Arch Exp Veterinarmed 32, 455–464 (ในภาษาเยอรมัน)
Kallin, E., Lo¨ nn, H. & Norberg, T. (1986). ขั้นตอนการดัดแปลงและการแยกแบบใหม่สำหรับการลดโอลิโกแซ็กคาไรด์ Glycoconj J 3, 311–319.
Knossow, M. & Skehel, J. J. (2006). ความแปรผันและการติดเชื้อการทำให้เป็นกลางในไข้หวัดใหญ่ Immunology 119, 1–7.
Lin, T., Wang, G., Li, A., Zhang, Q., Wu, C., Zhang, R., Cai, Q., Song, W. & Yuen, K.-Y. (2009). โครงสร้างเฮมากลูตินินของไวรัสไข้หวัดใหญ่ H1N1 ในนก Virology 392, 73–81.
Martı´n, J., Wharton, S. A., Lin, Y. P., Takemoto, D. K., Skehel, J. J., Wiley, D. C. & Steinhauer, D. A. (1998). การศึกษาคุณสมบัติการจับของตัวกลายพันธุ์ของตำแหน่งตัวรับฮีแมกกลูตินินของไวรัสไข้หวัดใหญ่ Virology 241, 101–111.
Meisner, J., Szretter, K. J., Bradley, K. C., Langley, W. A., Li, Z.-N., Lee, B.-J., Thoennes, S., Martin, J., Skehel, J. J. และผู้เขียนคนอื่นๆ (2008). การศึกษาการติดเชื้อของตัวกลายพันธุ์ของตำแหน่งการจับตัวรับฮีแมกกลูตินินของไวรัสไข้หวัดใหญ่ในหนู J Virol 82, 5079–5083.
Morino, H., Matsubara, A., Fukuda, T. & Shibata, T. (2007). [การยับยั้งการเจริญเติบโตของเส้นใยของเชื้อรา Alternaria alternata โดยก๊าซคลอรีนไดออกไซด์ที่ความเข้มข้นต่ำมาก]. Yakugaku Zasshi 127,
773–777 (เป็นภาษาญี่ปุ่น).
Morino, H., Fukuda, T., Miura, T., Lee, C., Shibata, T. & Sanekata, T. (2009). การทำให้ไวรัส feline calicivirus ซึ่งเป็นตัวแทนของ norovirus ไม่ทำงานโดยก๊าซคลอรีนไดออกไซด์. Biocontrol Sci 14, 147–153.
Morino, H., Fukuda, T., Miura, T. & Shibata, T. (2011). ผลของก๊าซคลอรีนไดออกไซด์ความเข้มข้นต่ำต่อแบคทีเรียและไวรัสบนพื้นผิวกระจกในสภาพแวดล้อมที่เปียกชื้น. Lett Appl Microbiol 53, 628–634.
Napolitano, M. J., Green, B. J., Nicoson, J. S. & Margerum, D. W. (2005). การออกซิเดชันของไทโรซีน, N-อะเซทิลไทโรซีน และโดปา ด้วยคลอรีนไดออกไซด์ Chem Res Toxicol 18, 501–508.
Ogata, N. (2007). การทำให้โปรตีนเสียสภาพด้วยคลอรีนไดออกไซด์: การดัดแปลงออกซิเดชันของสารตกค้างทริปโตเฟนและไทโรซีน Biochemistry 46, 4898–4911.
Ogata, N. & Shibata, T. (2008). ผลการป้องกันของก๊าซคลอรีนไดออกไซด์ความเข้มข้นต่ำต่อการติดเชื้อไวรัสไข้หวัดใหญ่สายพันธุ์ A J Gen Virol 89, 60–67.
Ogata, N. & Shibata, T. (2009). ผลของก๊าซคลอรีนไดออกไซด์ที่มีความเข้มข้นต่ำมากต่อการขาดเรียนของเด็กนักเรียน Int J Med Med Sci 1, 288–289. N. Ogata 2562
Sanekata, T. , Fukuda, T. , Miura, T. , Morino, H. , Lee, C. , Maeda, K. , Araki, K. , Otake, T. , Kawahata, T. & Shibata, T. (2010) การประเมินผลของกิจกรรมต้านไวรัสของคลอรีนไดออกไซด์และโซเดียมไฮโปคลอไรต์ต่อต้านไวรัสคาลิซิในแมว, ไวรัสไข้หวัดใหญ่ในมนุษย์, ไวรัสหัด, สุนัขไวรัสไข้หัด, เริมไวรัสของมนุษย์, อะดีโนไวรัสของมนุษย์, สุนัข adenovirus และ canine parvovirus ไบโอคอนโทรลวิทย์ 15, 45–49
Sauter, N.K., Glick, G.D., Crowther, R.L., Park, S.J., Eisen, M.B., Skehel, J. J. , Knowles, J. R. และ Wiley, D. C. (1992) การตรวจพบทางผลึกศาสตร์ของตำแหน่งการจับลิแกนด์ที่สองในฮีแมกกลูตินินของไวรัสไข้หวัดใหญ่ Proc Natl Acad Sci U S A 89, 324–328. Skehel, J. J. & Wiley, D. C. (2000). การจับตัวรับและการหลอมรวมของเยื่อหุ้มเซลล์ในการเข้าสู่ไวรัส: ฮีแมกกลูตินินของไวรัสไข้หวัดใหญ่ Annu Rev Biochem 69, 531–569.
Stevens, J., Corper, A. L., Basler, C. F., Taubenberger, J. K., Palese, P.& Wilson, I. A. (2004). โครงสร้างของฮีแมกกลูตินิน H1 ของมนุษย์ที่ยังไม่ถูกตัดจากไวรัสไข้หวัดใหญ่ปี 1918 ที่สูญพันธุ์ไปแล้ว Science 303, 1866–1870.
Stevens, J., Blixt, O., Tumpey, T. M., Taubenberger, J. K., Paulson, J. C.& Wilson, I. A. (2006). โครงสร้างและความจำเพาะของตัวรับของเฮมากลูตินินจากไวรัสไข้หวัดใหญ่ H5N1 Science 312, 404–410.
Stewart, D. J., Napolitano, M. J., Bakhmutova-Albert, E. V. & Margerum, D. W. (2008). จลนศาสตร์และกลไกของการออกซิเดชันของทริปโตเฟนด้วยคลอรีนไดออกไซด์ Inorg Chem 47, 1639–1647.
Xie, Y., Gong, J., Li, M., Fang, H. & Xu, W. (2011). ศักยภาพทางการแพทย์ของโปรตีนพื้นผิวไวรัสไข้หวัดใหญ่: เฮมากลูตินินและนิวรามินิเดส Curr Med Chem 18, 1050–1066.
Yang, Z.-Y., Wei, C.-J., Kong, W.-P., Wu, L., Xu, L., Smith, D. F. & Nabel, G. J. (2007). การสร้างภูมิคุ้มกันโดยฮีแมกกลูตินินกลายพันธุ์ของไวรัสไข้หวัดนก H5 ที่มีความจำเพาะในการจับกับตัวรับที่เปลี่ยนแปลงไป Science 317, 825–828.