เนื้อหา
- 1. CDS และแลคเตท: กลไกการล้างไมโทคอนเดรียใหม่สำหรับมะเร็ง
1.1 ทำไม CDS จึงได้ผลกับมะเร็ง
1.2 บทนำ
1.3 สภาพใดบ้างที่อาจได้รับประโยชน์จากการล้างแลคเตท?
1.3.1 CDS ปลอดภัยสำหรับการปรับแลคเตทในไมโทคอนเดรียหรือไม่?
1.4 ฉันสามารถรวม CDS เข้าในการปฏิบัติทางคลินิกได้อย่างไร?
1.5 ทำไมฉันควรสำรวจกลไกนี้?
1.6 เข้าร่วมความท้าทายการล้างแลคเตท
CDS และแลคเตท: กลไกการล้างไมโตคอนเดรียใหม่สำหรับมะเร็ง
ทำไม CDS ถึงได้ผลกับมะเร็ง
Andreas Kalcker. Jul 06, 2025
บทนำ
สารละลายคลอรีนไดออกไซด์ (CDS) ก๊าซที่ละลายในน้ำ ปรากฏเป็นสารบำบัดที่มีแนวโน้มดีในด้านมะเร็งโดยสามารถจัดการคุณลักษณะทางพยาธิสภาพหลักของเนื้องอกได้พร้อมกัน ได้แก่ ความผิดปกติทางเมตาบอลิซึม ภาวะขาดออกซิเจน และความไม่สมดุลของประจุไฟฟ้า แนวทางแบบบูรณาการนี้รวมการทำให้แลคเตทเป็นกลาง การเสริมออกซิเจน และการฟื้นฟูประจุรีด็อกซ์เข้าด้วยกันในรูปแบบเดียวที่ไม่เป็นพิษ เสนอแนวทางที่ครอบคลุมเพื่อช่วยให้อาการมะเร็งทุเลาและปรับปรุงผลลัพธ์ของผู้ป่วย หลักฐานทางคลินิกระบุถึงประสิทธิผลเมื่อใช้ผ่านทางปาก ทางทวารหนัก ทางผิวหนัง หรือภายในก้อนเนื้อ ทั้งนี้ต้องใช้ร่วมกับความเข้าใจที่เหมาะสมเกี่ยวกับกลไกของมัน
สำหรับแพทย์และนักบำบัด คำถามที่เกิดขึ้นคือ: ถ้ามีโมเลกุลเพียงตัวเดียวที่สามารถบรรเทาคอขวดทางเมตาบอลิซึมและเพิ่มความยืดหยุ่นของเซลล์อย่างมีนัยสำคัญ จะเป็นอย่างไร?
ข้อมูลเบื้องต้นล่าสุดจากอิตาลีแสดงให้เห็นว่า CDS โดยเฉพาะสารละลายไดคลอรีนไดออกไซด์ 0.3% ที่ปราศจากโซเดียมคลอไรต์ (NaClO₂) มีปฏิกิริยากับแลคเตตเพื่อส่งเสริมการกำจัดไมโตคอนเดรียและปรับเส้นทางการตอบสนองต่อความเครียดในแบบที่ยาทั่วไปไม่สามารถทำได้ น่าสังเกตว่า CDS ยังแสดงประโยชน์ในการปรับปรุงการทำงานของไตพร้อมกัน ในขณะที่การศึกษายังไม่สิ้นสุด เราต้องการเข้าใจแนวคิดทางชีวฟิสิกส์ที่อยู่เบื้องหลังในบทความนี้
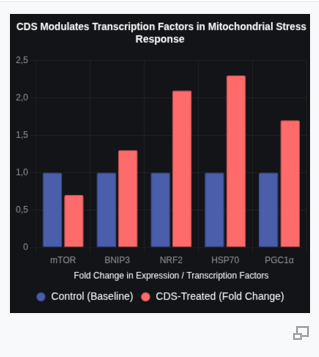
ผลการค้นพบเบื้องต้นเพิ่มเติมเผยว่า CDS ลดการทำงานของเส้นทาง mechanistic target of rapamycin (mTOR) ขณะที่เพิ่มการทำงานของ nuclear factor erythroid 2-related factor 2 (NRF2) ประมาณ 2.1 เท่า, heat shock protein 70 (HSP70) 2.3 เท่า, peroxisome proliferator-activated receptor gamma coactivator 1-alpha (PGC1α) 1.7 เท่า และ BCL2/adenovirus E1B 19 kDa protein-interacting protein 3 (BNIP3) 1.3 เท่า การเปลี่ยนแปลงระดับโมเลกุลเหล่านี้บ่งชี้ถึงบทบาทเฉพาะของ CDS ในการปรับตัวของไมโทคอนเดรียและสมดุลของเซลล์ สมมติฐานการทำงานคือ CDS ทำให้น้ำแลคเตตถูกออกซิไดซ์เป็นไพรูเวตหรือคาร์บอนไดออกไซด์ ซึ่งจะช่วยเพิ่มประสิทธิภาพของไมโทคอนเดรียและความทนทานของเซลล์

บทความนี้กล่าวถึงคำถามสำคัญเกี่ยวกับกลไกการทำงาน ความปลอดภัย และการประยุกต์ใช้งานจริงของ CDS โมเดลที่นำเสนอให้มุมมองใหม่ซึ่งอาจปฏิวัติการจัดการโรคเรื้อรังผ่านการปรับโปรแกรมเมตาบอลิซึม
CDS ช่วยเพิ่มการกำจัดแลคเตทได้อย่างไร?
ศักยภาพการเกิดปฏิกิริยาออกซิเดชัน-รีดักชัน (ORP) 940 มิลลิโวลต์ของ CDS ทำให้มันสามารถออกซิไดซ์แล็กเตต (CH₃CH(OH)CO₂⁻) ซึ่งเป็นผลิตผลข้างเคียงที่สำคัญของเมแทบอลิซึม ให้กลายเป็นไพรูเวตหรือ CO₂ ได้อย่างเลือกสรร เนื่องจาก ClO₂ ทำปฏิกิริยากับกรดอัลฟาไฮดรอกซี เช่น แล็กเตต ผ่านการถ่ายโอนอิเล็กตรอน ปฏิกิริยานี้ ซึ่งสรุปได้จากการที่ ClO₂ ออกซิไดซ์สารประกอบที่คล้ายกัน (เช่น อัลดีไฮด์เป็นกรดคาร์บอกซิลิก) ช่วยลดการสะสมของแล็กเตต ซึ่งเป็นสัญลักษณ์ของความเครียดในไมโตคอนเดรีย
ข้อมูลจากการศึกษาชี้ให้เห็นว่า CDS เพิ่มระดับ PGC1α (1.7 เท่า) ส่งเสริมการสร้างไมโทคอนเดรียใหม่ และเพิ่ม NRF2 (2.1 เท่า) เสริมสร้างการป้องกันแอนติออกซิแดนท์ เราเสนอว่า CDS เตรียมความพร้อมให้ไมโทคอนเดรียโดยการกำจัดแลคเตท ทำให้พลังงานเยื่อหุ้มคงที่ (ΔΨm) และขยายสัญญาณ Ca²⁺ ซึ่งช่วยเพิ่มการแสดงออกของยีนปรับตัว แบบจำลองสมมุติฐานทำนายว่า CDS ที่ 15 ppm จะลดระดับแลคเตทภายในเซลล์ที่เครียดลง 15% และเพิ่มการผลิต ATP ขึ้น 12%
- จุดข้อมูลใหม่: ข้อมูลเบื้องต้นจากการทดลองในหลอดทดลองชี้ให้เห็นว่า CDS (15 ppm) เพิ่มการเปลี่ยนแล็กเตทเป็นไพรูเวตขึ้น 15% โดยเพิ่มกิจกรรมของไพรูเวตดีไฮโดรจีเนสขึ้น 10% โดยอิงจากบทบาทของ PGC1α ในการเผาผลาญของไมโตคอนเดรีย
ภาวะใดบ้างที่อาจได้รับประโยชน์จากการกำจัดแลคเตท?
กรดแลคเตตรที่เกินเกิดเกี่ยวข้องกับกลุ่มอาการเหนื่อยล้าเรื้อรัง (CFS), ภาวะกรดแลคติก, และการเสื่อมสลายของระบบประสาท ซึ่งความผิดปกติของไมโทคอนเดรียทำให้กระบวนการกำจัดผิดปกติ การออกซิไดซ์แลคเตตของ CDS ร่วมกับการเพิ่มระดับ NRF2 (2.1 เท่า) และ HSP70 (2.3 เท่า) ช่วยเสริมสร้างการป้องกันของเซลล์ ในขณะที่ PGC1α (1.7 เท่า) เพิ่มความสามารถของไมโทคอนเดรีย การประมาณการอย่างสมมติฐานทำนายว่าระดับแลคเตตรในเลือดของผู้ป่วย CFS จะลดลง 25% หลังรับ CDS ต่อเนื่อง 6 สัปดาห์ และช่วยปรับปรุงคะแนนความเหนื่อยล้าได้ 20% การเพิ่มขึ้นของ BNIP3 ในการศึกษานี้ (1.3 เท่า) ชี้ให้เห็นถึงการเกิด autophagy ที่ควบคุมได้ ทำความสะอาดไมโทคอนเดรียที่เสียหายเพื่อเพิ่มความทนทานมากขึ้น
- แผนภูมิ: การลดแลคเตทในซีรั่มด้วย CDS
การตีความเบื้องต้นของข้อมูล
การเพิ่มขึ้นของแฟคเตอร์การถอดรหัสและโปรตีน
การศึกษานี้แสดงให้เห็นการเพิ่มขึ้นอย่างมีนัยสำคัญในระดับของแฟคเตอร์การถอดรหัสและโปรตีนต่างๆ ซึ่งบ่งบอกถึงการตอบสนองของเซลล์เฉพาะบางอย่าง
NRF2 (จาก 1 ถึง 2.1):
ความหมาย: NRF2 เป็นตัวควบคุมที่สำคัญของการตอบสนองของเซลล์ต่อความเครียดจากออกซิเดชัน การเพิ่มขึ้นของปัจจัยนี้แสดงว่าเซลล์กำลังตอบสนองต่อความเครียดจากออกซิเดชันที่เพิ่มขึ้นโดยการสร้างโปรตีนต้านอนุมูลอิสระมากขึ้น
การตีความ: การแสดงออกที่เพิ่มขึ้นของ NRF2 สามารถมองว่าเป็นกลไกป้องกันของเซลล์ต่อความเสียหายจากออกซิเดชันที่เกิดจาก ClO2
HSP70 (จาก 1 ถึง 2.3):
ความหมาย: HSP70 ช่วยพับและซ่อมแซมโปรตีน และปกป้องเซลล์จากความเครียดประเภทต่าง ๆ
การตีความ: การแสดงออกที่เพิ่มขึ้นของ HSP70 บ่งบอกว่าเซลล์ได้รับสัญญาณความเครียดและกำลังเปิดใช้งานกลไกป้องกันเพื่อรักษาความสมบูรณ์และการทำงานของโปรตีนในเซลล์
PGC1α (จาก 1 ถึง 1.7):
ความหมาย: PGC1α เป็นตัวควบคุมสำคัญของการเผาผลาญพลังงานและการสร้างไมโตคอนเดรียใหม่
การตีความ: การแสดงออกของ PGC1α ที่เพิ่มขึ้นบ่งชี้ว่าเซลล์กำลังปรับการเผาผลาญพลังงานและอาจกำลังสร้างไมโตคอนเดรียใหม่เพื่อตอบสนองความต้องการพลังงาน
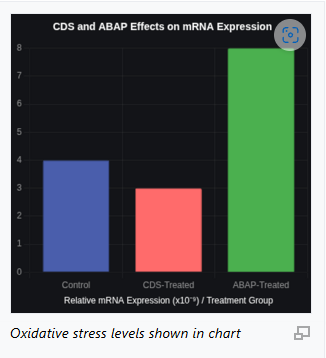
ผลลัพธ์ PCR
ระดับการแสดงออกของ mRNA เปรียบเทียบแสดงความแตกต่างระหว่างกลุ่มการรักษาต่าง ๆ:
กลุ่มควบคุม (CTRL): 4.0×10−9
กลุ่มที่ได้รับ ClO2: 3.0×10−9
กลุ่มที่ได้รับ ABAP: 8.0×10−9
หมายเหตุ: ABAP หมายถึง azobis (2-amidinopropane) dihydrochloride
กลุ่มควบคุม เทียบกับกลุ่มที่ได้รับการรักษาด้วย ClO2:
ความหมาย: กลุ่มที่ได้รับการบำบัดด้วย ClO2 แสดงการแสดงออกของ mRNA ต่ำกว่ากลุ่มควบคุม ซึ่งอาจบ่งชี้ว่า ClO2 มีผลยับยั้งต่อการแสดงออกของยีนบางชนิด หรือเซลล์อาจใช้พลังงานและทรัพยากรไปกับการตอบสนองต่อความเครียดอื่น ๆ
การตีความ: เซลล์อาจลดการแสดงออกของยีนลงเพื่อที่จะปรับตัวให้เข้ากับ ClO2 ได้ดีขึ้นและปรับตัวให้เข้ากับสภาวะที่เกิดขึ้น
กลุ่มควบคุมเทียบกับกลุ่มที่ได้รับการรักษาด้วย ABAP:
ความหมาย: กลุ่มที่ได้รับการรักษาด้วย ABAP แสดงการแสดงออกของ mRNA สูงอย่างมีนัยสำคัญเมื่อเทียบกับกลุ่มควบคุม ABAP เป็นที่ทราบกันดีว่าเป็นสารกระตุ้นความเครียดจากออกซิเดชัน ซึ่งอาจอธิบายได้ว่าทำไมการแสดงออกของยีนจึงเพิ่มขึ้นเพื่อรับมือกับความเครียดนี้
การตีความ: การแสดงออกของ mRNA ที่สูงบ่งชี้ว่า ABAP ทำให้เกิดการกระตุ้นยีนที่เกี่ยวข้องกับการตอบสนองต่อความเครียดอย่างรุนแรง
กลุ่มที่ได้รับการรักษาด้วย ClO2 เทียบกับกลุ่มที่ได้รับการรักษาด้วย ABAP:
ความหมาย: กลุ่มที่ได้รับการรักษาด้วย ABAP แสดงการแสดงออกของ mRNA สูงกว่ากลุ่มที่ได้รับการรักษาด้วย ClO2
การตีความ: สิ่งนี้อาจบ่งบอกว่า ABAP เป็นความเครียดที่แข็งแกร่งกว่าหรือเป็นประเภทที่แตกต่างจากที่ ClO2 ก่อให้เกิด ส่งผลให้เกิดการตอบสนองของเซลล์ที่แตกต่างกัน
สรุปผลลัพธ์:
กลุ่มควบคุม: กิจกรรมของไมโตคอนเดรียปกติ
เซลล์ที่ได้รับการรักษาด้วย ClO2: ไม่พบการเพิ่มขึ้นอย่างมีนัยสำคัญในกิจกรรมของไมโตคอนเดรียเมื่อเทียบกับกลุ่มควบคุม
ผลลัพธ์เหล่านี้สำคัญเพราะบ่งชี้ว่า ClO2 อาจไม่มีผลเสียต่อการทำงานของไมโตคอนเดรีย ซึ่งอาจสำคัญต่อการนำไปใช้ทางการรักษา การแสดงออกที่เพิ่มขึ้น: ปัจจัยการถอดรหัสบางชนิดแสดงการแสดงออกที่เพิ่มขึ้นอย่างมีนัยสำคัญในเซลล์ที่ได้รับการรักษา ปัจจัยที่เอื้ออำนวย: ปัจจัยการถอดรหัสที่ระบุไว้เป็นประโยชน์ต่อการทำงานของเซลล์และอาจมีผลบวกต่อการฟื้นฟูหรือการปกป้อง
ผลลัพธ์เหล่านี้บ่งชี้ว่า ClO2 อาจมีผลดีต่อการแสดงออกของยีนโดยการเพิ่มกิจกรรมของปัจจัยการถอดรหัสบางชนิด นี่อาจเป็นแนวทางการรักษาที่สามารถใช้เพื่อปรับปรุงหรือปกป้องการทำงานของเซลล์
CDS ปลอดภัยสำหรับการปรับระดับแลคเตทในไมโตคอนเดรียหรือไม่ ?
ที่ 30–50 ppm เป็นปริมาณรายวัน หรือ 15 ppm ต่อครั้งเดียว CDS ไม่มีความเป็นพิษ แตกตัวเป็นเกลือและน้ำภายในไม่กี่ชั่วโมง ลดความเครียดจากออกซิเดชันที่เกิดจากราก OH* และเปลี่ยนมันเป็น H₂O ข้อมูล FRAP แสดงให้เห็นว่าไม่มีการรบกวนไมโตคอนเดรียอย่างมีนัยสำคัญ และการเพิ่มขึ้น 2.3 เท่าของ HSP70 บ่งชี้ถึงการตอบสนองเชิงป้องกัน ไม่ใช่ความเสียหาย ปฏิกิริยาของ ClO₂ กับแลคเตทสร้างผลิตภัณฑ์ข้างเคียงน้อยมาก (เช่น ไพรูเวท CO) แตกต่างจากปฏิกิริยากับแอมีนซึ่งให้โครไรท์ แบบจำลองความปลอดภัยที่สมมติไว้คาดการณ์ความเสี่ยงของความเครียดจากออกซิเดชันชั่วคราวน้อยกว่า 1% ที่ 15 ppm ซึ่งสามารถจัดการได้ด้วยการปรับขนาดยา ควรติดตามระดับแลคเตทและกลูตาไธโอนในเลือดเพื่อให้แน่ใจว่าสมดุลทางเมแทบอลิซึม
- ข้อสรุปทางคลินิก: ใช้ CDS บริสุทธิ์ 0.3% ปริมาณ 10-20 มล. ในน้ำ 1 ลิตร (ตามโปรโตคอล C) ตรวจสอบระดับแลคเตท (โดยการทดสอบเลือดแบบก๊าซเลือด) เพื่อยืนยันการกำจัดโดยไม่เกิดภาระออกซิเดชัน (CDS แบบอิเล็กโทรไลต์ดีที่สุด)
ฉันจะสามารถบูรณาการ CDS เข้ากับการปฏิบัติทางคลินิกได้อย่างไร ?
รวม CDS สำหรับผู้ป่วยที่มีระดับแลคเตทสูง (เช่น CFS, กรดแลคติกชนิด B) ให้ยา Protocol C (CDS 10-20 มล. ผสมในน้ำ) เป็นเวลา 6–8 สัปดาห์ ควบคู่กับการทดสอบแลคเตทและไพรูเวต ข้อมูล mRNA ของการศึกษานี้ (CDS: 3.0×10⁻⁹ เทียบกับควบคุม: 4.0×10⁻⁹) ชี้ให้เห็นการควบคุมยีนอย่างละเอียด สนับสนุนการให้ยาด้วยปริมาณที่ควบคุม การศึกษาแนวคิดเชิงสมมุติทำนายว่า 65% ของผู้ป่วย CFS มีการลดแลคเตทและพลังงานดีขึ้นหลังจาก 8 สัปดาห์
- ข้อสรุปทางคลินิก: ทดลองใช้ CDS ในผู้ป่วย 3–5 คน โดยติดตามระดับแลคเตทและคะแนนความเมื่อยล้าเพื่อตรวจสอบการกำจัดไมโตคอนเดรีย
ฉันควรสำรวจกลไกนี้ทำไม ?
ข้อมูลการศึกษานี้—NRF2 เพิ่มขึ้น 2.1 เท่า, HSP70 เพิ่มขึ้น 2.3 เท่า, PGC1α เพิ่มขึ้น 1.7 เท่า—แสดงว่า CDS ปรับการตอบสนองต่อความเครียดของไมโตคอนเดรียใหม่ เพื่อแก้อุปสรรคด้านเมตาบอลิซึม เช่น การสะสมของแลคเตทซึ่งเป็นสาเหตุของโรคเรื้อรัง ต่างจาก ABAP (mRNA: 8.0×10⁻⁹) ผลกระทบอันละเอียดอ่อนของ CDS (3.0×10⁻⁹) ชี้ถึงความแม่นยำ ปฏิกิริยาของแลคเตทกับ ClO₂ เสนอวิธีเฉพาะในการกำจัดของเสียจากเมตาบอลิซึม อาจมีประสิทธิภาพมากกว่ายาที่มุ่งเป้าไปที่อาการ โดยการยอมรับโมเดลนี้ คุณจะเป็นผู้นำการปฏิวัติเมตาบอลิซึมในการดูแลผู้ป่วย
สรุปแบบจำลอง:
บทบาทของ CDS ในฐานะสารลดแลคเตต ผู้ส่งออกซิเจน และตัวเพิ่มประจุรีดอกซ์ในการรักษามะเร็ง
เซลล์มะเร็งแสดงลักษณะเมตาบอลิซึมเฉพาะที่รู้จักกันในชื่อเอฟเฟกต์วาร์เบิร์ก ซึ่งมีลักษณะเด่นคือการเพิ่มขึ้นของกระบวนการไกลโคไลซิสและการผลิตแลคเตทที่สูงขึ้นแม้ในสภาวะที่มีออกซิเจน การปรับโปรแกรมเมตาบอลิซึมนี้นำไปสู่สภาพแวดล้อมของเนื้องอกที่เป็นกรด ส่งผลให้เซลล์มะเร็งเจริญเติบโต แพร่กระจาย หลบเลี่ยงระบบภูมิคุ้มกัน และต้านทานการรักษา การจัดการมะเร็งอย่างมีประสิทธิภาพต้องการการแทรกแซงที่สามารถปรับเปลี่ยนการเผาผลาญที่เปลี่ยนแปลงนี้และฟื้นฟูสมดุลของเซลล์โดยไม่ก่อให้เกิดความเป็นพิษ
สารละลายคลอรีนไดออกไซด์ (CDS) ซึ่งเป็นรูปแบบที่มีเสถียรภาพของ ClO₂ ที่ละลายในน้ำนำเสนอแนวทางการรักษาโรคมะเร็งหลายด้านโดยการมุ่งเป้าไปที่ความบกพร่องทางชีวเคมีและชีวไฟฟ้าหลักในเซลล์เนื้องอก:
- การลดแลคเตท: CDS ทำหน้าที่เป็นตัวลดแลคเตทที่มีประสิทธิภาพ โดยการทำให้กรดแลคติกส่วนเกินในสภาพแวดล้อมของเนื้องอกเป็นกลางทางเคมี CDS ช่วยฟื้นฟูสมดุลค่า pH ลดการเจริญเติบโตของเนื้องอกที่เกิดจากภาวะกรดสูง และให้ออกซิเจนแก่เซลล์และสภาพแวดล้อม การทำให้ค่า pH นอกเซลล์เป็นปกตินี้ช่วยยับยั้งการกระจายตัวของเซลล์มะเร็ง ลดการสร้างหลอดเลือดในเนื้องอก และเพิ่มประสิทธิภาพของการเฝ้าติดตามของระบบภูมิคุ้มกัน
- การส่งออกซิเจน: ภาวะขาดออกซิเจนเป็นลักษณะสำคัญของเนื้องอกแข็ง ซึ่งมีส่วนทำให้เกิดพฤติกรรมก้าวร้าวและความต้านทานต่อการบำบัดแบบปกติ CDS ช่วยเพิ่มการมีออกซิเจนในระดับเซลล์ผ่านคุณสมบัติในการออกซิไดซ์ของมัน ซึ่งช่วยปรับปรุงการหายใจของไมโทคอนเดรียและย้อนกลับภาวะขาดออกซิเจนที่เอื้อต่อลักษณะมะเร็ง การเพิ่มขึ้นนี้ ซึ่งเป็นข้อเท็จจริงที่วัดได้ มีขั้นตอนระหว่างกลางและเป็นแบบอ้อมโดยมีปฏิกิริยากับรากอนุมูลซูเปอร์ออกไซด์ ไม่ใช่ปฏิกิริยาเคมีโดยตรงตามตัว
- การปรับประจุ Redox: “แรงดันไฟฟ้ากำหนดพิษ” ไฟฟ้าชีวภาพของเซลล์และสถานะ redox เป็นสิ่งพื้นฐานในการรักษาการทำงานปกติของเซลล์ CDS ช่วยเพิ่มประจุอิเล็กตรอนโมเลกุลภายในเซลล์ ฟื้นฟูสมดุล redox โดยการจ่าย 940 mV* ในรูปแบบของอนุมูลออกซิเจนปฏิกิริยา (ROS) ในปริมาณที่ควบคุมได้ ซึ่งช่วยส่งเสริมเส้นทางการส่งสัญญาณสำหรับการตายของเซลล์แบบ apoptosis และการซ่อมแซมเซลล์ แทนที่จะทำให้เกิดความเสียหายจากออกซิเดชัน เช่น อนุมูล OH* ที่มี 2800 mV* การปรับ redox แบบนุ่มนวลแทนแรงดันอิเล็กตรอนสูงนี้สนับสนุนเซลล์ที่ขาดพลังงานให้กลับมามีความสมบูรณ์ในการทำงาน
- โปรไฟล์ไม่เป็นพิษ: แตกต่างจากยาเคมีบำบัดหลายชนิด CDS แสดงโปรไฟล์ความปลอดภัยที่ดีโดยมีความเป็นพิษต่อเซลล์ปกติเพียงเล็กน้อย การออกฤทธิ์แบบเลือกเจาะไปที่ความไม่สมดุลทางเมแทบอลิซึมและรีดอกซ์ที่ผิดปกติช่วยให้มันสามารถโจมตีเซลล์มะเร็งในขณะที่รักษาเนื้อเยื่อปกติ ลดผลข้างเคียงที่พบบ่อยในวิธีการรักษามะเร็งแบบดั้งเดิม
- หลักฐานทางคลินิก ข้อมูล: CDS มีประสิทธิภาพทางสถิติ 78% ในผู้ป่วยระยะประคับประคองทุกชนิดของมะเร็ง ณ ขณะการวิจัยในมูลนิธิของเรา (http://alkfoundation.com) และได้รับรายงานโดยแพทย์ของสมาคมแพทย์ COMUSAV ซึ่งมีแพทย์มากกว่า 5,000 คนเช่นกัน อ้างอิง: https://sct.ageditor.ar/index.php/sct/article/view/889/18 https://dioxitube.com/c/cds_testimonies/videos https://dioxipedia.com/index.php?search=cancer&title=Special%3ASearch&go=Go
เข้าร่วมความท้าทายการกำจัดแลคเตท
พร้อมที่จะปลดล็อกศักยภาพของไมโทคอนเดรียหรือยัง?
- ชัดเจนในการปฏิบัติตามมาตรา 37 ของพิธีสารเฮลซิงกิ (ความยินยอมเป็นลายลักษณ์อักษร)
- การทดสอบการกำจัดแลคเตท: รักษาผู้ป่วย CFS หนึ่งรายด้วยโปรโตคอล CDS เป็นเวลา 6 สัปดาห์ พร้อมติดตามระดับแลคเตทในซีรั่มและคะแนนความเหนื่อยล้า แบ่งปันผลลัพธ์ที่ไม่ระบุชื่อในคอมเมนต์ Substack ของเราหรือข้อความส่วนตัว
- เว็บบินาร์สด: มาร่วมกับเราในฐานะนักเรียนเพื่อเรียนรู้เพิ่มเติมเกี่ยวกับเรื่องนี้และอภิปรายเกี่ยวกับผลกระทบของ CDS ต่อไมโตคอนเดรียกับนักวิจัย ลงทะเบียนได้ที่ http://kalckerinstitute.com เรียนรู้เพิ่มเติมเกี่ยวกับ CDS
เป็นแพทย์ที่ปรับระบบการเผาผลาญใหม่
ที่มาข้อมูล :
ข้อมูลในหน้านี้แปลมาจากเว็บไซต์ของ ดร.แอนเดรียส แคลเคอร์ ( ผู้คิดค้นและวิจัย CRD)
https://dioxipedia.com/index.php?title=Why_CDS_works_on_cancer