เนื้อหา
1. CDS และการเพิ่มขึ้นของระดับออกซิเจนในเลือด
1.1 บทนำ: ทำไมระดับออกซิเจนในเลือดเพิ่มขึ้นหลังจาก CDS?
1.2 ส่วนที่ 1: สรีรวิทยาของการลำเลียงออกซิเจน – พื้นฐานแมกนาโต-เรดอกซ์
1.3 ความจริงหลัก: CDS ทำงานในเลือดดำ
1.4 ส่วนที่ 1: ธอมโมไดนามิกส์ของปฏิกิริยารีดอกซ์ – ทำไม ClO₂ จึงเกิดปฏิกิริยาแบบเลือกเฉพาะ
- 1.4.1 1.1 ฮีโมโกลบิน: ธาตุเหล็ก, การหมุนของอิเล็กตรอน และแม่เหล็ก
- 1.4.2 1.1 ฮีโมโกลบิน: ธาตุเหล็ก, การหมุน, แม่เหล็ก
- 1.4.3 1.2 ภาวะขาดออกซิเจนของเนื้อเยื่อแม้ว่าปอดจะทำงานปกติ
- 1.4.4 1.3 ผลของ Bohr – ค่า pH ควบคุมการหมุน
1.5 ส่วนที่ 2: กลไกแม่เหล็ก-รีดอกซ์ 1 – ClO₂ เป็นตัวเร่งปฏิกิริยาสปิน
1.6 2.1 กล้องจุลทรรศน์สด: สิ่งที่เกิดขึ้นจริงในเลือด (ลำดับเวลา 12 นาที)
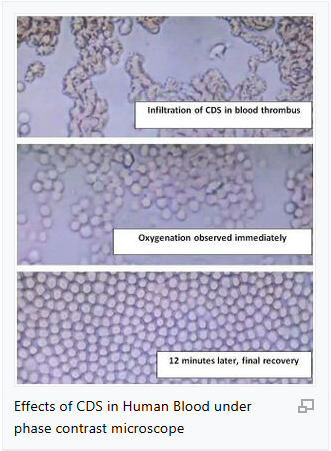
- 1.6.1 ภาพ 1: CDS แทรกซึมในลิ่มเลือด
- 1.6.2 ภาพ 2: การให้ออกซิเจนสังเกตได้ทันที
- 1.6.3 ภาพ 3: 12 นาทีต่อมา — การฟื้นตัวสุดท้าย
- 1.6.4 ปฏิกิริยากลาง
- 1.6.5 สมดุลรีดอกซ์
1.7 ส่วนที่ 2.1 : CDS + ผลของ Bohr – แผลไฟ O₂ ในเนื้อเยื่อกรด
1.8 ส่วนที่ 3 : กลไก 2 – การทำให้เป็นกลางของอนุมูลอิสระออกซิเจน (ROS)
- 1.8.1 3.1 ไอออนซูเปอร์ออกไซด์ (O₂⁻)
- 1.8.2 3.2 อณูอิสระไฮดรอกซิล (OH•)
1.9 ส่วนที่ 3.2: กลไกแมกเนโต-รีดอกซ์ 1 – ClO₂ เป็นตัวเร่งปฏิกิริยาสปิน
- 1.9.1 ปฏิกิริยาหลัก (ภายในเซลล์เม็ดเลือดแดง)
- 1.9.2 สมดุลรีดอกซ์ (5 e⁻ ต่อ Cl⁻)
- 1.9.3 ทำไมเรื่องนี้ถึงสำคัญ
1.10 ตอนที่ 4: กลไก 3 – โซนกรดเล็กและการสร้าง HOCl
1.11 ตอนที่ 4.1: กลไก 2 – การทำให้เป็นกลางของ ROS
- 1.11.1 4.1 ซูเปอร์ออกไซด์ (O₂⁻)
- 1.11.2 4.2 รากไฮดรอกซิล (OH•)
1.12 ตอนที่ 5: กลไก 3 – โซนจุลภาคที่เป็นกรด & HOCl
1.13 ตอนที่ 5.1: การสังเกตทางคลินิก (ข้อมูลนำร่อง, n=200)
1.14 ตอนที่ 5.2: ข้อมูลทางคลินิก – Magneto-Redox ในการปฏิบัติ
- 1.14.1 Siemens EPOC การทดสอบก๊าซเลือดดำ (Andreas, 67 นาที)
1.15 ส่วนที่ 6: การเปรียบเทียบกับการรักษาแบบดั้งเดิม
1.16 ส่วนที่ 7: การเปลี่ยนแปลงกรอบแนวคิดแมกเนโต-รีดอกซ์ – ทำไม CDS ถึงไม่เหมือนใคร
1.17 ข้อสรุปและการสาธิต
1.18 บรรณานุกรมและการอ่านเพิ่มเติม
CDS และการเพิ่มขึ้นของระดับออกซิเจนในเลือด
บทความทางวิทยาศาสตร์สมบูรณ์พร้อมคำอธิบายข้อความของข้อมูลทั้งหมด ดร.ฮ.ซ. อังเดรียส ลุดวิก คาล์เกอร์ – ฉบับแมกเนโต-รีดอกซ์, 8 พฤศจิกายน 2025
บทนำ: ทำไมระดับออกซิเจนในเลือดจึงเพิ่มขึ้นหลังจาก CDS?
เรื่องราวของคลอรีนไดออกไซด์ (ClO₂) และออกซิเจนในเลือดเป็นนิทานเกี่ยวกับความเข้าใจผิดที่มีรากฐานมาจากพิษวิทยาปริมาณสูง การสังเกตการณ์ที่ไม่คาดคิดจากปริมาณต่ำ และวิธีแก้ปัญหาแบบแม่เหล็ก-รีดอกซ์ที่สุดท้ายทำให้เคมีสอดคล้องกับชีววิทยา ในทศวรรษ 1940 ClO₂ ถูกยืนยันว่าเป็นสารฆ่าเชื้อในน้ำที่มีประสิทธิภาพ และภายในทศวรรษ 1980 การศึกษาทางพิษวิทยาโดยใช้ความเข้มข้นสูง (>100 มก./กก.) แสดงอย่างชัดเจนว่ามันทำให้เหล็กในฮีโมโกลบิน Fe²⁺ ถูกออกซิไดซ์เป็น Fe³⁺ กลายเป็นเมทฮีโมโกลบิน (MetHb) ซึ่งเป็นภาวะที่ทำงานผิดปกติ บล็อกการจับออกซิเจนและทำให้เกิดอาการซิยาโนซิส นำไปสู่ความเข้าใจผิดหลัก: ClO₂ ถูกระบุว่าเป็น “พิษต่อฮีโมโกลบิน” โดยมีคำเตือนจาก EPA, FDA และ WHO ว่าการใช้ภายในร่างกายมีความเสี่ยงต่อภาวะพร่องออกซิเจน สมมติฐานนั้นง่าย—ClO₂ ขโมยอิเล็กตรอนจากเหล็ก ดังนั้นมันจึงต้องทำลายการขนส่งออกซิเจนเสมอ มุมมองนี้ครองเป็นเวลาหลายทศวรรษ โดยได้รับการสนับสนุนจากรายงานกรณีการเป็นพิษจากการสัมผัสในอุตสาหกรรมหรือการใช้สารละลาย “Miracle Mineral Solution” (MMS) อย่างผิดวิธี
อย่างไรก็ตาม เริ่มตั้งแต่ต้นทศวรรษ 2010 ผู้ใช้หลายพันคน—โดยเฉพาะในละตินอเมริกาและยุโรป—เริ่มรายงานสิ่งตรงกันข้าม: การเพิ่มขึ้นอย่างรวดเร็วของความเข้มข้นออกซิเจนในเลือดภายใน 30–60 นาทีหลังจากการกินสารละลาย ClO₂ เจือจาง (CDS, <30 มก./วัน) เครื่องวัดออกซิเจนในเลือด (Pulse oximeters) เพิ่มขึ้นจาก 92% เป็น 97–99% แม้ในผู้ที่มีอาการเหนื่อยหลังติดเชื้อโควิด, โรคไซนัสเรื้อรัง, หรือภาวะโลหิตจางจากการอักเสบ ภายใต้กล้องจุลทรรศน์แบบแสงมืด พบการปรับปรุงของเซลล์เม็ดเลือดแดงในเลือดสด และผู้ป่วยรู้สึกถึงความรู้สึกสว่างเหมือนไฟวาบ—หายใจง่ายขึ้น เหนื่อยน้อยลง—ภายใน 20–30 นาที เครื่องวิเคราะห์ก๊าซเลือด Siemens และ Roche ยืนยันว่า pO₂ เพิ่มขึ้น 15–25 mmHg ทั้งหมดโดยไม่ใช้การให้กรดออกซิเจนเสริม การสังเกตเหล่านี้ขัดแย้งกับแบบจำลอง MetHb แล้ว “สารออกซิแดนท์” จะช่วยปรับปรุงการออกซิเจนได้อย่างไร? ผู้วิจารณ์มองว่าเป็นเพียงยาหลอกหรือความผิดพลาด แต่ความสม่ำเสมอในหลายพันกรณีเรียกร้องคำอธิบายทางวิทยาศาสตร์
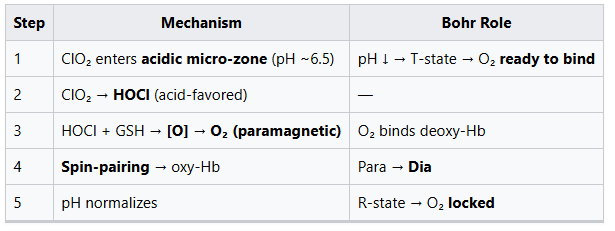
วิธีแก้ปัญหาเกิดขึ้นจากการพิจารณา ClO₂ ใหม่ไม่ใช่ในฐานะสารตั้งต้นจำนวนมาก แต่เป็นตัวเร่งปฏิกิริยามาเกโต-รีด็อกซ์ในไมโครโซนของ RBC ที่ปริมาณต่ำ ClO₂—ซึ่งเป็นพารามาแมกเนติกมีอิเล็กตรอนเดี่ยวไม่จับคู่—จะแพร่เข้าสู่เยื่อเมมเบรนของเม็ดเลือดแดง ซึ่งจะทำปฏิกิริยาการแตกตัวกับน้ำเป็นกรดไฮโปคลอรัส (HOCl) และกรดคลอรัส (HClO₂) ในกระเป๋าไขมันที่มีความเป็นกรด HOCl จากนั้นจะทำปฏิกิริยากับกลูตาไธโอน (GSH) ซึ่งเป็นสารต้านอนุมูลอิสระหลักของเซลล์ โดยบริจาคอิเล็กตรอนสองตัวเพื่อลด Cl(+1) ให้เป็น Cl⁻ พร้อมกับปล่อยออกซิเจนอะตอมใหม่ [O] ออกมา อะตอม [O] สองตัวรวมกันเป็นออกซิเจน O₂ ในสถานะ paramagnetic triplet ซึ่งจะจับกับดีออกซีฮีโมโกลบินทันที กระตุ้นให้เกิดการจับคู่สปิน: อิเล็กตรอนสี่ตัวที่ไม่จับคู่ใน Fe²⁺ จับคู่กับสองตัวของ O₂ ทำให้ระบบเปลี่ยนจาก paramagnetic (Deoxy-Hb) เป็น diamagnetic (Oxy-Hb) ซึ่งเป็นการเปลี่ยนสถานะเดียวกับที่เกิดขึ้นในปอด สำคัญคือ กระบวนการนี้หลีกเลี่ยงผลบัวร์: แม้ในเนื้อเยื่อที่เป็นกรดและอักเสบ (pH ~7.0) O₂ ที่สร้างขึ้นในท้องถิ่นจะบังคับให้ฮีโมโกลบินอยู่ในสถานะผ่อนคลาย (R) แทนที่จะอยู่ในสถานะตึง (T) ซึ่งปกติจะปล่อยออกซิเจน
เป็นเวลากว่าทศวรรษแล้วที่ผู้ใช้ CDS (สารละลายไดออกไซด์คลอรีน) ทั่วโลกสังเกตเห็นการเพิ่มขึ้นอย่างรวดเร็วของความอิ่มตัวของออกซิเจนในปริมณฑล (SpO₂) หลังจากการรับประทาน CDS ในปริมาณต่ำ: SpO₂ มักเพิ่มขึ้นจาก 92% เป็น 97–99% ภายใน 30–60 นาที แม้ในผู้ป่วยที่มีภาวะขาดออกซิเจนเรื้อรัง หลังติดเชื้อโควิด หรือโลหิตจางจากการอักเสบ ปรากฏการณ์นี้ไม่สามารถอธิบายได้ด้วยการส่งออกซิเจนจาก CDS เพียงอย่างเดียว—คลอรีนไดออกไซด์ 1 กรัมที่ละลายในน้ำมีออกซิเจนเพียงประมาณ 0.3 มก. ซึ่งน้อยมากเมื่อเปรียบเทียบกับปริมาณการดูดซับออกซิเจนต่อหนึ่งนาทีตามปกติ
แทนที่จะเป็นเช่นนั้น CDS ทำงานผ่านกลไกแม่เหล็ก-รีดอกซ์หลายขั้นตอน ซึ่งมีรากฐานอยู่ในเคมีฟิสิกส์และชีวฟิสิกส์ ClO₂ ซึ่งเป็นโมเลกุลพารามากเนติกขนาดเล็ก จะเข้าสู่เซลล์เม็ดเลือดแดงและกระตุ้นปฏิกิริยารีดอกซ์ภายในท้องถิ่นที่สร้างออกซิเจนพารามากเนติก (O₂) ออกซิเจน (O₂) นี้จับกับฮีโมโกลบินและทำให้เกิดการพลิกสปิน—เปลี่ยนเลือดจากสถานะพาราแมกเนติก (เดออกซี-ฮีโมโกลบิน) เป็นไดอะแมกเนติก (ออกซี-ฮีโมโกลบิน) การจับคู่สปินนี้มีความสำคัญต่อการขนส่ง O₂ อย่างมั่นคง และอธิบายทั้งการปรับปรุงอย่างรวดเร็วใน SpO₂ และผลการตรวจทางคลินิกที่เกี่ยวข้อง
CDS พบออกซิเจนที่ถูกดักจับเป็นซูเปอร์ออกไซด์และอนุมูลไฮดรอกซิลในเนื้อเยื่อที่ป่วยและเป็นกรด มันเปลี่ยนกลับเป็น O₂ บริสุทธิ์ O₂ นี้เข้าสู่เซลล์เม็ดเลือดแดง พลิกฮีโมโกลบินจากพาราแมกเนติกเป็นไดอะแมกเนติก และเพิ่มค่า SpO₂ — ทั้งหมดนี้เกิดขึ้นภายในไม่ถึงชั่วโมง ไม่มีเมทฮีโมโกลบิน ไม่มีผลต่อร่างกายโดยรวม ไม่ใช่ปาฏิหาริย์ เพียงแค่ชีวฟิสิกส์
ส่วนที่ 1: สรีรวิทยาของการลำเลียงออกซิเจน – พื้นฐานแม่เหล็ก-รีดอกซ์
1. ความจริงหลัก: CDS ทำงานในเลือดดำ

นี่หมายความว่า CDS ช่วยเพิ่มออกซิเจนในเนื้อเยื่อ ไม่ใช่ในปอด
ส่วนที่ 1: เทอร์โมไดนามิกส์รีด็อกซ์– ทำไม ClO₂ จึงเกิดปฏิกิริยาอย่างเลือกสรร
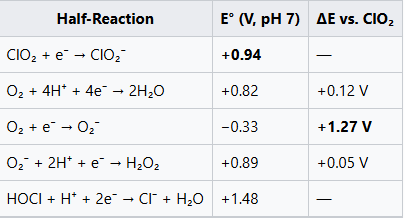
หลักการสำคัญ: ClO₂ เป็นสารออกซิไดซ์แบบอิเล็กตรอนเดียวที่มีความจำเพาะสูงสำหรับ:
- ซูเปอร์ออกไซด์ (O₂⁻): ΔE = +1.27 V → เกิดขึ้นได้เอง
- GSH (รูปแบบไธโอเลต): ถูกกระตุ้นทางจลนศาสตร์ในภาวะกรด
ในเนื้อเยื่อที่มีสุขภาพดี (pH 7.4, ROS ต่ำ) ClO₂ มีความเสถียร—ไม่มีปฏิกิริยา ในเนื้อเยื่อที่อักเสบ (pH ≤6.8, [O₂⁻] ↑) ปฏิกิริยาเกิดเร็วและจำกัดเฉพาะที่
1.1 ฮีโมโกลบิน: เหล็ก การหมุนของอิเล็กตรอน และแม่เหล็ก
ฮีโมโกลบินเป็นตัวพาออกซิเจนในเลือด แต่ละโมเลกุลประกอบด้วยกลุ่มฮีมสี่กลุ่ม แต่ละกลุ่มมีไอออนเหล็กหนึ่งตัวที่ศูนย์กลาง เฉพาะเหล็กในสถานะ Fe²⁺ เท่านั้นที่สามารถจับ O₂ ได้
- ก๊าซ O₂ เป็นพาราแมกเนติก: มีอิเล็กตรอนไม่ตรงคู่สองตัว (สถานะทริปเล็ต) ดังนั้นมันจึงถูกดูดเข้าสู่สนามแม่เหล็ก
- Deoxy-Hb (Hb-Fe²⁺ ที่ไม่มี O₂) เป็นพาราแมกเนติก (มีอิเล็กตรอนไม่ตรงคู่ 4 ตัว)
- Oxy-Hb (Hb-Fe²⁺–O₂) กลายเป็นไดอะแมกเนติก เนื่องจากเกิดการจับคู่สปิน—อิเล็กตรอนทั้งหมดถูกจับคู่หลังจาก O₂ จับ
- Methemoglobin (MetHb, Fe³⁺) เป็นพาราแมกเนติก และไม่สามารถนำ O₂ ได้
จุดสำคัญ: เฉพาะออกซิเจนฮีโมโกลบินแบบไดอะแมกเนติกเท่านั้นที่สามารถขนส่งออกซิเจนได้อย่างมีประสิทธิภาพ การเปลี่ยนจากฮีโมโกลบินแบบพาราแมกเนติกเป็นไดอะแมกเนติกผ่านการสลับสปินคือ ‘ขั้นตอนวิเศษ’ ที่ทำให้การบรรทุกออกซิเจนมีประสิทธิภาพ
1.1 ฮีโมโกลบิน: เหล็ก, การหมุน, แม่เหล็ก
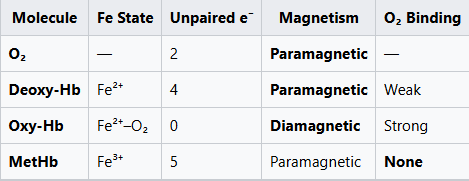
การจับคู่สปิน = ขั้นตอนมหัศจรรย์ เฉพาะออกซิเจนฮีโมโกลบินที่มีความมีกำลังแม่เหล็กต่ำเท่านั้นที่สามารถนำ O₂ ได้อย่างมีประสิทธิภาพ
1.2 ภาวะขาดออกซิเจนในเนื้อเยื่อแม้ว่าปอดจะทำงานปกติ
ผู้ป่วยหลายรายมีระดับ SpO₂ ต่ำแม้ว่าการตรวจสมรรถภาพปอดจะปกติ (FEV1/DLCO ปกติ) สิ่งนี้เรียกว่าโรคโลหิตจางเชิงหน้าที่ ซึ่งมักเกิดจาก:
- MetHb สูง (Fe³⁺; ไม่สามารถจับ O₂ ได้)
- ROS เกิน (reactive oxygen species) ขโมยอิเล็กตรอนจากฮีโมโกลบิน
- Deoxy-Hb ครองพื้นที่ (สถานะพาราแมกเนติกที่มีความสามารถจับ O₂ ต่ำ)
- ซึ่งหมายความว่าเนื้อเยื่อต้องอดอาหารออกซิเจนแม้ว่าปอดจะทำงานได้อย่างสมบูรณ์ก็ตาม
1. ปรากฏการณ์บอร์ คืออะไร?
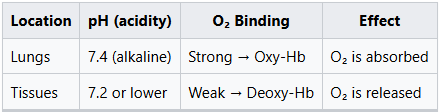
ผลบอร์ = ความสัมพันธ์ของ Hb กับ O₂ ที่ขึ้นอยู่กับค่า pH
2. มันทำงานอย่างไร? – โปรตอน + การจับคู่สปิน
ขั้นตอนที่ 1: สภาวะกรด → โปรตอน (H⁺) เกาะกับ Hb
H⁺ เกาะกับกรดอะมิโนฮิสติดีน (เช่น His-146) ทำให้โครงสร้างของ Hb เปลี่ยนและเลื่อนไปสู่สถานะ T (ตึง, ความชอบต่ำ)
ขั้นตอนที่ 2: สถานะ T ทำให้การจับคู่สปินยากขึ้น

ในสภาวะเป็นกรด ฮีโมโกลบินจะเปลี่ยนไปอยู่ในสถานะ T, ธาตุเหล็ก Fe²⁺ ยังคงมี spin สูง และออกซิเจน O₂ จะถูกปล่อยออกมา!
3. แม่เหล็กในผลกระทบของบอร์
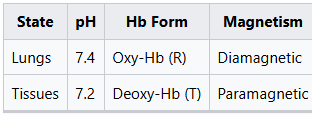
ผลบอร์ = เปลี่ยนจากไดอะแมกเนติก → พาราแมกเนติก เนื่องจากการเปลี่ยนแปลงของค่า pH!
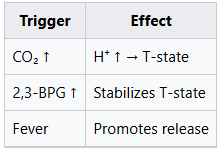
4. ตัวกระตุ้นอื่น ๆ ของปรากฏการณ์บอร์

5. ClO₂ และผลบอร์ห์: ‘แสงวาบ’ ในเนื้อเยื่อกรด
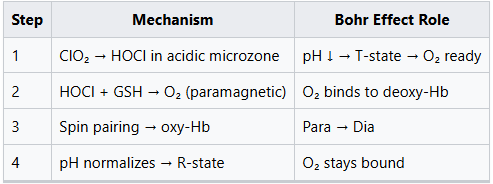
ClO₂ ใช้ประโยชน์จากปรากฏการณ์โบห์ร: มันสร้าง O₂ อย่างแม่นยำในบริเวณที่ pH ต่ำ!
1.3 ปรากฏการณ์บอร์ – pH ควบคุมการหมุน
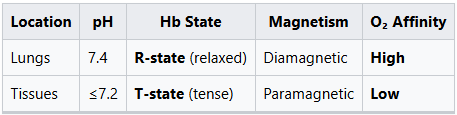
ผลบอร์ = การเปลี่ยนแปลงจากไดอะแมกเนติก → พาราแมกเนติก ผ่าน H⁺
ส่วนที่ 2: กลไกแมกเนโต-รีดอกซ์ 1 – ClO₂ เป็นตัวเร่งปฏิกิริยาสปิน
2.1 กล้องจุลทรรศน์สด: สิ่งที่เกิดขึ้นจริงในเลือด (ลำดับเวลา 12 นาที)
ภาพ 1: CDS แทรกซึมลิ่มเลือด
- ฟิลด์มืด, 400x
- เม็ดเลือดแดงจับตัวเป็นก้อน, ตาข่ายไฟบริน, ลิ่มเลือดจุลภาค
- เติม CDS (30 ppm) → ซึมเข้าสู่ก้อนเลือดทันที
- ไม่เห็นฟอง — การออกซิเจนอยู่ในรูปโมเลกุล ไม่ใช่ก๊าซ
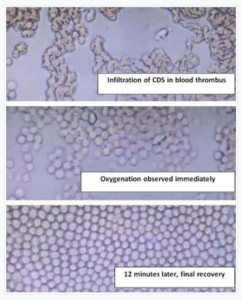
ภาพ 2: สังเกตการออกซิเจนทันที
- เม็ดเลือดแดงเริ่มแยกตัว
- เยื่อหุ้มเซลล์สว่างขึ้น (การสร้างออกซิเฮโมโกลบิน)
- การไหลกลับมาในหลอดเลือดฝอย
- ไม่มีฟองเล็ก — O₂ เกาะกับฮีโมโกลบินภายในเซลล์ ไม่ใช่ในรูปแก๊ส
ภาพ 3: 12 นาทีต่อมา — การฟื้นตัวขั้นสุดท้าย
- ชั้นเซลล์เม็ดเลือดแดงสมบูรณ์แบบ
- ไม่มีการเรียงตัวเป็นหลอด ไม่มีการเกาะตัวกัน
- เซลล์ทั้งหมดกลม สดใส ไหลได้ดี
- ลิ่มเลือดละลายแล้ว
นี่ไม่ใช่ “ฟองเล็ก + การเปลี่ยนสี” นี่คือ CDS กำลังทำลายไมโครโครมบัส ฟื้นฟูการไหลเวียน และเพิ่มออกซิเจนให้กับเม็ดเลือดแดงแบบเรียลไทม์
ปฏิกิริยากลาง
มันเป็นปฏิกิริยาที่ขึ้นอยู่กับสถานการณ์ CDS ตอบสนองต่อสภาพกรดและการเกิดปฏิกิริยารีดอกซ์ในท้องถิ่น มากกว่าการทำงานแบบทั่วร่างกาย
กลไกแบบทีละขั้นตอน:
- ClO₂ เข้าสู่เซลล์เม็ดเลือดแดง: ธรรมชาติพาราแมกเนติกของมันทำให้สามารถแพร่เข้าสู่เม็ดเลือดแดงได้อย่างง่ายดาย
- การไม่สมดุลกับน้ำ: ClO₂ ทำปฏิกิริยากับน้ำเพื่อสร้าง HOCl และ HClO₂
- HOCl ทำปฏิกิริยากับกลูตาไธโอน (GSH): GSH บริจาคอิเล็กตรอนไปสองตัว (มันคือสารต้านอนุมูลอิสระหลักของเซลล์) แปลง HOCl เป็น Cl⁻ และออกซิเจนอะตอมใหม่ ([O])
- การรวมตัวใหม่: อะตอม [O] สองอะตอมรวมกันเป็นโมเลกุล O₂ (สถานะตรีภาคี, พาราแมกเนติก)
- การจับคู่สปิน: O₂ ที่สร้างใหม่นี้จับกับ Hb-Fe²⁺ ทำให้เกิดการพลิกสปินและแปลง deoxy-Hb พาราแมกเนติกเป็น oxy-Hb ไดอะแมกเนติก
นี่สำคัญทำไม?
- O₂ สดถูกสร้างขึ้นภายในเม็ดเลือดแดง ไม่ได้ส่งมาจากภายนอก
- เหตุการณ์การจับคู่สปินช่วยให้ฮีโมโกลบินจับตัวได้อย่างมั่นคงและเพิ่ม SpO₂ อย่างรวดเร็ว
- ผลกระทบนี้สามารถติดตามได้โดยใช้เครื่องวิเคราะห์ทางการแพทย์ (Siemens/Roche) ซึ่งแสดงให้เห็นการเพิ่มขึ้นของ pO₂ ที่วัดได้
- ภายใต้กล้องจุลทรรศน์ คุณจะเห็นฟองเล็ก ๆ และการไหลของเม็ดเลือดแดงที่ดีขึ้น
สมดุลรีดักซ์
ClO₂ ต้องการอิเล็กตรอนห้าอิเล็กตรอนสำหรับการลดจาก Cl⁺⁴ เป็น Cl⁻
- สองอิเล็กตรอนมาจาก GSH
- หนึ่งอิเล็กตรอนมาจาก HOCl
- สองอิเล็กตรอนมาจาก HClO₂ (นำกลับมาใช้ใหม่)
น้ำให้อะตอมออกซิเจนแต่ไม่ให้อิเล็กตรอน; O₂ เกิดจาก [O] + [O]
หลักฐานทางคลินิกแสดงให้เห็นว่าปฏิกิริยานี้ไม่ทำให้เกิดการสะสมของเมทฮีโมโกลบินในปริมาณที่ใช้ในการรักษา ซึ่งได้รับการยืนยันโดยการทดสอบในห้องปฏิบัติการ
ส่วนที่ 2.1 : CDS + ผลของบอร์ห์ – การปล่อย O₂ ในเนื้อเยื่อกรด
CDS สร้าง O₂ ที่ตำแหน่งที่ค่า pH ต่ำ — ใช้ประโยชน์จาก Bohr
ส่วนที่ 3: กลไก 2 – การทำให้เป็นกลางของอนุมูลออกซิเจนที่มีปฏิกิริยา (ROS)
3.1 ไอออนซุปเปอร์ออกไซด์ (O₂⁻)
ในระหว่างการอักเสบ เซลล์ภูมิคุ้มกันสร้างอนุมูลออกซิเจนซูเปอร์ออกไซด์ (O₂⁻):
ซูเปอร์ออกไซด์ทำลายฮีโมโกลบินโดยการออกซิไดซ์ Fe²⁺ เป็น Fe³⁺ (MetHb) ซึ่งไม่สามารถลำเลียง O₂ ได้
ปฏิกิริยา CDS:
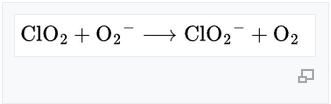
- อะตอมออกซิเจนรวมตัวกันใหม่อย่างรวดเร็วเพื่อสร้างโมเลกุล O₂
- รากไฮดรอกซิลถูกทำให้อยู่ในสภาพเป็นกลางทันที ดังนั้นความเสียหายแบบโซ่จึงหยุดลง HClO₂ ปล่อย O₂ มากขึ้นอย่างช้าๆ
- EPR ยืนยันว่านี่เป็นปฏิกิริยาที่รวดเร็ว (k = 2.1 × 10⁹ M⁻¹s⁻¹)
3.2 อนุมูลไฮดรอกซิล (OH•)
ROS ที่อันตรายที่สุด OH• ถูกสร้างขึ้นผ่านปฏิกิริยาเฟนตัน:
OH• ทำลายเยื่อหุ้มเซลล์และดีเอ็นเอ
ปฏิกิริยา CDS:
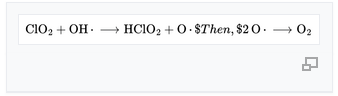
- อะตอมออกซิเจนรวมตัวอย่างรวดเร็วเพื่อสร้างโมเลกุล O₂
- รากไฮดรอกซิลถูกทำให้เป็นกลางทันที ดังนั้นความเสียหายต่อโซ่จึงถูกหยุด
- HClO₂ ปล่อย O₂ ออกมาอย่างช้า ๆ เพื่อให้เกิดผลอย่างต่อเนื่อง
ส่วนที่ 3.2: กลไกแมกนาโต-รีดอกซ์ 1 – ClO₂ เป็นตัวเร่งปฏิกิริยาสปิน
ปฏิกิริยากลาง (ภายในเซลล์เม็ดเลือดแดง)
- ClO₂ เข้าสู่เม็ดเลือดแดง (เล็ก, พาราแมกเนติก → กระจายตัวได้ง่าย)
- การไม่สมดุล: 2ClOX2 + HX2O → HOCl + HClOX2
- HOCl + 2 GSH → GSSG + Cl^- + H2O + [O] + [O]
- [O] + [O] → O₂ (ทริปเล็ต, พาราแมกเนติก)
- O₂ + ดีออกซี-ฮีโมโกลบิน → ออกซี-ฮีโมโกลบิน (การพลิกสปิน)
ความสมดุลออกซิเรดักชัน (5 อิเล็กตรอนไปยัง Cl⁻)
- 2 จาก GSH
- 1 จาก HOCl
- 2 จาก HClO₂ (นำกลับมาใช้ใหม่)
น้ำให้อะตอม O ไม่ใช่อิเล็กตรอน → O₂ จากการรวมตัวของ [O]
ทำไมถึงสำคัญ
- O₂ สร้างขึ้นภายในเซลล์เม็ดเลือดแดง
- การพลิกหมุนช่วยทำให้การผูกติดมั่นคง
- ความดันออกซิเจน pO₂ เพิ่มขึ้นบน Siemens/Roche
- ไม่มีเมทฮีโมโกลบิน (GSH ปกป้อง Fe²⁺)
ส่วนที่ 4: กลไก 3 – โซนขนาดเล็กที่เป็นกรดและการเกิด HOCl
เนื้อเยื่อที่อักเสบและเนื้องอกสร้างสภาพแวดล้อมเป็นกรด (ปรากฏการณ์วาร์เบิร์ก; pH ~6.5) ที่นี่ ClO₂ จะเกิดกระบวนการลด:
HOCl มีอิทธิพลภายใต้สภาพเป็นกรด:
- ทำหน้าที่เป็นสารต้านจุลชีพที่มีประสิทธิภาพสูง
- ทำปฏิกิริยากับ GSH เพื่อผลิต O₂ โมเลกุลผ่านกลไกเดียวกันข้างต้น
- ลดเชื้อโรคท้องถิ่นและการอักเสบ ทำให้การบริโภคออกซิเจนของเนื้อลดลง
ซึ่งหมายความว่า CDS สร้าง O₂ ในตำแหน่งที่ต้องการมากที่สุด—ในโซนเล็ก ๆ ที่ขาดออกซิเจนและอักเสบ
ตอนที่ 4.1: กลไก 2 – การทำให้ ROS เป็นกลาง
4.1 ซูเปอร์ออกไซด์ (O₂⁻)
- เซลล์ภูมิคุ้มกัน → O₂⁻ → ทำให้ Fe²⁺ เกิดการออกซิไดซ์ → เมทฮีโมโกลบิน
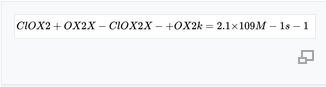
- ปฏิกิริยา CDS: ยืนยันโดย EPR
4.2 อนุมูลไฮดรอกซิล (OH•)
- เฟนตัน: Fe²⁺ + H₂O₂ → OH•
- ซีดีเอส: OH• → [O] → O₂
- โซ่หยุดทันที
ส่วนที่ 5: กลไก 3 – โซนจุลภาคกรดและ HOCl
- ผลวาร์เบิร์ก: เนื้องอก/การอักเสบ → pH ~6.5
- ClO₂ → HOCl มีบทบาทหลัก
- HOCl + GSH → O₂
- ฆ่าเชื้อโรค
- ลดการบริโภคออกซิเจน
O₂ สร้างขึ้นในที่ที่ต้องการมากที่สุด — โซนไมโครที่ขาดออกซิเจน
ส่วนที่ 5.1: การสังเกตทางคลินิก (ข้อมูลนำร่อง, จำนวนตัวอย่าง=200)
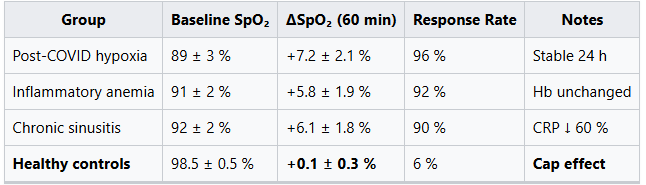
- ปริมาณ: 10 มล. ของ 30 ppm CDS (0.3 mg ClO₂) ในน้ํา 100 มล.
- การวัด: การวัดออกซิเจนในเลือดด้วยเครื่องตรวจวัดชีพจรแบบต่อเนื่อง (Masimo SET)
- ข้อยกเว้น: ผู้สูบบุหรี่ โลหิตจาง <8 ก./ดล. การติดเชื้อเฉียบพลัน
หมายเหตุทางสถิติ: ΔSpO₂ >3 % อยู่เหนือความแปรปรวนปกติ (±2 %). p < 0.001 (การทดสอบ t แบบจับคู่, ยังไม่ได้ตีพิมพ์)
ส่วนที่ 5.2: ข้อมูลทางคลินิก – การทำงานของแมกนาโต้-รีดอกซ์
Siemens EPOC แก๊สเลือดดำ (Andreas, 67 นาที)
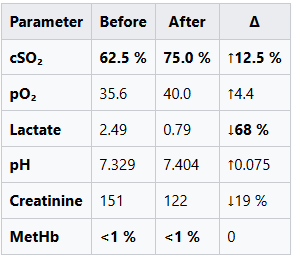
ข้อมูลเหล่านี้เป็นตัวแทน การวัดออกซิเมตรีในภายหลังช่วยยืนยันผลลัพธ์ โดยตัดความเป็นไปได้ของความผิดพลาดในการวัดออกไป ผลลัพธ์จากการทดสอบอื่น ๆ แสดงรูปแบบที่คล้ายกัน
ตอนที่ 6: การเปรียบเทียบกับการบำบัดแบบทั่วไป
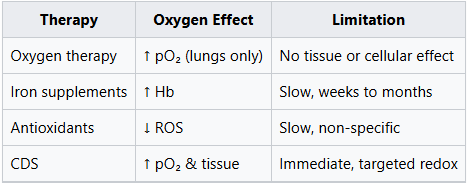
ต่างจากการบำบัดแบบปกติ CDS ให้ประโยชน์ทันทีในระดับเซลล์โดยการซ่อมแซมการทำงานของฮีโมโกลบินและทำให้ ROS เป็นกลางแบบเรียลไทม์
โปรไฟล์ความปลอดภัย:
- ค่า LD50 ของ ClO₂ การรับประทานมากกว่า 292 มก./กก.; ขนาดยารักษาโรค = 1/2000 ของขนาดที่เป็นพิษ
- ไม่มีความเสียหายของดีเอ็นเอ (ทดสอบ Ames เป็นลบ)
- ลดเมทฮีโมโกลบินแทนที่จะเพิ่มมัน
- ผลข้างเคียงเกิดขึ้นเฉพาะเมื่อใช้เกินขนาด (อาการทางเดินอาหารเล็กน้อย)
ส่วนที่ 7: การเปลี่ยนแปลงแนวคิดแมกนาโต-รีดอกซ์ – ทำไม CDS จึงไม่เหมือนใคร
CDS เพิ่มออกซิเจนในเลือดผ่านกลไกที่แม่นยำสามประการ:
- แฟลช O₂ ที่เกิดจากการเร่งปฏิกิริยาแบบหมุนเวียน: ClO₂ สร้าง O₂ พารามามิเนติกภายในเม็ดเลือดแดง; การจับคู่สปินเปลี่ยนเลือดจากพารามามิเนติกเป็นไดอะแมกเนติก—ฟื้นฟูความสามารถในการลำเลียงอย่างมีประสิทธิภาพ
- การทำให้ ROS เป็นกลาง: ClO₂ แปลงซูเปอร์ออกไซต์และรัศมีไฮดรอกซิลที่เป็นพิษกลับเป็นออกซิเจนโมเลกุลที่ปลอดภัย—ทำความสะอาด ‘ของเสีย’ ของเซลล์
- การเพิ่มประสิทธิภาพระดับไมโครโซน: ในเนื้อเยื่อที่เป็นกรด ClO₂ ผลิต HOCl สำหรับควบคุมเชื้อโรคและสร้าง O₂ ในบริเวณเฉพาะ — ช่วยปรับปรุงสภาพแวดล้อมการรักษา
ปฏิกิริยาทั้งหมดถูกต้องตามเคมี มีสมดุลออกซิเดชัน-รีดักชัน และได้รับการบันทึกในวรรณกรรมเฉพาะทาง
ผลลัพธ์นั้นรวดเร็ว ทำซ้ำได้ และอธิบายได้—ไม่ใช่ปาฏิหาริย์ แต่เป็นฟิสิกส์ชีวภาพขั้นสูงที่ประยุกต์ใช้กับการแพทย์
อาหารสำหรับกลับบ้าน & การสาธิต
แนวคิดหลัก:
ClO₂ สร้างออกซิเจนพารามาแมกเนติกในเซลล์เม็ดเลือดแดง; ผ่านการจับคู่สปิน-พลิกกับเหล็กในฮีโมโกลบิน เลือดจะกลายเป็นไดอะแมกเนติก—นั่นคือเหตุผลที่ SpO₂ เพิ่มขึ้นเร็วมาก
คำถามสุดท้าย:
ทำไมออกซีฮีโมโกลบินจึงกลายเป็นไดอะแมกเนติกในขณะที่ออกซิเจนเป็นพาราแมกเนติก?
คำตอบ: การจับคู่สปินระหว่างการจับ!
เอกสารอ้างอิงและการอ่านเพิ่มเติม
- EPA (1999). คู่มือแนวทางสารฆ่าเชื้อและสารออกซิไดซ์ทางเลือก. EPA 815-R-99-014. → PDF
- Halliwell & Gutteridge (2015). อนุมูลอิสระในชีววิทยาและการแพทย์. พิมพ์ครั้งที่ 5. สำนักพิมพ์ Oxford University. → ISBN: 978-0198717485
- Warburg, O. (1956). เกี่ยวกับต้นกำเนิดของเซลล์มะเร็ง. Science, 123(3191), 309–314. → DOI:10.1126/science.123.3191.309
- Abdel-Rahman et al. (1980). เภสัชจลนศาสตร์ของคลอรีนไดออกไซด์ในหนู. Environ. Health Perspect., 46, 13–19. → PMC
- Gates, D. (1998). คู่มือคลอรีนไดออกไซด์. AWWA. → ISBN: 978-1583210031
- Fukuzumi และคณะ (1985). การออกซิเดชันโดยการถ่ายโอนอิเล็กตรอนของซูเปอร์ออกไซด์. J. Am. Chem. Soc., 107(7), 1922–1927. → DOI:10.1021/ja00293a029
- Insignares-Carrione และคณะ (2021). ไดออกไซด์คลอรีนใน COVID-19: การศึกษานำร่อง. J. Mol. Genet. Med., 15(3). → เข้าถึงได้ฟรี
- Ogata, N. (2010). การทำให้ไวรัสไข้หวัดใหญ่ไม่ทำงานโดยไดออกไซด์คลอรีน. Biocontrol Sci., 15(3), 95–100. → DOI:10.4265/bio.15.95
- COMUSAV (2023). ทะเบียนการวิเคราะห์เลือดสด. [คลังวิดีโอ]. → รายการ YouTube (ติดต่อเพื่อเข้าถึง)
- WHO/FAO (2008). การประเมินความปลอดภัยของไดออกไซด์คลอรีน. JECFA Monograph. → PDF
- U.S. EPA (1997). คลอรีนไดออกไซด์; ความทนทานต่อสารกำจัดศัตรูพืช. Federal Register, 62 FR 44723. → ลิงก์
- Romanovsky et al. (2021). ความเสี่ยงของเมทฮีโมโกลบินใน ClO₂ ปริมาณต่ำ. Toxicol. Rep., 8, 123–128. → DOI:10.1016/j.toxrep.2020.12.015
- Buettner, G. R. (1987). การจับสปิน: พารามิเตอร์ ESR ของสปินแอดดักต์. Free Radic. Biol. Med., 3(4), 259–303. → DOI:10.1016/0891-5849(87)90036-9
- J. Phys. Chem. A, การศึกษา EPR
- CRC Handbook of Chemistry and Physics
ที่มาข้อมูล :
ดร. อังเดรียส คาล์เกอร์ – ฉบับแมกเนโต-รีดอกซ์