หน้าหลักนี้ประกอบด้วยเอกสารฉบับแปลของบทความวิชาการต้นฉบับ อย่างไรก็ตาม เรา ได้จัดทำสรุปเนื้อหาที่สำคัญแบบย่อยง่ายไว้ให้ผู้อ่านได้ศึกษาเป็นลำดับแรก เพื่อให้เข้าใจภาพรวมของงานวิจัยชิ้นนี้ได้อย่างรวดเร็ว หากท่านมีความสนใจในรายละเอียดเชิงลึกหรือข้อมูลทางสถิติเพิ่มเติม ท่านสามารถเลือกอ่านเอกสารฉบับเต็มได้ทั้งในรูปแบบภาษาอังกฤษ (Original) ได้ที่ลิงกนี้: https://esmed.org/MRA/mra/article/view/4218 หรือหากต้องการอ่านฉบับภาษาไทย (Translated) เราได้จัดทำบทแปลไว้ให้แล้วในหน้านี้ (ล่างสุด)
บทความวิจัยนี้ศึกษาประสิทธิภาพของ สารละลายคลอรีนไดออกไซด์ (Chlorine Dioxide – ClO2) ในการกำจัดเชื้อแบคทีเรียที่ดื้อต่อยาปฏิชีวนะ (Antimicrobial Resistance – AMR) จำนวน 5 ชนิด ได้แก่ E. coli, S. aureus, K. pneumoniae, S. pneumoniae, A. baumannii และ P. aeruginosa ซึ่งเป็นสาเหตุสำคัญของการเสียชีวิตทั่วโลก โดยผลการทดลองในห้องปฏิบัติการ (In Vitro) พบว่าการใช้สารละลายคลอรีนไดออกไซด์ที่ความเข้มข้นเพียง 7 ppm (ส่วนในล้านส่วน) สามารถกำจัดเชื้อแบคทีเรียดื้อยาเหล่านี้ได้มากกว่า 95% ภายในระยะเวลาอันสั้น งานวิจัยระบุว่าคลอรีนไดออกไซด์มีคุณสมบัติเป็นสารต้านจุลชีพที่เลือกทำลายตามขนาด (Size-selective) โดยสามารถทำลายจุลินทรีย์ขนาดเล็กได้อย่างรวดเร็วผ่านกระบวนการออกซิเดชัน แต่จะไม่ทำลายเนื้อเยื่อของสิ่งมีชีวิตขนาดใหญ่อย่างมนุษย์หรือสัตว์หากใช้ในความเข้มข้นต่ำและระยะเวลาที่เหมาะสม จึงถือเป็นทางเลือกที่มีศักยภาพและมีประสิทธิภาพสูงในการรับมือกับวิกฤตการณ์เชื้อดื้อยาในปัจจุบัน
ข้อมูลการเผยแพร่
-
ชื่อบทความ: Eradication of Antibiotic-Resistant E. coli, S. aureus, K. pneumoniae, S. pneumoniae, A. baumannii, and P. aeruginosa with Chlorine Dioxide In Vitro
-
ผู้เขียน: Georgiou, G.
-
วารสารที่ตีพิมพ์: Medical Research Archives (โดย European Society of Medicine)
-
ปีที่พิมพ์: 2023 (กรกฎาคม)
บทคัดย่อ
การดื้อยาปฏิชีวนะของแบคทีเรีย (AMR) เป็นปัญหาในทุกภูมิภาค โดยมีเชื้อโรค 6 ชนิดที่เป็นสาเหตุของการเสียชีวิตถึง 73.4% จากการดื้อยาปฏิชีวนะของแบคทีเรีย ได้แก่ Escherichia coli (E. coli), Staphylococcus aureus (S. aureus), Klebsiella pneumoniae (K. pneumoniae), Streptococcus pneumoniae (S. pneumoniae), Acinetobacter baumannii (A. baumannii) และ Pseudomonas aeruginosa (P. aeruginosa) องค์การอนามัยโลกได้ริเริ่มแผนปฏิบัติการระดับโลกเกี่ยวกับการดื้อยาปฏิชีวนะในปี 2021 ซึ่งยังคงดำเนินการอยู่จนถึงปัจจุบัน ค่าใช้จ่ายด้านการดูแลสุขภาพที่เกี่ยวข้องกับการดื้อยาปฏิชีวนะทั่วโลกมีมูลค่าหลายพันล้านดอลลาร์ การวิจารณ์เรื่องการดื้อยาต้านจุลชีพที่ได้รับมอบหมายจากรัฐบาลอังกฤษระบุว่า การดื้อยาปฏิชีวนะอาจคร่าชีวิตผู้คนได้ถึง 10 ล้านคนต่อปีภายในปี 2050 และได้กลายเป็นภัยคุกคามด้านสาธารณสุขที่ยิ่งใหญ่ที่สุดอย่างหนึ่งในศตวรรษที่ 21 เชื้อแบคทีเรียดื้อยาปฏิชีวนะเพียงชนิดเดียว คือ Staphylococcus aureus ที่ดื้อต่อเมธิซิลลิน (MRSA) ทำให้มีผู้เสียชีวิตทั่วโลกมากกว่า 100,000 ราย และเชื้อแบคทีเรียดื้อยาปฏิชีวนะอีก 4 ชนิดที่กล่าวถึงในงานวิจัยนี้ก็ทำให้มีผู้เสียชีวิตจำนวนมากเช่นกัน งานวิจัยนี้มุ่งเน้นศึกษาประสิทธิภาพของคลอรีนไดออกไซด์ในการกำจัดแบคทีเรียดื้อยาปฏิชีวนะ 5 ชนิดในหลอดทดลอง ในฐานะวิธีการรักษาใหม่ที่มีประสิทธิภาพ งานวิจัยนี้ใช้ความเข้มข้นของคลอรีนไดออกไซด์ที่แตกต่างกันกับแบคทีเรียดื้อยาปฏิชีวนะ 5 ชนิด ตั้งแต่ 1-7 ppm
ผลการศึกษาเปรียบเทียบการฆ่าเชื้อกับกลุ่มควบคุม และแสดงให้เห็นว่าความเข้มข้น 7 ppm สามารถฆ่าเชื้อได้มากกว่า 95% คลอรีนไดออกไซด์เป็นสารต้านจุลชีพที่เลือกขนาด สามารถฆ่าจุลินทรีย์ขนาดไมครอนได้อย่างรวดเร็ว แต่จะไม่ก่อให้เกิดอันตรายต่อสิ่งมีชีวิตขนาดใหญ่ เช่น สัตว์หรือมนุษย์ เนื่องจากไม่สามารถแทรกซึมลึกเข้าไปในเนื้อเยื่อของพวกมันได้ จึงปลอดภัยเมื่อใช้ในความเข้มข้นต่ำและระยะเวลาสั้นๆ จำเป็นต้องมีการทดลองทางคลินิกเพื่อเก็บเกี่ยวประสบการณ์เกี่ยวกับปริมาณยาและวิธีการที่ดีที่สุดในการกำจัดจุลินทรีย์ดื้อยาปฏิชีวนะออกจากร่างกาย
บทนำ
แบคทีเรียดื้อยาปฏิชีวนะ 5 ชนิดที่เราใช้ในการศึกษาวิจัยนี้ ได้แก่ Escherichia coli, Staphylococcus aureus ที่ดื้อต่อเมธิซิลลิน, Klebsiella pneumonia, Acinetobacter baumannii และ Pseudomonas aeruginosa กลุ่มธนาคารโลกในปี 2017 เตือนว่าในปี 2050 การติดเชื้อดื้อยาอาจก่อให้เกิดความเสียหายทางเศรษฐกิจทั่วโลกเทียบเท่ากับวิกฤตการณ์ทางการเงินในปี 2008 การดื้อยาต้านจุลชีพยังคุกคามการบรรลุเป้าหมายการพัฒนาที่ยั่งยืนหลายประการของสหประชาชาติ โดยเฉพาะอย่างยิ่งเป้าหมายด้านสุขภาพที่ดีและความเป็นอยู่ที่ดี ค่าใช้จ่ายในโรงพยาบาลประมาณการไว้มากกว่า 900 ล้านยูโรในปี 2007 ค่าใช้จ่ายผู้ป่วยนอกอยู่ที่ 10 ล้านยูโร และการสูญเสียผลิตภาพจากการทำงานอยู่ที่ 150 ล้านยูโร นอกจากนี้ การสูญเสียผลิตภาพเนื่องจากการติดเชื้อที่ทำให้เสียชีวิตประมาณการไว้ประมาณ 450 ล้านยูโรต่อปี ต้นทุนทางเศรษฐกิจเหล่านี้จะสูงขึ้นอย่างมากหากใช้ตัวเลขที่รายงานไว้ในรายงานภาระทั่วโลกของเชื้อแบคทีเรียดื้อยาต้านจุลชีพในปี 2019 เนื่องจากแบคทีเรียดื้อยาต้านจุลชีพแพร่หลายไปทั่วโลก และยาปฏิชีวนะมีประสิทธิภาพลดลงเรื่อยๆ การค้นหาวิธีการธรรมชาติและวิธีใหม่ๆ ในการกำจัดเชื้อแบคทีเรียเหล่านี้จึงเป็นสิ่งจำเป็น คลอรีนไดออกไซด์เป็นวิธีที่ปลอดภัยและมีประสิทธิภาพในการกำจัดแบคทีเรียดื้อยาต้านจุลชีพโดยไม่ก่อให้เกิดการดื้อยาเพิ่มขึ้น การค้นพบสารต้านแบคทีเรียจากธรรมชาติชนิดใหม่ที่มีกลไกการออกฤทธิ์ใหม่ยังคงเป็นสิ่งสำคัญลำดับต้นๆ ทั่วโลก
หลังการรักษาแบคทีเรียดื้อยาปฏิชีวนะ
นับตั้งแต่การค้นพบเพนิซิลลินในปี 1940 มีการพัฒนายาปฏิชีวนะมากกว่า 150 ชนิด และยาปฏิชีวนะส่วนใหญ่ที่มีอยู่ในปัจจุบันนั้น แบคทีเรียที่ใช้รักษาได้เกิดการดื้อยาขึ้นแล้ว ด้วยเหตุนี้ ภายในปี 2050 จำนวนผู้เสียชีวิตอาจสูงมากอย่างน่าตกใจ คือ 1 คนทุกๆ สามวินาที แบคทีเรียได้ดื้อต่อยาปฏิชีวนะเกือบทุกชนิดที่พัฒนาขึ้นในช่วง 50 ปีที่ผ่านมา มีความสัมพันธ์เชิงบวกระหว่างการใช้และการแพร่หลายของยาปฏิชีวนะ โดยอัตราจะสูงขึ้นในประเทศที่มีการใช้ยาปฏิชีวนะสูงกว่า6 การสั่งจ่ายยาที่ไม่เหมาะสมโดยแพทย์ที่สั่งจ่ายยาปฏิชีวนะผิดประเภทสำหรับโรคติดเชื้ออื่นๆ เช่น การติดเชื้อไวรัสหรือเชื้อรา แทนที่จะเป็นการติดเชื้อแบคทีเรีย มีสมมติฐานว่าการใช้ยาปฏิชีวนะมากเกินไปมีความสัมพันธ์กับการสั่งจ่ายและการให้ยาปฏิชีวนะที่ไม่เหมาะสม7 การใช้ยาปฏิชีวนะอย่างไม่รับผิดชอบเป็นปัญหาหลักของการดื้อยาปฏิชีวนะ อิทธิพลของยาปฏิชีวนะกำลังลดลงเนื่องจากการดื้อยาที่เพิ่มขึ้นอย่างต่อเนื่องในยาต้านจุลชีพทุกชนิด
การดื้อยาปฏิชีวนะที่เพิ่มขึ้นเกิดจากปัจจัยหลายอย่างรวมกัน ได้แก่ เชื้อโรคที่สัมผัสกับยาปฏิชีวนะ การแพร่กระจายของเชื้อโรคเหล่านั้น และกลไกการดื้อยาของพวกมัน ยาปฏิชีวนะไม่เพียงแต่มีประสิทธิภาพลดลงเท่านั้น แต่การใช้ยาปฏิชีวนะยังอาจทำให้เกิดภาวะเสียสมดุลของจุลินทรีย์ในลำไส้ โดยเฉพาะในลำไส้หรือบริเวณที่มีการติดเชื้อแทรกซ้อน ผลกระทบต่อสุขภาพของมนุษย์อาจร้ายแรงมาก การใช้ยาปฏิชีวนะซ้ำมากเกินไปได้รับการพิสูจน์แล้วว่าทำลายจุลินทรีย์ในลำไส้ตามธรรมชาติส่วนใหญ่ บริษัทยายังไม่เต็มใจที่จะลงทุนในการพัฒนายาปฏิชีวนะด้วยเหตุผลหลายประการ รวมถึงผลตอบแทนต่ำในตลาด ข้อจำกัดในการใช้ยาปฏิชีวนะ ความยากลำบากทางวิทยาศาสตร์ในการพัฒนายาปฏิชีวนะ และสภาพแวดล้อมด้านกฎระเบียบที่มีอยู่ เส้นทางในการค้นหายาปฏิชีวนะใหม่และพัฒนาให้เป็นยานั้นยาวนานและมีค่าใช้จ่ายสูง การนำยาใหม่เข้าสู่ตลาดมีค่าใช้จ่าย 800 ล้านถึง 1 พันล้านดอลลาร์ โดยเฉลี่ยแล้วต้องใช้เวลามากกว่าสิบปีจึงจะเข้าสู่การทดลองทางคลินิก เนื่องจากแรงกดดันด้านเวลาที่เราเผชิญในการต่อสู้กับเชื้อดื้อยา จึงจำเป็นต้องมีแนวทางที่แตกต่างออกไปในการสำรวจทางเลือกอื่นนอกเหนือจากการรักษาด้วยยาปฏิชีวนะ เมื่อเปรียบเทียบกับสาเหตุการเสียชีวิตพื้นฐานทั้งหมดในรายงาน Global Burden of Diseases, Injuries, and Risk Factors Study (GBD) ปี 2019 การดื้อยาต้านจุลชีพ (AMR) จะเป็นสาเหตุการเสียชีวิตระดับ 3 ของ GBD อันดับสามในปี 2019 โดยพิจารณาจากสถานการณ์สมมติที่ไม่มีการติดเชื้อ มีเพียงโรคหลอดเลือดหัวใจตีบและโรคหลอดเลือดสมองเท่านั้นที่มีจำนวนผู้เสียชีวิตมากกว่าในปีนั้น
ยิ่งไปกว่านั้น เชื้อโรคในโรงพยาบาลหลายชนิดอาจไม่ถูกกำจัดออกไปโดยการทำความสะอาดตามปกติ ดังนั้น เชื้อโรคเหล่านี้จึงสามารถอยู่รอดได้เป็นเวลานานในโรงพยาบาล อากาศภายในอาคาร และพื้นผิวต่างๆ และมีส่วนทำให้เกิดการแพร่กระจายของการติดเชื้อ การรักษาทางเลือกเป็นสาขาการวิจัยที่มีแนวโน้มที่ดี ดังนั้นจึงจำเป็นอย่างยิ่งที่จะต้องแสวงหาการรักษาใหม่ๆ สำหรับเชื้อแบคทีเรียดื้อยา และนี่คือพื้นฐานของการวิจัยนี้ นั่นคือการใช้สารจากธรรมชาติเพื่อกำจัดเชื้อแบคทีเรียดื้อยา เช่น MRSA, E. coli, S. aureus, K. pneumoniae, A. baumannii และ P. aeruginosa โดยไม่ก่อให้เกิดการดื้อยาเพิ่มเติม การค้นพบสารต้านแบคทีเรียจากธรรมชาติชนิดใหม่ที่มีกลไกการออกฤทธิ์แบบใหม่ยังคงเป็นสิ่งสำคัญลำดับต้นๆ ในระดับโลก สารต้านจุลชีพจากธรรมชาติได้รับการใช้ในการรักษาแบคทีเรียอย่างประสบความสำเร็จ และเป็นแหล่งยาหลักตลอดประวัติศาสตร์ของมนุษย์ ซึ่งไม่ควรลืม ผลิตภัณฑ์จากธรรมชาติ รวมถึงพืชสมุนไพร ยังคงได้รับความนิยมอย่างแพร่หลายในปัจจุบัน โดยประมาณ 80% ของประชากรโลกพึ่งพาผลิตภัณฑ์สมุนไพรและอาหารเสริมที่เกี่ยวข้องเป็นส่วนหนึ่งของระบบการดูแลสุขภาพ ผลิตภัณฑ์จากธรรมชาติ เช่น Rosmarinus officinalis และ Mangifera indica L., Anacardiaceae เปปไทด์ต้านจุลชีพ น้ำมันหอมระเหยจากพืช และส่วนผสมของสิ่งเหล่านี้ ได้รับการพิสูจน์แล้วว่ามีประสิทธิภาพค่อนข้างดีในการยับยั้งเชื้อแบคทีเรียก่อโรคหลากหลายชนิด รวมถึงแบคทีเรีย AMR ทั้งห้าชนิดในงานวิจัยนี้ งานวิจัยนี้ศึกษาการกำจัด MRSA, Escherichia coli, Klebsiella pneumonia, Acinetobacter baumannii และ Pseudomonas aeruginosa ที่ดื้อต่อยาปฏิชีวนะด้วยแอมพูล CDSpure ที่มี 2,990 ppm ต่อแอมพูล 5 มล. คลอรีนไดออกไซด์ 16 ชนิด ในหลอดทดลอง
ความสำคัญของแบคทีเรียดื้อยาต้านจุลชีพทั้ง 5 ชนิด
อะซิเนโตแบคเตอร์ บาวมันนี (Acinetobacter Baumannii)
Acinetobacter baumannii ประกอบด้วยแบคทีเรียแกรมลบ แอโรบิกอย่างเคร่งครัด ไม่หมัก ไม่ต้องการสารอาหารเฉพาะ ไม่เคลื่อนที่ มีเอนไซม์คะตาเลสเป็นบวก และเอนไซม์ออกซิเดสเป็นลบ แม้ว่า A.baumannii จะคิดเป็นเปอร์เซ็นต์ที่ค่อนข้างต่ำของกรณีติดเชื้อในกระแสเลือดโดยรวม แต่การดื้อยาหลายชนิดเป็นปัญหาทั่วโลกสำหรับสายพันธุ์นี้ ทั่วโลกกว่า 71% ดื้อยาหลายชนิด ในสหรัฐอเมริกา 27% ของผู้ป่วยที่ใช้เครื่องช่วยหายใจมีเชื้อ A. baumannii สายพันธุ์ดื้อยาหลายชนิด A. baumannii ใช้กลยุทธ์การดื้อยา ได้แก่ β-lactamase ในโครโมโซม ปั๊มขับออก และเอนไซม์ดัดแปลงอะมิโนไกลโคไซด์ หลังจากสัมผัสกับอัลบูมินในซีรั่มของมนุษย์ A. A. baumannii ควบคุมการถอดรหัสของ β-lactamases ซึ่งบ่งชี้ถึงกลไกการต้านทานยาต้านจุลชีพโดยธรรมชาติในซีรั่ม เนื่องจากความแพร่หลายของการติดเชื้อและการระบาดที่เกิดจาก A. baumannii ที่ดื้อยาหลายชนิด ยาปฏิชีวนะเพียงไม่กี่ชนิดเท่านั้นที่มีประสิทธิภาพในการรักษาภาวะที่เกิดจากเชื้อก่อโรคนี้ รายงานหลายฉบับแสดงให้เห็นว่า A. baumannii พัฒนาความต้านทานต่อยาต้านจุลชีพอย่างรวดเร็ว และมีการแยกสายพันธุ์ที่ดื้อยาหลายชนิดออกมาได้ องค์การอนามัยโลก (WHO) ยังได้กำหนดให้ A. baumannii เป็นเชื้อก่อโรคที่มีความสำคัญอย่างยิ่ง ซึ่งเป็นภัยคุกคามอย่างมากต่อสุขภาพของมนุษย์ และจำเป็นต้องมีการพัฒนายาปฏิชีวนะใหม่ๆ อย่างเร่งด่วน
เอสเชอริเชีย โคลี (Escherichia coli)
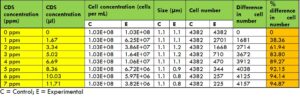
เชื้อ E. coli มักดื้อต่อยาต้านจุลชีพหลายชนิดในสายพันธุ์ที่ก่อให้เกิดการติดเชื้อทางเดินปัสสาวะและภาวะติดเชื้อในกระแสเลือดมากกว่า 50% E. coli เป็นสาเหตุสำคัญของโรคท้องร่วง เยื่อบุช่องท้องอักเสบ ลำไส้ใหญ่อักเสบ ภาวะติดเชื้อในกระแสเลือด อัตราการเสียชีวิตของทารก และการติดเชื้อทางเดินปัสสาวะทั่วโลก ซึ่งมีค่าใช้จ่ายในการรักษาหลายพันล้านดอลลาร์และคร่าชีวิตมนุษย์ประมาณ 2 ล้านคนต่อปี E. coli เป็นแบคทีเรียแกรมลบที่มีความหลากหลาย พบได้ง่าย และสามารถเปลี่ยนแปลงทางพันธุกรรมตามธรรมชาติและแบบสุ่มได้ มีขนาด 1-3 x 0.4-0.7 ไมโครเมตร และปริมาตร 0.6 ถึง 0.7 ไมโครเมตร
เคล็บซิเอลลา นิวโมเนีย (Klebsiella pneumoniae)
เชื้อ K. pneumoniae มักถูกจัดประเภทเป็นเชื้อฉวยโอกาส เชื้อก่อโรครุนแรง (hyKp) หรือเชื้อดื้อยาหลายชนิด (MDR) ในขณะที่ K. pneumoniae แบบคลาสสิก (cKp) ประกอบด้วยเชื้อฉวยโอกาสที่มักเกี่ยวข้องกับการติดเชื้อในโรงพยาบาล เชื้อก่อโรครุนแรงถือเป็นแบคทีเรียที่ได้รับมาจากชุมชนซึ่งสามารถติดเชื้อได้ในคนทุกวัย รวมถึงผู้ที่มีสุขภาพดี การแพร่กระจายอย่างรวดเร็วของเชื้อ K. pneumoniae ที่ดื้อยาหลายชนิดเป็นภัยคุกคามต่อสุขภาพทั่วโลก เนื่องจากเชื้อเหล่านี้เป็นสาเหตุของการติดเชื้อในโรงพยาบาลหลายแห่งที่มีอัตราการป่วยและเสียชีวิตสูง Klebsiella pneumoniae ถูกอธิบายว่าเป็นแบคทีเรียแกรมลบ มีแคปซูล และไม่เคลื่อนที่
เชื้อแบคทีเรีย Staphylococcus Aureus ที่ดื้อต่อเมธิซิลลิน (MRSA)
MRSA ถือเป็นหนึ่งในเชื้อก่อโรคในโรงพยาบาลที่อันตรายที่สุด ก่อให้เกิดการติดเชื้อที่รักษาได้ยากหลายชนิดในโรงพยาบาล และถูกตั้งชื่อว่า MRSA ที่เกี่ยวข้องกับโรงพยาบาล (HA-MRSA)40 ในช่วง 20-25 ปีที่ผ่านมา มีการแยกเชื้อ MRSA ได้จากแหล่งชุมชน ดังนั้นจึงเกิด MRSA ที่เกี่ยวข้องกับชุมชน (CA-MRSA) ขึ้นมา40 MRSA สามารถก่อให้เกิดการติดเชื้อเฉพาะอวัยวะต่างๆ ได้ โดยที่พบมากที่สุดคือผิวหนังและเนื้อเยื่อใต้ผิวหนัง รองลงมาคือการติดเชื้อแบบรุกราน เช่น โรคกระดูกอักเสบ เยื่อหุ้มสมองอักเสบ ปอดอักเสบ ฝีในปอด และหนองในช่องอก การติดเชื้อเยื่อบุหัวใจอักเสบที่เกิดจาก MRSA มีความสัมพันธ์กับอัตราการป่วยและอัตราการเสียชีวิตที่เพิ่มขึ้นเมื่อเทียบกับเชื้อจุลินทรีย์อื่นๆ และเชื่อมโยงกับการใช้ยาเสพติดทางหลอดเลือดดำ41 Staphylococcus aureus ที่ดื้อต่อเมธิซิลลิน (MRSA) เป็นแบคทีเรียแกรมบวกรูปทรงกลมที่มีทั้งเอนไซม์ catalase และ coagulase เป็นบวก42 Pseudomonas aeruginosa P. เชื้อ Streptococcus aeruginosa เป็นหนึ่งในห้าสาเหตุหลักของการติดเชื้อแบคทีเรียในโรงพยาบาล ซึ่งมักนำไปสู่ภาวะติดเชื้อในกระแสเลือดอย่างรุนแรง (sepsis)
P. aeruginosa เป็นแบคทีเรียแกรมลบที่สำคัญซึ่งเป็นเชื้อก่อโรคฉวยโอกาสที่ทำให้เกิดการติดเชื้อเฉียบพลันและเรื้อรังรุนแรงหลายชนิด โดยมีอัตราการป่วยและเสียชีวิตสูงถึง 40% สิ่งที่ทำให้ P. aeruginosa เป็นเชื้อก่อโรคที่ท้าทายอย่างยิ่งคือความต้านทานโดยธรรมชาติและความต้านทานที่ได้รับมาต่อยาปฏิชีวนะที่มีอยู่หลายชนิด เป็นเชื้อก่อโรคฉวยโอกาสในมนุษย์ที่สามารถก่อให้เกิดการติดเชื้อเฉียบพลันและเรื้อรังที่คุกคามชีวิตได้หลายชนิด โดยเฉพาะอย่างยิ่งในผู้ป่วยที่มีระบบภูมิคุ้มกันบกพร่อง มีความสำคัญอย่างยิ่งเนื่องจากเป็นสาเหตุหลักของการป่วยและเสียชีวิตในผู้ป่วยโรคซิสติกไฟบรอยด์ (CF) เป็นหนึ่งในเชื้อก่อโรคในโรงพยาบาลอันดับต้น ๆ ที่ส่งผลกระทบต่อผู้ป่วยที่เข้ารับการรักษาในโรงพยาบาล ในขณะที่มีความต้านทานโดยธรรมชาติต่อยาปฏิชีวนะหลายชนิด
คลอรีนไดออกไซด์ (ClO2) สารต้านจุลชีพ
คลอรีนไดออกไซด์ (ClO2) เป็นก๊าซสีเหลืองถึงเหลืองอมแดงที่สามารถสลายตัวได้อย่างรวดเร็วในอากาศ คลอรีนไดออกไซด์มีน้ำหนักโมเลกุล 67.45 กรัม/โมล และความสามารถในการละลายในน้ำที่ระดับน้ำทะเลคือ 3.01 กรัม/ลิตร (3000 ppm) ที่อุณหภูมิ 25 °C และความดัน 34.5 มม. ปรอท เป็นสารฆ่าเชื้อที่มีประสิทธิภาพที่ความเข้มข้นต่ำเพียง 0.1 ppm และในช่วง pH ที่กว้าง แม้ในน้ำเย็นก็ยังละลายได้มากกว่าคลอรีนถึงสิบเท่า คลอรีนไดออกไซด์มีศักยภาพในการออกซิเดชันต่ำกว่าโอโซนและคลอรีน ค่า pH ที่เหมาะสมอยู่ระหว่าง 6.0 ถึง 10.0 และโดยทั่วไปจะมีประสิทธิภาพในการกำจัดจุลินทรีย์ได้ดีกว่าคลอรีนที่ค่า pH สูงกว่า 8.0 เมื่อทำปฏิกิริยากับน้ำ จะเกิดเป็นไอออนคลอไรต์ ซึ่งเป็นสารเคมีที่มีปฏิกิริยาสูงมาก สามารถฆ่าแบคทีเรียและจุลินทรีย์ในสารละลายใดๆ ก็ได้ คลอรีนไดออกไซด์สามารถฆ่าแบคทีเรีย ไวรัส และ Giardia ได้อย่างรวดเร็ว และมีประสิทธิภาพต่อ Cryptosporidium นอกจากนี้ คลอรีนไดออกไซด์ยังช่วยปรับปรุงรสชาติและกลิ่น ทำลายซัลไฟด์และฟีนอล ควบคุมสาหร่าย และทำให้ไอออนเหล็กและแมงกานีสเป็นกลาง เป็นสารฆ่าเชื้อที่มีประสิทธิภาพที่ความเข้มข้นต่ำเพียง 0.1 ppm และในช่วง pH ที่กว้าง
คลอรีนไดออกไซด์ ฟิล์มชีวภาพ และการดื้อยา
คลอรีนไดออกไซด์เหมาะสมกว่าสำหรับการใช้ในการรักษาโรค เนื่องจากสามารถแทรกซึมและกำจัดไบโอฟิล์มได้ ตามที่ Simpson et al. (1993) กล่าวไว้ คลอรีนไดออกไซด์สามารถกำจัดไบโอฟิล์มได้อย่างรวดเร็วเพราะละลายน้ำได้ดีมาก ต่างจากโอโซน คลอรีนไดออกไซด์จะไม่ทำปฏิกิริยากับพอลิแซ็กคาไรด์นอกเซลล์ของไบโอฟิล์ม ด้วยวิธีนี้ คลอรีนไดออกไซด์จึงสามารถแทรกซึมเข้าไปในไบโอฟิล์มได้อย่างรวดเร็วเพื่อเข้าถึงและฆ่าจุลินทรีย์ที่อาศัยอยู่ภายในฟิล์ม การแทรกซึมเข้าไปในไบโอฟิล์มเพื่อกำจัดจุลินทรีย์เป็นความท้าทายอย่างแท้จริงสำหรับทั้งการแพทย์แผนธรรมชาติและการแพทย์แผนปัจจุบัน
ไบโอฟิล์มเป็นโครงสร้างสามมิติที่เกิดจากเซลล์จุลินทรีย์ที่ยึดเกาะกับพื้นผิวที่มีชีวิตหรือไม่มีชีวิตภายใต้ปัจจัยทางสรีรวิทยาและสิ่งแวดล้อมต่างๆ ที่ยังต้องได้รับการระบุเพิ่มเติม นอกจากนี้ เซลล์เหล่านี้ยังเพิ่มจำนวนอย่างต่อเนื่องและผลิตสารพอลิเมอร์นอกเซลล์ (EPS) ก่อตัวเป็นเมทริกซ์ที่ห่อหุ้มจุลินทรีย์เหล่านี้ไว้ ไบโอฟิล์มเป็นกลุ่มของเซลล์จุลินทรีย์ที่ถูกห่อหุ้มด้วยเมทริกซ์พอลิแซ็กคาไรด์นอกเซลล์ที่ผลิตขึ้นเองบนพื้นผิวที่มีชีวิตหรือไม่มีชีวิต ไบโอฟิล์มแสดงให้เห็นถึงการป้องกันยาปฏิชีวนะ การป้องกันภูมิคุ้มกันของโฮสต์ และสภาวะแวดล้อมที่ไม่เอื้ออำนวยได้ดีกว่าเซลล์ที่ดำรงชีวิตแบบอิสระ มีการประมาณการว่า 65–80% ของการติดเชื้อในมนุษย์เกิดจากแบคทีเรียที่สร้างไบโอฟิล์ม
คาดว่าไบโอฟิล์มมีความต้านทานต่อยาปฏิชีวนะมากกว่าเซลล์ที่ดำรงชีวิตอิสระถึง 1,000 เท่า ปฏิสัมพันธ์ระหว่างเซลล์แบคทีเรียและปัจจัยด้านสิ่งแวดล้อมเป็นตัวกระตุ้นให้เกิดการก่อตัวของไบโอฟิล์ม คลอรีนไดออกไซด์สามารถแทรกซึมและกำจัดไบโอฟิล์มได้ ซึ่งเป็นข้อได้เปรียบที่สำคัญเหนือยาปฏิชีวนะหลายชนิดที่ไม่สามารถทำเช่นนี้ได้
ข้อดีที่สำคัญอีกประการหนึ่งของการใช้คลอรีนไดออกไซด์ในการรักษาเมื่อเทียบกับยาปฏิชีวนะคือ คลอรีนไดออกไซด์ไม่สามารถทำให้แบคทีเรียดื้อยาปฏิชีวนะได้ การมีอยู่ของกรดอะมิโนทั้งสี่ชนิด (ซิสเทอีน เมไทโอนีน ไทโรซีน และทริปโตเฟน) และโดยเฉพาะอย่างยิ่งซิสเทอีนและไทออลทางชีวภาพมีบทบาทสำคัญในระบบสิ่งมีชีวิตทั้งหมด รวมถึงจุลินทรีย์ ดังนั้นจึงไม่มีจุลินทรีย์ใดสามารถพัฒนาความต้านทานต่อคลอรีนไดออกไซด์ได้
คลอรีนไดออกไซด์แทรกซึมเข้าไปในผนังเซลล์ของแบคทีเรียและทำปฏิกิริยากับกรดอะมิโนที่สำคัญในไซโตพลาสซึมของเซลล์เพื่อฆ่าแบคทีเรีย ผลพลอยได้จากปฏิกิริยานี้คือคลอไรต์ ซึ่งยังไม่เป็นที่ทราบแน่ชัดว่าก่อให้เกิดความเสี่ยงต่อสิ่งแวดล้อมหรือสุขภาพของมนุษย์อย่างมีนัยสำคัญ
ความปลอดภัยและประสิทธิภาพของคลอรีนไดออกไซด์
ในปี 1967 สำนักงานคุ้มครองสิ่งแวดล้อมแห่งสหรัฐอเมริกา (US EPA) ได้ขึ้นทะเบียนคลอรีนไดออกไซด์ในรูปของเหลวเป็นครั้งแรกเพื่อใช้เป็นสารฆ่าเชื้อและสารทำความสะอาด คลอรีนไดออกไซด์เป็นสารต้านจุลชีพที่เลือกขนาดได้ ซึ่งสามารถฆ่าจุลินทรีย์ขนาดไมครอนได้อย่างรวดเร็ว แต่ไม่สามารถทำร้ายสิ่งมีชีวิตขนาดใหญ่กว่า เช่น สัตว์หรือมนุษย์ได้ เนื่องจากไม่สามารถแทรกซึมลึกเข้าไปในเนื้อเยื่อที่มีชีวิตได้ คลอรีนไดออกไซด์ไม่สามารถแทรกซึมลึกเข้าไปในเนื้อเยื่อของสิ่งมีชีวิตขนาดใหญ่ได้ และการไหลเวียนของสิ่งมีชีวิตขนาดใหญ่จะให้สารต้านอนุมูลอิสระอย่างต่อเนื่อง ซึ่งให้การป้องกันต่อผลกระทบของสารออกซิแดนต์คลอรีนไดออกไซด์ งานวิจัยอื่น ๆ แสดงให้เห็นว่าคลอรีนไดออกไซด์ ซึ่งเป็นสารออกซิแดนต์ที่แรง สามารถยับยั้งหรือทำลายจุลินทรีย์ได้ที่ความเข้มข้นตั้งแต่ 1 ถึง 100 ppm ทำให้เกิดฤทธิ์ต้านไวรัสที่ทรงพลัง โดยทำให้ไวรัสไม่ทำงานมากกว่าหรือเท่ากับ 99.9% ภายใน 15 วินาทีสำหรับการกระตุ้น Georgiou (2021) ได้แสดงให้เห็นถึงประสิทธิภาพของคลอรีนไดออกไซด์ต่อ MRSA ในหลอดทดลอง สามารถยับยั้งการเจริญเติบโตได้ถึง 99.99% -100% แม้ในความเข้มข้นต่ำ
งานวิจัยที่กำลังดำเนินอยู่ของมูลนิธิวิจัยชีววิทยา Innerlight ได้ศึกษาการใช้คลอรีนไดออกไซด์ในทางคลินิก รวมถึงสปอร์ แบคทีเรีย และไวรัสที่ไม่จำเพาะเจาะจง สำหรับการใช้งานหลายด้านมานานกว่ายี่สิบห้าปีแล้ว มีการใช้คลอรีนไดออกไซด์ในทางคลินิกอย่างกว้างขวางเพื่อต่อต้านไวรัส Epstein-Barr (EBV), ไวรัส cytomegalovirus (CMV); ไวรัสตับอักเสบ A; B; HIV (ไวรัสเอดส์) และอื่นๆ อย่างต่อเนื่อง เมื่อวันที่ 14 ตุลาคม 2020 รัฐสภาโบลิเวียได้ผ่านร่างกฎหมาย (ley 1351) ที่อนุญาตให้ใช้คลอรีนไดออกไซด์เป็นยาต้าน COVID-19 คลอรีนไดออกไซด์ถูกนำมาใช้ประสบความสำเร็จในประเทศต่างๆ เช่น โบลิเวีย เม็กซิโก เปรู บราซิล และโคลอมเบีย ในโบลิเวีย กฎหมายฉบับที่ 1351 ปี 2020 (ราชกิจจานุเบกษาของโบลิเวีย ปี 2020) ได้รับการอนุมัติให้เตรียม จำหน่าย จัดหา และใช้สารละลายคลอรีนไดออกไซด์เพื่อป้องกันและรักษาโรคโควิด-19 เมื่อไม่นานมานี้ ในปี 2021 การศึกษาโดย Insignares-Carrione58 ที่ดำเนินการเพื่อตรวจสอบประสิทธิภาพของคลอรีนไดออกไซด์ชนิดรับประทานในการรักษาโควิด-19 แสดงให้เห็นว่าคลอรีนไดออกไซด์มีประสิทธิภาพในการรักษาโควิด-19
คลอรีนไดออกไซด์มีอะตอม 3 อะตอม นักวิทยาศาสตร์เรียกพันธะนี้ว่าไอออน “ไม่เสถียร” หรือ “ประจุลบ” เมื่อพันธะของอะตอมเหล่านี้แยกออกจากกัน มันจะสร้างพัลส์พลังงานระดับอะตอมย่อยที่เล็กมาก พัลส์นี้เกิดขึ้นเมื่อคลอรีนไดออกไซด์เข้าใกล้เชื้อโรคในร่างกาย มันจะโจมตีเฉพาะจุลินทรีย์ “ที่เป็นกรด” และ “ไม่ใช้ออกซิเจน” (ไวรัส แบคทีเรีย เชื้อรา หรือปรสิต) ในร่างกายเท่านั้น และจะไม่เป็นอันตรายต่อไมโครไบโอม แบคทีเรียเหล่านี้อยู่รอดได้ก็ต่อเมื่อขาดออกซิเจนและรวมถึงสิ่งมีชีวิตที่ก่อโรคหลายชนิด สิ่งมีชีวิตที่ไม่ใช้ออกซิเจนไม่ได้พัฒนาการป้องกันที่เพียงพอต่อการโจมตีของออกซิเจน โดยเฉพาะออกซิเจนที่เกิดขึ้นใหม่ และจะตายอย่างรวดเร็วจากฤทธิ์ที่ร้ายแรงของมัน เซลล์ที่แข็งแรงทั้งหมดที่ต้องการออกซิเจนในการดำรงชีวิตหรือเป็น “ด่าง” จะปลอดภัย
พิษวิทยาของคลอรีนไดออกไซด์
ภาพที่ 1 แสดงระดับอ้างอิงสำหรับการฆ่าเชื้อในน้ำดื่มจากสำนักงานคุ้มครองสิ่งแวดล้อมแห่งสหรัฐอเมริกา (โซนสีฟ้า) ระดับประสิทธิภาพในการรักษาที่อาจเกิดขึ้นในสัตว์ทดลองที่ระดับความเป็นพิษเป็นศูนย์แสดงอยู่ในโซนสีเขียว ระดับที่เป็นพิษแสดงอยู่ในโซนสีแดง (สูงกว่า 399 ppm) ระดับ 5 ppm ที่กำจัดแบคทีเรียดื้อยาปฏิชีวนะได้ 99% หรือมากกว่าในงานวิจัยนี้ อยู่ภายในพื้นที่สีฟ้า/เขียวซึ่งมีความเป็นพิษเป็นศูนย์
ปริมาณคลอรีนไดออกไซด์ที่ใช้ในการศึกษาแบบให้ยาซ้ำหลายครั้ง ในระยะกึ่งเฉียบพลัน (<28 วัน) หรือระยะเรื้อรัง (>90 วัน)
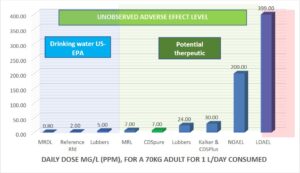
คลอรีนไดออกไซด์ถูกเติมลงในน้ำดื่มเพื่อปกป้องผู้คนจากแบคทีเรียที่เป็นอันตรายและจุลินทรีย์อื่นๆ คนส่วนใหญ่ได้รับคลอรีนไดออกไซด์และคลอไรต์ในปริมาณเล็กน้อยจากการดื่มน้ำที่ผ่านการบำบัดแล้ว รวมถึงอาหาร เนื่องจากมีการใช้เป็นสารฆ่าเชื้อในอุตสาหกรรมอาหาร ไม่มีหลักฐานว่าคลอรีนไดออกไซด์หรือคลอไรต์ส่งผลกระทบต่อการสืบพันธุ์ในมนุษย์ การศึกษาเกี่ยวกับการสืบพันธุ์ในสัตว์เพศผู้ไม่ได้แสดงให้เห็นถึงการเปลี่ยนแปลงในดัชนีการสร้างอสุจิ รูปร่างที่ผิดปกติ หรือการเคลื่อนไหวอย่างสม่ำเสมอ อย่างไรก็ตาม ผลกระทบที่รายงานปรากฏขึ้นในปริมาณที่สูงกว่าผลกระทบด้านพัฒนาการที่ไม่พึงประสงค์ ในทำนองเดียวกัน การเปลี่ยนแปลงในพารามิเตอร์ทางโลหิตวิทยาเกิดขึ้นในปริมาณที่สูงขึ้น ไม่พบข้อมูลเกี่ยวกับการเสียชีวิตในมนุษย์หลังจากการได้รับคลอรีนไดออกไซด์ทางปาก ในการศึกษาโดย Scatina อาสาสมัครคนดื่มคลอรีนไดออกไซด์ในสารละลายที่มีความเข้มข้นสูงถึง 24 ppm และไม่แสดงผลกระทบที่ไม่พึงประสงค์ใดๆ
ระเบียบวิธี
เครื่องมือและวิธีการ
การศึกษาครั้งนี้ใช้แบคทีเรียดื้อยาปฏิชีวนะ 5 ชนิด ได้แก่ E. coli, S. aureus, K. pneumoniae, S. pneumoniae, A. baumannii และ P. aeruginosa แบคทีเรียทั้งหมดได้มาจากห้องปฏิบัติการที่ได้รับการรับรอง (ATTC ประเทศเยอรมนี) บรรจุในหลอดแช่แข็งและเพาะเลี้ยงบนจานวุ้นเลือด นำตัวอย่างแบคทีเรียแต่ละชนิดจากวัฒนธรรมที่แยกได้โดยใช้ลูปที่ผ่านการฆ่าเชื้อแล้วในตู้ความปลอดภัยระดับ II จากจานเพาะเลี้ยง และใส่ลงในหลอดปลอดเชื้อที่มีน้ำซุปทริปติกซอย (TSB) 5 มล. นำหลอดเพาะเลี้ยงเหล่านี้ไปบ่มที่อุณหภูมิ 37 องศาเซลเซียสในตู้บ่มเพาะ Heraeus เมื่อได้จำนวนแบคทีเรียที่เหมาะสมแล้ว จึงนำหลอดไปแช่แข็งและเก็บไว้ในไนโตรเจนเหลวที่อุณหภูมิ -176 องศาเซลเซียสจนกว่าจะใช้งาน
การนับแบคทีเรีย
ในการวัดปริมาณแบคทีเรียในห้องปฏิบัติการ มักจะใช้วิธีนับหน่วยก่อตัวของโคโลนี (colony-forming units) ซึ่งเป็นวิธีที่ง่ายและให้ภาพรวมที่ดีเกี่ยวกับความมีชีวิตของเซลล์ ข้อเสียเปรียบที่สำคัญอย่างหนึ่งคือต้องใช้เวลาหลายวันกว่าจะได้ผลลัพธ์ และผลลัพธ์จะแตกต่างกันไปในแต่ละห้องปฏิบัติการ ขึ้นอยู่กับเทคนิคและสภาวะการเตรียมตัวอย่าง งานวิจัยนี้ได้นับจำนวนแบคทีเรียโดยใช้เครื่องนับเซลล์จุลินทรีย์ QUANTOM Tx™ จาก Logos Biosystems ซึ่งเป็นเครื่องนับเซลล์อัตโนมัติแบบใช้ภาพ ที่สามารถระบุและนับจำนวนแบคทีเรียแต่ละตัวได้ภายในไม่กี่นาที QUANTOM Tx จะโฟกัส จับภาพ และวิเคราะห์ภาพเซลล์ที่ย้อมด้วยสารเรืองแสงหลายภาพโดยอัตโนมัติ เพื่อตรวจจับเซลล์แบคทีเรียด้วยความไวและความแม่นยำสูง ประกอบด้วยอัลกอริทึมการตรวจจับและแยกกลุ่มเซลล์ที่ซับซ้อน ซึ่งสามารถระบุเซลล์แบคทีเรียแต่ละตัวได้อย่างแม่นยำแม้ในกลุ่มเซลล์ที่หนาแน่นที่สุด ในการทดลองเหล่านี้ เราใช้ชุดตรวจเซลล์ที่มีชีวิต (Viable Cell Staining Kit) เพื่อตรวจจับเซลล์ที่มีชีวิตหรือเซลล์ที่ยังมีชีวิตอยู่ เทียบกับเซลล์ที่ตายแล้ว ในการเตรียมตัวอย่างสำหรับเครื่องนับ QUANTOM นั้น เราใช้ปิเปตอิเล็กทรอนิกส์ DLAB ที่สอบเทียบแล้ว ดูดเอาตัวอย่างสารละลายเพาะเลี้ยง 10 ไมโครลิตร (μl) ใส่ลงในหลอด Eppendorf ขนาด 1.5 มิลลิลิตรที่ผ่านการฆ่าเชื้อแล้ว จากนั้นเติมสีย้อมเซลล์ที่มีชีวิต (Viable Cell Staining Dye) 2 μl ลงไป และนำไปบ่มในตู้อบ Heraeus ที่อุณหภูมิ 37 องศาเซลเซียส เป็นเวลา 30 นาที สุดท้าย เราเติมบัฟเฟอร์ 8 μl ลงในตัวอย่างนี้เพื่อเพิ่มความชัดเจนของสัญญาณเรืองแสง
การเตรียมสารละลายคลอรีนไดออกไซด์
ในการเตรียมคลอรีนไดออกไซด์ ได้ใช้หลอดบรรจุคลอรีนไดออกไซด์ขนาด 5 มล. ชื่อ CDS Pure® ซึ่งมีคลอรีนไดออกไซด์ 2,990 ppm (CAS 10049-04-41) ผลิตโดย AQARIUS pro-life สำหรับการทดลอง นี่คือสารละลายคลอรีนไดออกไซด์พร้อมใช้งาน ผ่านการฆ่าเชื้อแล้ว บรรจุในหลอดแก้วปิดผนึก มีความบริสุทธิ์สูง ผ่านการกรองระดับนาโน มีค่า pH เป็นกลาง และปราศจากคลอรีน สารละลายคลอรีนไดออกไซด์ (น้ำปราศจากแร่ธาตุ คลอรีนไดออกไซด์) ไม่มีสารตกค้าง ไอออนเงิน หรืออนุภาคนาโน เนื่องจากแต่ละหลอดขนาด 5 มล. มีคลอรีนไดออกไซด์ 2,900 ppm จึงง่ายต่อการคำนวณปริมาณมิลลิลิตรที่ต้องการ ความเข้มข้นที่ใช้แตกต่างกันไปตั้งแต่ 1 – 7 ppm ของคลอรีนไดออกไซด์ ปริมาณที่ใช้สำหรับแต่ละความเข้มข้นคือ 1 ppm = 1.667 μl CDS Pure®; 2 ppm = 3.344 μl; 3 ppm = 5.016 μl; 4 ppm = 6.688 μl; 5 ppm = 8.336 μl; 6 ppm = 10.032 μl และ 7 ppm = 11.704 μl ระยะเวลาการสัมผัสไม่สำคัญเนื่องจากการฆ่าเชื้อเกิดขึ้นทันทีภายในไม่กี่วินาที เติมคลอรีนไดออกไซด์ในความเข้มข้นต่างๆ ลงในหลอดทดลอง
ความเข้มข้นของคลอรีนไดออกไซด์ที่ใช้ในการทดลองมีตั้งแต่ 1.667 μl (1 ppm) ถึง 11.704 μl (7 ppm) โดยเติมลงในหลอดทดลองด้วยปิเปตอิเล็กทรอนิกส์ DLAB และผสมเบาๆ สำหรับแบคทีเรียแต่ละชนิด เตรียมหลอดควบคุมจากอาหารเลี้ยงเชื้อชนิดเดียวกันสำหรับแต่ละหลอดทดลองด้วย ตามปริมาณคลอรีนไดออกไซด์ที่ใช้ในหลอดทดลอง ปริมาณน้ำกลั่นที่เท่ากันถูกเติมลงในหลอดควบคุมเพื่อรักษาระดับการเจือจางให้คงที่ จากหลอดควบคุมและหลอดทดลองเหล่านี้ ตัวอย่าง 6 ไมโครลิตรถูกดูดด้วยปิเปตอิเล็กทรอนิกส์และวางลงบนสไลด์นับเซลล์ M50 สไลด์ถูกนำไปใส่ในเครื่องปั่นเหวี่ยง QUANTOM เป็นเวลา 8 นาที ที่แรงเหวี่ยงสัมพัทธ์ 300 RCF (Relative Centrifugal Force) จากนั้นจึงนำไปใส่ในเครื่องนับเซลล์จุลินทรีย์ QUANTOM เพื่อวัดค่าพื้นฐาน (ควบคุม) และวัดค่าอีกครั้งจากหลอดทดลอง การตั้งค่าเครื่องนับเซลล์จุลินทรีย์ QUANTOM ที่เหมาะสมที่สุดสำหรับแบคทีเรียชนิดต่างๆ ถูกตั้งค่าตามรูปร่างและขนาดของแบคทีเรียแต่ละชนิดเพื่อเพิ่มประสิทธิภาพในการนับ
ผลลัพธ์
เพื่อประเมินศักยภาพในการฆ่าเชื้อของคลอรีนไดออกไซด์ต่อแบคทีเรียดื้อยาปฏิชีวนะ 5 ชนิดในงานวิจัยนี้ ใช้หลอดบรรจุ CDSpure ขนาด 5 มล. ตลอดการทดลอง เนื่องจากหลอดเหล่านี้มีความเข้มข้นมาตรฐาน 2,990 ppm ความเข้มข้นที่ใช้คือ 1 ppm ถึง 7 ppm โดยเพิ่มขึ้นทีละ 1 ppm ตัวอย่างควบคุมและตัวอย่างทดลองที่ความเข้มข้นต่างๆ ทำซ้ำ 3 ครั้ง แล้วนำค่าเฉลี่ยมาเปรียบเทียบกับตัวอย่างควบคุมที่ไม่มีคลอรีนไดออกไซด์ CDSpure โดยทั่วไปแล้ว ในแบคทีเรียทั้ง 5 ชนิด พบว่ามีการฆ่าเชื้อมากกว่า 95% ที่ความเข้มข้นสูงสุด 7 ppm ของคลอรีนไดออกไซด์ โดยบางชนิดถูกกำจัดได้ที่ความเข้มข้นต่ำกว่า 4–7 ppm (การทดสอบ t-test, p<0.01)
เรามาพิจารณาแบคทีเรียแต่ละชนิดโดยละเอียดในตารางและรูปภาพด้านล่างนี้กัน
การฆ่าเชื้อแบคทีเรีย Acinetobacter baumannii
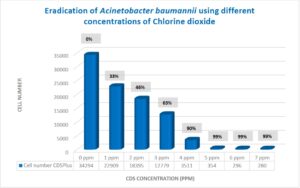
เมื่อใช้ Acinetobacter baumannii พบว่ามีการฆ่าเชื้อได้ 99% ที่ความเข้มข้นของคลอรีนไดออกไซด์ 5, 6 และ 7 ppm (t-test, p<0.01) (ตารางที่ 1, ภาพที่ 2)
ตารางที่ 1: การเปรียบเทียบจำนวนแบคทีเรีย Acinetobacter baumannii ก่อนและหลังการสัมผัสคลอรีนไดออกไซด์
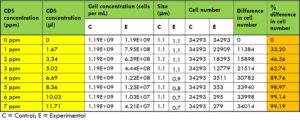
ภาพที่ 2 การเปรียบเทียบกลุ่มควบคุมกับกลุ่มทดลองของเชื้อ Acinetobacter baumannii coli โดยใช้คลอรีนไดออกไซด์ที่ความเข้มข้นต่าง ๆ
การฆ่าเชื้อแบคทีเรีย Escherichia coli
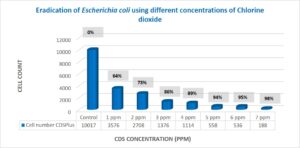
สำหรับเชื้อ E. coli พบว่ามีการฆ่าเชื้อมากกว่า 98% ที่ความเข้มข้นของคลอรีน 7 ppm (t-test, p<0.01) (ตารางที่ 2, ภาพที่ 3)
ตารางที่ 2: การเปรียบเทียบจำนวนแบคทีเรีย Escherichia coli ก่อนและหลังการสัมผัสคลอรีนไดออกไซด์
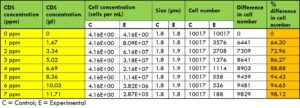
ภาพที่ 3 การเปรียบเทียบกลุ่มควบคุมกับกลุ่มทดลองของแบคทีเรีย Escherichia coli โดยใช้คลอรีนไดออกไซด์ที่ความเข้มข้นต่าง ๆ
การฆ่าเชื้อแบคทีเรีย Klebsiella pneumoniae
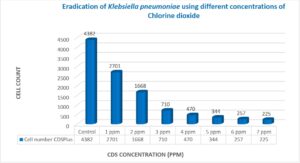
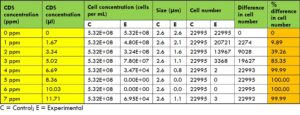
สำหรับแบคทีเรีย K. pneumoniae พบว่ามีการฆ่าเชื้อมากกว่า 94% ที่ความเข้มข้นของคลอรีน 6 และ 7 ppm (การทดสอบ t, p<0.01) (ตารางที่ 3 ภาพที่ 4)
ตารางที่ 3: การเปรียบเทียบจำนวนแบคทีเรีย Klebsiella pneumoniae ก่อนและหลังการสัมผัสคลอรีนไดออกไซด์
ภาพที่ 4 การเปรียบเทียบกลุ่มควบคุมกับกลุ่มทดลองของเชื้อ Klebsiella pneumoniae โดยใช้คลอรีนไดออกไซด์ที่ความเข้มข้นต่าง ๆ
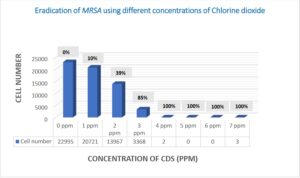
การฆ่าเชื้อแบคทีเรีย Staphylococcus Aureus ที่ดื้อต่อเมธิซิลลิน (MRSA)
สำหรับเชื้อ MRSA พบว่ามีการฆ่าเชื้อมากกว่า 99% ที่ความเข้มข้นของคลอรีน 4-7 ppm (การทดสอบ t, p<0.01) (ตารางที่ 4 ภาพที่ 5)
ตารางที่ 4: การเปรียบเทียบจำนวนแบคทีเรีย MRSA ก่อนและหลังการสัมผัสคลอรีนไดออกไซด์
ภาพที่ 5 การเปรียบเทียบกลุ่มควบคุมกับกลุ่มทดลองของเชื้อ MRSA โดยใช้คลอรีนไดออกไซด์ที่ความเข้มข้นต่าง ๆ
การฆ่าเชื้อแบคทีเรีย Pseudomonas aeruginosa
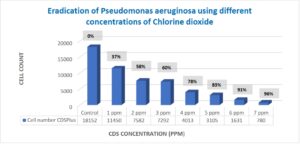
จากการทดสอบกับแบคทีเรีย P. aeruginosa พบว่ามีการฆ่าเชื้อมากกว่า 95% ที่ความเข้มข้นของคลอรีน 7 ppm (t-test, p<0.01) (ตารางที่ 5, ภาพที่ 6) งานวิจัยนี้แสดงให้เห็นว่าสารละลายคลอรีนไดออกไซด์เป็นสารธรรมชาติที่มีประสิทธิภาพในการกำจัดแบคทีเรียดื้อยาปฏิชีวนะทุกชนิดที่ทำการทดสอบ ความเข้มข้นของคลอรีนไดออกไซด์ที่จำเป็นเพื่อให้ได้ผลการฆ่าเชื้อ 95% หรือมากกว่าสำหรับแบคทีเรียดื้อยาปฏิชีวนะทั้ง 5 ชนิดนั้นอยู่ระหว่าง 4-7 ppm ซึ่งอยู่ในขอบเขตที่อาจปลอดภัย (ดูภาพที่ 1)
ภาพที่ 6 การเปรียบเทียบกลุ่มควบคุมกับกลุ่มทดลองของเชื้อ Pseudomonas aeruginosa โดยใช้คลอรีนไดออกไซด์ที่ความเข้มข้นต่าง ๆ
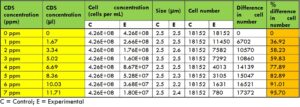
ตารางที่ 5: การเปรียบเทียบจำนวนแบคทีเรีย Pseudomonas aeruginosa ก่อนและหลังการสัมผัสคลอรีนไดออกไซด์
การอภิปราย
การเพิ่มขึ้นของแบคทีเรียดื้อยาปฏิชีวนะเป็นภัยคุกคามที่สำคัญต่อสุขภาพของประชาชนทั่วโลก แบคทีเรียที่ทนทานเหล่านี้ได้พัฒนาความต้านทานต่อยาปฏิชีวนะแบบดั้งเดิม ทำให้การรักษาการติดเชื้อยากขึ้นเรื่อยๆ และนำไปสู่การเพิ่มขึ้นของอัตราการเสียชีวิตและค่าใช้จ่ายด้านการดูแลสุขภาพที่สูงขึ้น มีการคาดการณ์ว่าจำนวนผู้เสียชีวิตประจำปีจากโรคดื้อยาปฏิชีวนะจะเกิน 10 ล้านคนภายในปี 2050 ซึ่งมากกว่าจำนวนผู้เสียชีวิตจากโรคมะเร็ง นี่เป็นภัยคุกคามร้ายแรงต่อสุขภาพทั่วโลก เนื่องจากการติดเชื้อที่เคยจัดการได้อย่างรวดเร็วในปัจจุบันอาจส่งผลให้เกิดอาการป่วยเรื้อรัง นำไปสู่ความทุกข์ทรมานอย่างมากและเป็นภาระต่อระบบการดูแลสุขภาพ ผลกระทบของการวิจัยเกี่ยวกับแนวทางทางเลือกในการกำจัดแบคทีเรียดื้อยาปฏิชีวนะจึงไม่สามารถมองข้ามได้ การวิจัยนี้สามารถช่วยชีวิตผู้คนทั่วโลกได้ด้วยวิธีดังต่อไปนี้:
1. ผลลัพธ์การรักษาผู้ป่วยดีขึ้น: กลยุทธ์ทางเลือกสามารถรักษาการติดเชื้อที่เคยคิดว่ารักษาไม่ได้ได้อย่างมีประสิทธิภาพ โดยการมุ่งเป้าไปที่แบคทีเรียดื้อยาปฏิชีวนะ วิธีการเหล่านี้สามารถปรับปรุงผลลัพธ์การรักษาผู้ป่วย ลดอัตราการเจ็บป่วยและเสียชีวิต และคืนความหวังให้กับผู้ที่ได้รับผลกระทบจากการติดเชื้อดื้อยา
2. ลดภาระด้านการดูแลสุขภาพ: ภาระที่เพิ่มขึ้นของการติดเชื้อที่ดื้อต่อยาปฏิชีวนะกำลังสร้างความตึงเครียดให้กับระบบการดูแลสุขภาพทั่วโลก การค้นหาวิธีการทางเลือกในการต่อสู้กับเชื้อดื้อยาจะช่วยลดภาระต่อทรัพยากรด้านการดูแลสุขภาพ ส่งผลให้ประสิทธิภาพดีขึ้น ระยะเวลาการพักรักษาตัวในโรงพยาบาลลดลง และค่าใช้จ่ายด้านการดูแลสุขภาพลดลง
3. การป้องกันการระบาด: หากไม่ควบคุม แบคทีเรียดื้อยาอาจก่อให้เกิดการระบาดเป็นวงกว้าง การวิจัยเกี่ยวกับแนวทางทางเลือกเปิดโอกาสในการป้องกันการเกิดขึ้นและการแพร่กระจายของสายพันธุ์ดื้อยา ซึ่งท้ายที่สุดแล้วจะเป็นการปกป้องสุขภาพของประชาชนและหลีกเลี่ยงการระบาดใหญ่
4. การเพิ่มทางเลือกในการรักษา: การรักษาแบบใหม่และวิธีธรรมชาติเป็นทางเลือกใหม่ในการต่อสู้กับเชื้อแบคทีเรียดื้อยาปฏิชีวนะ เป็นการขยายขอบเขตของทางเลือกในการรักษาที่มีให้แก่ผู้ให้บริการด้านสุขภาพ ทำให้พวกเขามีเครื่องมือหลายอย่างในการต่อสู้กับการติดเชื้อดื้อยา การเพิ่มทางเลือกนี้จะเพิ่มโอกาสในการรักษาให้ประสบความสำเร็จและช่วยแก้ไขข้อจำกัดของยาปฏิชีวนะแบบดั้งเดิม
5. การเอาชนะกลไกการดื้อยา: แบคทีเรียดื้อยาปฏิชีวนะได้พัฒนากลไกที่ซับซ้อนเพื่อหลีกเลี่ยงผลของยาปฏิชีวนะแบบดั้งเดิม การรักษาแบบใหม่และวิธีธรรมชาติมีศักยภาพในการกำหนดเป้าหมายแบคทีเรียผ่านเส้นทางที่แตกต่างกัน หลีกเลี่ยงหรือเอาชนะกลไกการดื้อยาที่มีอยู่ ทำให้เกิดแนวทางใหม่ในการต่อสู้กับสายพันธุ์ดื้อยา และลดโอกาสในการรักษาล้มเหลว
6. ลดผลข้างเคียงและความเป็นพิษ: ยาปฏิชีวนะแบบดั้งเดิมหลายชนิดมีผลข้างเคียงและอาจเป็นพิษต่อร่างกาย โดยเฉพาะอย่างยิ่งเมื่อใช้เป็นเวลานาน การรักษาแบบธรรมชาติ เช่น คลอรีนไดออกไซด์ อาจมีพิษน้อยกว่าและมีผลข้างเคียงน้อยกว่า สิ่งนี้มีประโยชน์อย่างยิ่งสำหรับกลุ่มประชากรที่เปราะบาง เช่น เด็ก สตรีมีครรภ์ และผู้สูงอายุ ซึ่งอาจมีความอ่อนไหวต่อผลข้างเคียงของยาปฏิชีวนะแบบดั้งเดิมมากกว่า
7. การรักษาสมดุลของจุลินทรีย์ในลำไส้: ยาปฏิชีวนะทั่วไปมักรบกวนสมดุลของแบคทีเรียที่เป็นประโยชน์ในลำไส้ ทำให้เกิดภาวะเสียสมดุลของจุลินทรีย์ในลำไส้ และอาจส่งผลเสียต่อสุขภาพในระยะยาว การรักษาแบบใหม่และแบบธรรมชาติอาจเสนอแนวทางที่มุ่งเป้าไปที่การกำจัดแบคทีเรียที่เป็นอันตรายอย่างเลือกสรร ในขณะเดียวกันก็รักษาความหลากหลายและหน้าที่ของจุลินทรีย์ในลำไส้ การรักษาสมดุลนี้มีความสำคัญอย่างยิ่ง เนื่องจากจุลินทรีย์ในลำไส้ที่แข็งแรงมีบทบาทสำคัญต่อการทำงานของระบบภูมิคุ้มกัน การย่อยอาหาร และสุขภาพโดยรวม
8. แนวทางแก้ไขที่ยั่งยืนและเป็นมิตรต่อสิ่งแวดล้อม: การผลิตและการใช้ยาปฏิชีวนะแบบดั้งเดิมอาจส่งผลเสียต่อสิ่งแวดล้อม รวมถึงการเกิดเชื้อแบคทีเรียดื้อยาในสิ่งแวดล้อม การรักษาด้วยวิธีธรรมชาติมักมาจากแหล่งทรัพยากรหมุนเวียน เช่น พืชหรือสารประกอบที่ได้จากจุลินทรีย์ ซึ่งสามารถผลิตได้อย่างยั่งยืน นอกจากนี้ การรักษาเหล่านี้อาจมีผลกระทบต่อสิ่งแวดล้อมน้อยที่สุด เนื่องจากมักสลายตัวได้ง่ายกว่า ลดความเสี่ยงต่อความเสียหายทางนิเวศวิทยาในระยะยาว
9. ศักยภาพในการรักษาแบบผสมผสาน: การรักษาด้วยวิธีธรรมชาติสามารถผสมผสานกับยาปฏิชีวนะแบบดั้งเดิมหรือการรักษาทางเลือกอื่นๆ เพื่อสร้างผลลัพธ์ที่เสริมฤทธิ์กันและเพิ่มประสิทธิภาพการรักษา แนวทางนี้ช่วยให้สามารถกำหนดแผนการรักษาเฉพาะบุคคลและปรับให้เหมาะสมที่สุด เพิ่มประสิทธิภาพของประโยชน์ที่อาจได้รับจากการรักษาแต่ละวิธี การรักษาแบบผสมผสานอาจมีประสิทธิภาพมากขึ้นในการต่อสู้กับแบคทีเรียดื้อยา ลดระยะเวลาการรักษา และป้องกันการพัฒนาการดื้อยาต่อไป
10. ตัวเลือกการรักษาที่เข้าถึงได้และราคาไม่แพง: การเข้าถึงยาปฏิชีวนะแบบดั้งเดิมอาจมีจำกัดหรือมีราคาสูงเกินไปในหลายส่วนของโลก การรักษาด้วยวิธีธรรมชาติที่ได้จากทรัพยากรที่มีอยู่ในท้องถิ่นอาจเป็นทางเลือกที่เข้าถึงได้และราคาไม่แพงกว่าสำหรับการรักษาการติดเชื้อดื้อยา สิ่งนี้อาจส่งผลกระทบอย่างมากต่อสุขภาพทั่วโลก โดยเฉพาะอย่างยิ่งในประเทศที่มีทรัพยากรจำกัด ซึ่งมีภาระของเชื้อแบคทีเรียดื้อยาปฏิชีวนะสูง
ในการค้นหาทางเลือกที่มีประสิทธิภาพ คลอรีนไดออกไซด์ได้กลายเป็นทางเลือกที่น่าสนใจในการกำจัดแบคทีเรียดื้อยาปฏิชีวนะ โดยออกฤทธิ์ทำลายโครงสร้างเซลล์ของแบคทีเรีย ป้องกันไม่ให้แบคทีเรียเพิ่มจำนวนและก่อให้เกิดอันตรายต่อไป
ข้อดีของคลอรีนไดออกไซด์
คลอรีนไดออกไซด์ได้กลายเป็นอาวุธที่มีศักยภาพในการต่อสู้กับเชื้อโรคที่ดื้อยาเหล่านี้ ด้วยคุณสมบัติในการออกฤทธิ์ครอบคลุมวงกว้าง มีประสิทธิภาพคงอยู่ยาวนาน ลดโอกาสการดื้อยา และปลอดภัยต่อสิ่งแวดล้อม ทำให้มันเป็นเครื่องมือที่มีค่าอย่างยิ่งในการกำจัดแบคทีเรียดื้อยาปฏิชีวนะ การนำคลอรีนไดออกไซด์มาใช้เป็นส่วนหนึ่งของกลยุทธ์การควบคุมการติดเชื้อแบบครบวงจร จะช่วยลดอัตราการเสียชีวิตที่เกี่ยวข้องกับการติดเชื้อเหล่านี้ได้อย่างมีนัยสำคัญ ปกป้องสุขภาพของประชาชน และแก้ไขปัญหาการดื้อยาปฏิชีวนะที่กำลังเพิ่มขึ้น
การใช้คลอรีนไดออกไซด์ในการรักษาจุลินทรีย์ดื้อยาปฏิชีวนะมีข้อดีหลายประการ เช่น ประสิทธิภาพในการออกฤทธิ์: คลอรีนไดออกไซด์แสดงให้เห็นถึงประสิทธิภาพในการต่อต้านแบคทีเรียหลายชนิด รวมถึง MRSA และสายพันธุ์ดื้อยาปฏิชีวนะอื่นๆ ความสามารถในการโจมตีผนังเซลล์ของแบคทีเรียและขัดขวางกระบวนการเผาผลาญที่จำเป็น ทำให้คลอรีนไดออกไซด์เป็นสารต้านจุลชีพที่มีประสิทธิภาพ
ประสิทธิภาพคงอยู่: แตกต่างจากน้ำยาฆ่าเชื้อแบบดั้งเดิม คลอรีนไดออกไซด์มีฤทธิ์คงอยู่ ซึ่งช่วยปกป้องพื้นผิวได้แม้หลังจากการใช้งานครั้งแรก ฤทธิ์คงอยู่นี้มีความสำคัญอย่างยิ่งในสถานพยาบาลที่พื้นผิวอาจปนเปื้อนได้อย่างรวดเร็ว โดยเป็นเกราะป้องกันที่ทรงประสิทธิภาพต่อการเจริญเติบโตและการแพร่กระจายของแบคทีเรีย
ลดโอกาสการเกิดการดื้อยา: กลไกการออกฤทธิ์ของคลอรีนไดออกไซด์ช่วยลดโอกาสที่แบคทีเรียจะดื้อยา ต่างจากยาปฏิชีวนะแบบดั้งเดิมที่มุ่งเป้าไปที่ส่วนประกอบเฉพาะของแบคทีเรีย คลอรีนไดออกไซด์จะโจมตีโครงสร้างเซลล์หลายส่วนพร้อมกัน ทำให้แบคทีเรียพัฒนาความต้านทานได้ยากขึ้น การกำจัดไบโอฟิล์ม: งานวิจัยแสดงให้เห็นว่าคลอรีนไดออกไซด์สามารถแทรกซึมและกำจัดไบโอฟิล์มได้ คาดว่าไบโอฟิล์มมีความต้านทานต่อยาปฏิชีวนะมากกว่าเซลล์อิสระถึง 1,000 เท่า ความปลอดภัยต่อสิ่งแวดล้อม: คลอรีนไดออกไซด์ได้รับการยอมรับว่ามีคุณสมบัติที่เป็นมิตรต่อสิ่งแวดล้อม มันสลายตัวเป็นผลพลอยได้ที่ไม่เป็นอันตราย โดยไม่ทิ้งสารตกค้างที่เป็นพิษ คุณลักษณะนี้ทำให้มั่นใจได้ว่าการใช้เพื่อวัตถุประสงค์ในการฆ่าเชื้อจะไม่ก่อให้เกิดความเสียหายต่อสิ่งแวดล้อมในระยะยาว
ผลกระทบที่อาจเกิดขึ้น: ความสำคัญของคลอรีนไดออกไซด์ในการกำจัดแบคทีเรียดื้อยาปฏิชีวนะนั้นไม่อาจมองข้ามได้ การเป็นทางเลือกในการรักษา คลอรีนไดออกไซด์สามารถช่วยต่อสู้กับปัญหาการดื้อยาปฏิชีวนะที่เพิ่มขึ้น ลดอัตราการเสียชีวิต และบรรเทาภาระของระบบสาธารณสุข ประสิทธิภาพของมันในการต่อต้านเชื้อ MRSA และสายพันธุ์ดื้อยาอื่นๆ สามารถปรับปรุงผลลัพธ์ของผู้ป่วย ลดระยะเวลาการพักรักษาตัวในโรงพยาบาล และลดค่าใช้จ่ายด้านการดูแลสุขภาพ ความคุ้มค่า: สารละลายคลอรีนไดออกไซด์มีราคาถูกและสามารถลดค่าใช้จ่ายด้านการดูแลสุขภาพของประเทศได้อย่างมีนัยสำคัญในระยะยาว
บทสรุป
งานวิจัยนี้มุ่งเน้นศึกษาประสิทธิภาพของคลอรีนไดออกไซด์ในหลอดทดลองต่อแบคทีเรียดื้อยาปฏิชีวนะที่สำคัญที่สุดบางชนิด ซึ่งเป็นสาเหตุของการเสียชีวิตหลายล้านคนต่อปีทั่วโลก เราได้แสดงให้เห็นว่าความเข้มข้นของคลอรีนไดออกไซด์ที่เหมาะสมที่สุดซึ่งส่งผลให้เกิดการฆ่าเชื้อเกือบสมบูรณ์ในหลอดทดลองคือ 7 ppm (p<0.01) นี่เป็นปริมาณที่ปลอดภัยเนื่องจากเป็นปริมาณใกล้เคียงกับที่ใช้ในการบำบัดน้ำ สิ่งที่สังเกตได้ในหลอดทดลองน่าจะพบได้ในร่างกายมนุษย์เช่นกัน เช่นเดียวกับเลือด คลอรีนไดออกไซด์จะปล่อยออกซิเจนเมื่อพบกับความเป็นกรด ไม่ว่าจะเป็นจากกรดแลคติกหรือความเป็นกรดของจุลินทรีย์ เมื่อคลอรีนไดออกไซด์แตกตัว มันจะปล่อยออกซิเจนเข้าสู่กระแสเลือด เช่นเดียวกับเม็ดเลือดแดง โดยใช้หลักการเดียวกัน (ที่รู้จักกันในชื่อปรากฏการณ์โบห์ร) ซึ่งก็คือการเลือกตอบสนองต่อความเป็นกรด
คลอรีนไดออกไซด์เป็นสารต้านจุลชีพที่เลือกขนาดได้ ซึ่งสามารถฆ่าจุลินทรีย์ขนาดไมครอนได้อย่างรวดเร็ว แต่ไม่สามารถก่อให้เกิดอันตรายต่อสิ่งมีชีวิตขนาดใหญ่กว่า เช่น สัตว์หรือมนุษย์ได้ เนื่องจากไม่สามารถแทรกซึมลึกเข้าไปในเนื้อเยื่อที่มีชีวิตได้ มีข้อถกเถียงมากมายเกี่ยวกับการใช้คลอรีนไดออกไซด์ อย่างไรก็ตาม ต้องคำนึงถึงว่า เช่นเดียวกับยาหรืออาหารเสริมใดๆ ผลกระทบจากการสัมผัสสารใดๆ ขึ้นอยู่กับวิธีการใช้ (เช่น การสูดดม การทา หรือการรับประทาน) สถานะของโมเลกุล (เช่น ก๊าซ หรือสารละลาย) ความเข้มข้นของปริมาณ ระยะเวลาการสัมผัส ลักษณะส่วนบุคคลและนิสัย และว่ามีสารเคมีหรือสิ่งเจือปนอื่นๆ อยู่หรือไม่
เน้นย้ำว่ามีการศึกษาทางพิษวิทยามากมายเกี่ยวกับคลอรีนไดออกไซด์ในมนุษย์และสัตว์ตลอดหลายปีที่ผ่านมา ซึ่งแสดงให้เห็นถึงความปลอดภัยและประสิทธิภาพ เนื่องจากมีการนำไปใช้ในหลายด้านเพื่อให้แน่ใจว่ามนุษย์ได้รับสารในระดับที่ปลอดภัย เมื่อใช้ในปริมาณต่ำที่จำเป็นต่อการทำลายจุลินทรีย์อย่างเหมาะสม คลอรีนไดออกไซด์ได้รับการพิสูจน์แล้วว่าปลอดภัย มีผลลัพธ์ที่ดีในการทดลองทางคลินิกเมื่อเร็วๆ นี้เกี่ยวกับคลอรีนไดออกไซด์ที่ดำเนินการกับ COVID-19 โดย Insignares-Carrione ในปี 2021 โดยให้คลอรีนไดออกไซด์ CDS บริสุทธิ์พิเศษ (2,990 ppm) ทางหลอดเลือดดำแก่ผู้ป่วย นอกจากนี้ การอนุมัติจากรัฐบาลเกี่ยวกับการใช้สารละลายคลอรีนไดออกไซด์เพื่อป้องกันและรักษาการระบาดของโรคโควิด-19 ในโบลิเวียได้กลายเป็นกฎหมายในปี 2020 โดยที่คณะกรรมการด้านจริยธรรมได้รับการจัดตั้งขึ้นอย่างถูกต้องตามกฎหมายและได้รับการรับรองจากกระทรวงสาธารณสุขของโบลิเวีย ซึ่งดำเนินการวิจัยเกี่ยวกับคลอรีนไดออกไซด์เพื่อใช้ในแอปพลิเคชันต่างๆ ผ่านคณะกรรมการวิจัยทางคลินิก วิทยาศาสตร์ และจริยธรรมของกระทรวง
นอกจากนี้ ยังมีการนำคลอรีนไดออกไซด์ไปใช้ในทางคลินิกอย่างกว้างขวางเพื่อต่อต้านไวรัส Epstein-Barr (EBV), ไวรัส cytomegalovirus (CMV), ไวรัสตับอักเสบ A, B, HIV (ไวรัสเอดส์) และอื่นๆ อย่างต่อเนื่อง มีการวิจัยเพิ่มเติมเกี่ยวกับการใช้คลอรีนไดออกไซด์ในทางคลินิก รวมถึงสปอร์ แบคทีเรีย และไวรัสที่ไม่จำเพาะเจาะจงมาหลายปีแล้ว นอกจากนี้ยังมีคำบอกเล่าจากอาสาสมัครอีกหลายร้อยรายเกี่ยวกับการใช้คลอรีนไดออกไซด์ในด้านต่างๆ ที่ Jim Humble ได้รวบรวมไว้ตลอดหลายปีที่ผ่านมาจำเป็นต้องมีการทดลองทางคลินิกเพื่อเก็บเกี่ยวประสบการณ์ทางคลินิกเกี่ยวกับสิ่งที่ได้ผลดีที่สุดในการปฏิบัติทางคลินิก แพทย์ที่ใช้การให้ยาทางหลอดเลือดดำสามารถใช้หลอด CDSpure ขนาด 5 มล. (2,990 ppm) โดยตรงหรือรับประทานเมื่อเจือจางให้ได้ระดับที่ต้องการ
ความขัดแย้งทางผลประโยชน์: ไม่มี
คำชี้แจงเกี่ยวกับการสนับสนุนทางการเงิน: ไม่มี
เอกสารอ้างอิง
1. กลุ่มธนาคารโลก. การติดเชื้อดื้อยา: ภัยคุกคามต่ออนาคตทางเศรษฐกิจของเรา. วอชิงตัน: ธนาคารระหว่างประเทศเพื่อการบูรณะและการพัฒนา/ธนาคารโลก. 2017. สืบค้นเมื่อจาก https://documents1.worldbank.org/curated/en/323311493396993758/pdf/final-report.pdf
2. สหประชาชาติ. เป้าหมายการพัฒนาที่ยั่งยืน (เข้าถึง 2023). สืบค้นเมื่อจาก สหประชาชาติ: https://www.un.org/sustainabledevelopment/sustainable-development-goals/
3. Sharma P และ Towse A. ยาใหม่เพื่อรับมือกับเชื้อดื้อยา: การวิเคราะห์ทางเลือกนโยบายของสหภาพยุโรป (25 สิงหาคม 2558). สืบค้นเมื่อจาก SSRN: https://papers.ssrn.com/sol3/papers.cfm?abstract_id=2640028
4. ผู้ร่วมงานด้านการต่อต้านเชื้อดื้อยา. ภาระทั่วโลกของเชื้อดื้อยาแบคทีเรียในปี 2019. Lancet. 2022;399, 629-655.
5. Gatadi S, Gour J และ Nandu S. สารตั้งต้นยาต้านเชื้อ MRSA ที่มีศักยภาพจากผลิตภัณฑ์ธรรมชาติ: บทวิจารณ์. Bioorganic & Medicinal Chemistry. 2019;27(17), 3760-3774.
6.Sharma P, & Towse A. ยาใหม่เพื่อรับมือกับการดื้อยาต้านจุลชีพ: การวิเคราะห์ตัวเลือกนโยบายของสหภาพยุโรป 25 สิงหาคม 2558 สืบค้นจาก SSRN: https://papers.ssrn.com/sol3/papers.cfm?abstract_id=2640028
7.Ventola CL. วิกฤตการดื้อยาปฏิชีวนะ: ตอนที่ 1: สาเหตุและภัยคุกคาม เภสัชกรรมและการบำบัด 2015;40(4), 277–283.
8.Lobanovska M, & Pilla G. การค้นพบเพนิซิลลินและการดื้อยาปฏิชีวนะ: บทเรียนสำหรับอนาคต? วารสารชีววิทยาและการแพทย์ของเยล 2017;90(1), 135–145.
9.Langdon A, Crook N, & Dantas G. ผลกระทบของยาปฏิชีวนะต่อไมโครไบโอมตลอดช่วงพัฒนาการและแนวทางทางเลือกสำหรับการปรับเปลี่ยนการรักษา Genome Medicine, 2016;8, 39.
10.GBD 2019 Diseases and Injuries Collaborators. ภาระโรคและการบาดเจ็บ 369 ชนิดทั่วโลกใน 204 ประเทศและดินแดน ระหว่างปี 1990-2019: การวิเคราะห์อย่างเป็นระบบสำหรับการศึกษาภาระโรคทั่วโลกปี 2019 Lancet. 2020;17(396(10258):), 1204–1222.
11.Kramer, A., Schwebke, I., & Kampf, G. เชื้อโรคในโรงพยาบาลคงอยู่บนพื้นผิวที่ไม่มีชีวิตนานแค่ไหน? การทบทวนอย่างเป็นระบบ MC Infectious Diseases. 2006;16(6), 130.
12.Khin M, Knowles SL, Crandall WJ, Jones Jr, DD, Oberlies NH, Cech NB., & Houriet J. Capturing the Antimicrobial Profile of Rosmarinus officinalis against Methicillin-resistant Staphylococcus aureus (MRSA) with Bioassay-guided Fractionation and Bioinformatics. Journal of Pharmaceutical & Biomedical Analysis, 2021;197, 113965.
13.Bodeker G, Ong CK, Grundy CK, Burford G, & Shein K. WHO global atlas of traditional, complementary and alternative medicine.Kobe, Japan: World Health Organization.2005.
14.Bshabshe AA, Joseph MR, Awad El-Gied AA, Fadul AN, Chandramoorthy HC, & Hamid ME. ความเกี่ยวข้องทางคลินิกและโปรไฟล์ต้านจุลชีพของเชื้อ Staphylococcus aureus ที่ดื้อต่อเมธิซิลลิน (MRSA) ต่อยาปฏิชีวนะทั่วไปและสารสกัดเอทานอลจากเมล็ดมะม่วง (Mangifera indica L.) Biomed Research International, 2020, 4150678.
15.ZouhirA, JridiT, Nefz A, Hamida JB, Sebei K, NefziA, Hamida JB, Sebei K. การยับยั้งเชื้อ Staphylococcus aureus ที่ดื้อต่อเมธิซิลลิน (MRSA) โดยเปปไทด์ต้านจุลชีพ (AMPs) และน้ำมันหอมระเหยจากพืช Pharmaceutical Biology. Volume 54, 2016; ฉบับที่ 12.https://doi.org/10.1080/13880209.2016.1190763
16.CDSpure-https://aquarius-prolife.com/en/maltesian-mineral-solution/104-cdspure-6x5ml-ampoules
17.สำนักงานคุ้มครองสิ่งแวดล้อมแห่งสหรัฐอเมริกา การตัดสินใจเกี่ยวกับคุณสมบัติในการขึ้นทะเบียนใหม่ (RED) สำหรับคลอรีนไดออกไซด์และโซเดียมคลอไรต์ (กรณีที่ 4023) สำนักงานคุ้มครองสิ่งแวดล้อมแห่งสหรัฐอเมริกา สำนักงานป้องกัน สารกำจัดศัตรูพืช และสารพิษ วอชิงตัน: รายงานทางเทคนิคหมายเลข EPA/738/R-06/007 สิงหาคม 2549 สืบค้นจากสำนักงานคุ้มครองสิ่งแวดล้อมแห่งสหรัฐอเมริกา: https://www3.epa.gov/pesticides/chem_search/reg_actions/reregistration/red_PC-020503_3-Aug-06.pdf
18. Clordisys. อุปกรณ์และบริการกำจัดสิ่งปนเปื้อนและฆ่าเชื้อ 2557 สืบค้นจาก clordisys: https://www.clordisys.com/
19. Jin RY, Hu SQ, & Chi ZC. ผลของการบำบัดด้วยก๊าซคลอรีนไดออกไซด์ต่อการฆ่าเชื้อที่ผิวองุ่น วารสาร Advanced Materials Research. 2011;236, 2939–2944.
20. Park SH, & Kang DH. การบำบัดแบบผสมผสานของก๊าซคลอรีนไดออกไซด์และสารฆ่าเชื้อแบบละอองลอยเพื่อยับยั้งเชื้อก่อโรคในอาหารบนใบผักโขมและมะเขือเทศ วารสาร International Journal of Food Microbiology. 2015;207, 103–108.
21. Kalay TS, Kara Y, Karaoglu SA, & Kolaylı S. การประเมินคลอรีนไดออกไซด์ที่เสถียรในแง่ของฤทธิ์ต้านจุลชีพและความแข็งแรงของพันธะเดนติน วารสาร Combinatorial Chemistry & High Throughput Screening. 2022;25(9), 1427 -1436.
22. Peleg AY, Seifert H, & Paterson DL. Acinetobacter baumannii: การเกิดขึ้นของเชื้อก่อโรคที่ประสบความสำเร็จ วารสารจุลชีววิทยาคลินิก 2008;21, 538–582.
23.Lin MF, & Lan CY. (2014). การดื้อยาต้านจุลชีพใน Acinetobacter baumannii: จากห้องปฏิบัติการสู่ข้างเตียงผู้ป่วย วารสารกรณีศึกษาทางคลินิกโลก 2014;2, 787–814.
24.De Oliveira DM, Forde BM, Kidd TJ, Harris PN, Schembri MA, Beatson SA,Walker MJ. การดื้อยาต้านจุลชีพในเชื้อก่อโรค ESKAPE Clinical Microbiology Review, 33(3), e00181-19.Diekema , D. J., Hsueh , P. R., Mendes , R. E., Pfaller , M. A., Rolston , K. V., Sader , H. S., & Jones, R. N. (2019). จุลชีววิทยาของการติดเชื้อในกระแสเลือด: แนวโน้ม 20 ปีจากโครงการเฝ้าระวังยาต้านจุลชีพ SENTRY Antimicrobial Agents and Chemotherapy, 2020;63(7), e00355-19.
25.Diekema DJ, Hsueh PR, Mendes RE, Pfaller MA, Rolston KV, Sader HS, & Jones RN. จุลชีววิทยาของการติดเชื้อในกระแสเลือด: แนวโน้ม 20 ปีจากโครงการเฝ้าระวังยาต้านจุลชีพ SENTRY Antimicrobial Agents and Chemotherapy, 2019;63(7), e00355-19.
26.Thom KA, Maragakis LL, Richards K, Johnson JK, Roup B, Lawson P. Maryland MDRO Prevention Collaborative. Assessing the burden of Acinetobacter baumannii in Maryland: a statewide cross-sectional period prevalence survey. Infection Control & Hospital Epidemiology, 2012;33(9), 883-888.
27.Quinn B, Rodman N, Jara E, Fernandez JS, Martinez J, Traglia GM. Ramírez MS. Human serum albumin alters specific genes that can play a role in survival and persistence in Acinetobacter baumannii. Scientific Reports. 2018;8, 14741.
28.Lee CR, Lee JH, Park M, Park KS, Bae IK, Kim YB, Lee SH. ชีววิทยาของ Acinetobacter baumannii: พยาธิกำเนิด กลไกการดื้อยาปฏิชีวนะ และทางเลือกการรักษาในอนาคต Frontiers in Cellular and Infection Microbiology. 2017;7, 55.
29. McConnell MJ, Actis L, & Pachón J. Acinetobacter baumannii: การติดเชื้อในมนุษย์ ปัจจัยที่ก่อให้เกิดพยาธิสภาพ และแบบจำลองสัตว์ FEMS Microbiology Reviews, 2013;37(2), 130–155.
30. องค์การอนามัยโลก WHO เผยแพร่รายชื่อแบคทีเรียที่ต้องการยาปฏิชีวนะใหม่โดยเร่งด่วน 27 กุมภาพันธ์ 2017 สืบค้นจากองค์การอนามัยโลก: https://www.who.int/news/item/27-02-2017-who-publishes-list-of-bacteria-for-which-new-antibiotics-are-urgently-needed
31. Rangel K, Chagas TP, & De-Simone SG. การติดเชื้อ Acinetobacter baumannii ในช่วงเวลาของการระบาดใหญ่ของ COVID-19 เชื้อโรค, 2021;10(8), 1006.
32.Alhashash F, Weston V, & Diggle M. การติดเชื้อแบคทีเรีย Escherichia coli ที่ดื้อยาหลายชนิด Emerging Infectious Diseases, 2013;19(10), 1699–1701.
33.Kaper JB, Nataro JP., & Mobley HL. Escherichia coli ที่ก่อโรค Nature Reviews Microbiology. 2004;2, 123-140.
34.Santos Braz V, Melchior K, & Moreira CG. Escherichia coli เป็นแบคทีเรียที่ก่อโรคและมีความสามารถหลากหลาย Frontiers in Cellular and Infection Microbiology. 2020;10, 548492.
35.Aryal S. E. Coli (Escherichia Coli)-ภาพรวม. 2020;23 ธันวาคม. สืบค้นเมื่อจาก microbe notes:https://microbenotes.com/escherichia-coli-e-coli/#habitat-of-e-coli
36.Wang G, Zhao G, Chao X, Xie L, & Wang H. ลักษณะเฉพาะของความรุนแรง ไบโอฟิล์ม และการดื้อยาปฏิชีวนะของ Klebsiella Pneumoniae. วารสารวิจัยสิ่งแวดล้อมและสาธารณสุขระหว่างประเทศ. 2020;17(17), 1-17.
37.Chew KL, Lin RT, & Teo JW. Klebsiella Pneumoniae ในสิงคโปร์: การติดเชื้อที่มีความรุนแรงสูงและภัยคุกคามจากคาร์บาเพเนมเมส. Frontiers in Cellular and Infection Microbiology. 2017;7, 515.
38.รุสโซ TA และมาร์ CM. Klebsiella Pneumoniae ที่มีไวรัสรุนแรง บทวิจารณ์จุลชีววิทยาคลินิก. 2019;32(3), 1–4.
39.Ashurst JV และ Dawson A. Klebsiella Pneumonia.Treasure Island: สำนักพิมพ์ StatPearls, 2022
40.Jaradat ZW, Ababneh QO, Sha’aban ST, Alkofahi AA, Assaleh D, & Al Shara A.Methicillin-Resistant Staphylococcus aureus และ fomites สาธารณะ: บทวิจารณ์ เชื้อโรคและสุขภาพโลก 2020;114(8), 426–450.
41.ซิดดิกี อา. & Koirala J. Methicillin-Resistant Staphylococcus Aureus. 2022. สืบค้นเมื่อจาก StatPearls: https://www.ncbi.nlm.nih.gov/books/NBK482221/
42.Belleza M. Methicillin-Resistant Staphylococcus Aureus (MRSA). 2021. สืบค้นเมื่อจาก Nurseslabs: https://nurseslabs.com/methicillin-resistant-staphylococcus-aureus-mrsa/
43.Alhazmi A. Pseudomonas aeruginosa – การเกิดโรคและกลไกการก่อโรค วารสารชีววิทยานานาชาติ 2015;7(2), 44-67.
44.Wood SJ, Kuzel TM, & Shafikhani SH. Pseudomonas aeruginosa: การติดเชื้อ การสร้างแบบจำลองสัตว์ และการบำบัดรักษา เซลล์ 2023;12(1), 199.
45.Moradali MF, Ghods S, & Rehm BH. วิถีชีวิตของ Pseudomonas aeruginosa: แบบจำลองสำหรับการปรับตัว การอยู่รอด และความคงอยู่ แนวหน้าในจุลชีววิทยาของเซลล์และการติดเชื้อ 2017;7, 39.
46.Gale MJ, Maritato MS, Chen Y, & Abdulateef S. Pseudomonas aeruginosa ก่อให้เกิดก้อนอักเสบในโพรงจมูกในผู้ป่วยติดเชื้อ HIV ที่มีภูมิคุ้มกันบกพร่อง: เลียนแบบมะเร็ง 2015;2, 40-43.
47.Gomila A, Carratalà J, Badia JM, Camprubí D, Piriz M, Shaw E,Biondo S. การให้ยาปฏิชีวนะทางปากก่อนผ่าตัดช่วยลดการติดเชื้อ Pseudomonas aeruginosa ที่แผลผ่าตัดหลังการผ่าตัดลำไส้ใหญ่และทวารหนักแบบเลือก BMC Infectious Diseases, 2018;18, 507.
48.หน่วยงานด้านสารพิษและทะเบียนโรค ข้อมูลพิษวิทยาของคลอรีนไดออกไซด์และคลอไรต์ พ.ศ. 2547 สืบค้นจากหน่วยงานด้านสารพิษและโรค: https://www.atsdr.cdc.gov/toxprofiles/tp160.pdf
49. หน่วยงานด้านสารพิษและโรค คำถามที่พบบ่อยเกี่ยวกับสารพิษ (ToxFAQs™) สำหรับคลอรีนไดออกไซด์และคลอไรต์ กันยายน พ.ศ. 2547 สืบค้นจากหน่วยงานด้านสารพิษและโรค: https://www.atsdr.cdc.gov/toxfaqs/tfacts160.pdf
50. องค์การอนามัยโลก คลอรีนไดออกไซด์ คลอไรต์ และคลอเรตในน้ำดื่ม: เอกสารประกอบการพัฒนาแนวทางปฏิบัติขององค์การอนามัยโลกเกี่ยวกับคุณภาพน้ำดื่ม พ.ศ. 2559 เจนีวา: องค์การอนามัยโลก
51. Bajpai P. การควบคุมปัญหาทางจุลชีววิทยา อุตสาหกรรมเยื่อและกระดาษ พ.ศ. 2558;103-195.
52. Pratima B. การควบคุมปัญหาทางจุลชีววิทยา Elsevier Public Health Emergency Collection, 2015;103–195.
53. Knapp JE และ Bettisti DL. การฆ่าเชื้อ การทำให้ปลอดเชื้อ และการถนอมอาหาร (ฉบับที่ 5) (บรรณาธิการ S. S. Block) ฟิลาเดลเฟีย สหรัฐอเมริกา: Lippincott Williams & Wilkins, 2001.
54. Simpson G, Miller RF, Laxton GD, & Clements WR. การมุ่งเน้นไปที่คลอรีนไดออกไซด์: สารฆ่าเชื้อ “ในอุดมคติ” นิวออร์ลีนส์ สหรัฐอเมริกา 1993
55. Gunn JS, Bakaletz LO, & Wozniak DJ. สิ่งที่อยู่ภายนอกมีความสำคัญ: บทบาทของสารโพลีเมอร์นอกเซลล์ของไบโอฟิล์มแกรมลบในการหลีกเลี่ยงภูมิคุ้มกันของโฮสต์และเป็นเป้าหมายสำหรับการแทรกแซงทางการรักษา วารสารเคมีชีวภาพ 2016;291(24), 12538–12546
56. Ramos-Gallardo G. บาดแผลเรื้อรังในการบาดเจ็บจากไฟไหม้: รายงานกรณีศึกษาเกี่ยวกับความสำคัญของไบโอฟิล์ม วารสารศัลยกรรมพลาสติกโลก 2016;5(2), 175
57. Hall CW, & Mah TFM. กลไกโมเลกุลของการดื้อยาปฏิชีวนะและความทนทานต่อยาปฏิชีวนะในแบคทีเรียก่อโรคโดยอาศัยไบโอฟิล์ม FEMS Microbiology Reviews, 2017;41(3), 276-301.
58.Insignares-Carrione E, Bolano Gomez B, Andrade Y, Callisperis P, Suxo MA, Arturo MA, & Camila GO. การกำหนดประสิทธิภาพของคลอรีนไดออกไซด์ในการรักษา COVID 19 วารสาร Molecular and Genetic Medicine.2021;15, S2.
59.Noszticzius Z, Wittmann M, Kály-Kullai K, Beregvári Z, Kiss I, Rosivall L, & Szegedi J. คลอรีนไดออกไซด์เป็นสารต้านจุลชีพที่เลือกขนาด PLoS One, 2013;8(11), e79157.
60.Miura T, & Shibata T. ผลต้านไวรัสของคลอรีนไดออกไซด์ต่อไวรัสไข้หวัดใหญ่และการประยุกต์ใช้ในการควบคุมการติดเชื้อ วารสาร Open Antimicrobial Agents.2010;2, 1.
61.Sanekata T, Fukuda T, Miura T, Morino U, Lee C, Maeda K, Shibata T.การประเมินฤทธิ์ต้านไวรัสของคลอรีนไดออกไซด์และโซเดียมไฮโปคลอไรต์ต่อไวรัส feline calicivirus, ไวรัสไข้หวัดใหญ่ในมนุษย์, ไวรัสโรคหัด, ไวรัสไข้หัดสุนัข, ไวรัสเริมในมนุษย์, ไวรัสอะดีโนในมนุษย์, ไวรัสอะดีโนในสุนัข และไวรัสพาร์โวในสุนัข Biocontrol Science, 2010;15(2), 45-49.
62.Ma JW, Huang BS, Hsu CW, Peng CW, Cheng ML, & Kao JY.การประเมินประสิทธิภาพและความปลอดภัยของสารละลายคลอรีนไดออกไซด์ International Journal of Environmental Research & Public Health. 2017;14(3), 329.
63.Ofori I, Maddila S, Johnson L, & Jonnalagadda SB. การยับยั้ง Pseudomonas aeruginosa และ Staphylococcus aureus ในน้ำด้วยคลอรีนไดออกไซด์: จลนศาสตร์และกลไก วารสารวิศวกรรมการประมวลผลน้ำ 2018;26, 46–54.
64. Ogata N และ Shibata T. ผลการป้องกันของก๊าซคลอรีนไดออกไซด์ความเข้มข้นต่ำต่อการติดเชื้อไวรัสไข้หวัดใหญ่ A วารสารไวรัสวิทยาทั่วไป 2008;89, 60-67.
65. Georgiou G. การกำจัด MRSA โดยใช้คลอรีนไดออกไซด์ วารสารแบคทีเรียวิทยาและเชื้อรา: การเข้าถึงแบบเปิด 2021;9(3), 115-120.
66. Young RO. คลอรีนไดออกไซด์ (CLO2) เป็นสารต้านจุลชีพที่ไม่เป็นพิษสำหรับไวรัส แบคทีเรีย และยีสต์ (Candida Albicans) วารสารวัคซีนและการฉีดวัคซีนนานาชาติ 2016 ตุลาคม 8;2(6), 11-12.
67. Vobolex. กฎหมายโบลิเวีย กฎหมายฉบับที่ 1351. 14 ตุลาคม 2020 สืบค้นจาก Vobolex: https://www.vobolex.org/bolivia/ley-no-1351-del-14-de-octubre-de-2020/
68. Aparicio-Alonso M, Domínguez-Sánchez CA, & Banuet-Martínez M. ผลกระทบระยะยาวของ COVID19 ในผู้ป่วยที่ได้รับการรักษาด้วยคลอรีนไดออกไซด์ วารสารนานาชาติว่าด้วยการวิจัยและการวิเคราะห์แบบสหวิทยาการ 2021;4, 1159-1167.
69. Daniel FB, Condie LW, Robinson M, Stober JA, York GR, Olsen RG, & Wang S R. การศึกษาเปรียบเทียบความเป็นพิษเรื้อรังของสารฆ่าเชื้อสามชนิด วารสารสมาคมงานประปาอเมริกัน 1990;82(10), 61-69.
70.Scatina J, Abdel-Rahman MS, & Gold E. ผลยับยั้งของ alcide® ซึ่งเป็นยาต้านจุลชีพ ต่อการสังเคราะห์โปรตีนใน Escherichia coli วารสารพิษวิทยาประยุกต์ 1985;5(6), 388-394.
71.ATTC-https://www.atcc.org/microbe-products/bacteriology-and-archaea#t=productTab&numberOfResults=2472.https://logosbio.com/
73.Noszticzius Z, Wittmann M, Kály-Kullai K, Beregvári Z, Kiss I, Rosivall L, & Szegedi J. คลอรีนไดออกไซด์เป็นสารต้านจุลชีพที่เลือกขนาดได้ PLoS One, 2013;8(11), e79157.
74.Georgiou G. การกำจัด Borrelia Burgdoferi ในหลอดทดลองโดยใช้คลอรีนไดออกไซด์: แนวทางใหม่, Medical Research Archives. 2022;[ออนไลน์] 10(11). https://doi.org/10.18103/mra.v10i11.3279
75.ราชกิจจานุเบกษาของโบลิเวีย.กฎหมายฉบับที่ 1351.2020, 14 ตุลาคม.สืบค้นเมื่อจาก Derechoteca: https://www.derechoteca.com/gacetabolivia/ley-no-1351-del-14-de-octubre-de-2020/
76.Humble J. (เข้าถึง 2023). คำรับรอง MMS. ดึงข้อมูลจากคำรับรองของ MMS: https://mmstestimonials.co/