หน้าหลักนี้ประกอบด้วยเอกสารฉบับแปลของบทความวิชาการต้นฉบับ อย่างไรก็ตาม เรา ได้จัดทำสรุปเนื้อหาที่สำคัญแบบย่อยง่ายไว้ให้ผู้อ่านได้ศึกษาเป็นลำดับแรก เพื่อให้เข้าใจภาพรวมของงานวิจัยชิ้นนี้ได้อย่างรวดเร็ว หากท่านมีความสนใจในรายละเอียดเชิงลึกหรือข้อมูลทางสถิติเพิ่มเติม ท่านสามารถเลือกอ่านเอกสารฉบับเต็มได้ทั้งในรูปแบบภาษาอังกฤษ (Original) ได้ที่ลิงก์นี้:https://pubmed.ncbi.nlm.nih.gov/6295277/ หรือหากต้องการอ่านฉบับภาษาไทย (Translated) เราได้จัดทำบทแปลไว้ให้แล้วในหน้านี้ (ล่างสุด)
บทความวิจัยนี้ศึกษาถึง กลไกการยับยั้งเชื้อโปลิโอไวรัส (Poliovirus) ด้วยคลอรีนไดออกไซด์ (Chlorine Dioxide – ClO2) และไอโอดีน โดยพบว่าสารทั้งสองชนิดมีประสิทธิภาพในการทำลายฤทธิ์ของไวรัสได้ดีกว่าในสภาวะที่เป็นด่าง (pH 10.0) เมื่อเทียบกับสภาวะที่เป็นกรด (pH 6.0) ผลการวิเคราะห์พบว่าสารทั้งสองทำปฏิกิริยากับโปรตีนเปลือกหุ้ม (Capsid proteins) ของไวรัสและทำให้ค่า pI เปลี่ยนแปลงไป อย่างไรก็ตาม กลไกการยับยั้งมีความแตกต่างกัน โดยไอโอดีนจะเข้าไปทำลายความสามารถในการเกาะติดกับเซลล์เจ้าบ้าน (HeLa cells) ในขณะที่ คลอรีนไดออกไซด์จะเข้าไปทำปฏิกิริยากับ RNA ของไวรัส ซึ่งส่งผลโดยตรงต่อการยับยั้งความสามารถของรหัสพันธุกรรม (Genome) ในการทำหน้าที่เป็นต้นแบบ (Template) สำหรับการสังเคราะห์ RNA ใหม่ จึงทำให้ไวรัสไม่สามารถเพิ่มจำนวนได้
ข้อมูลการเผยแพร่
-
ชื่อบทความ: Mechanisms of inactivation of poliovirus by chlorine dioxide and iodine (กลไกการยับยั้งเชื้อโปลิโอไวรัสโดยคลอรีนไดออกไซด์และไอโอดีน)
-
วารสารที่ตีพิมพ์: Applied and Environmental Microbiology, เล่มที่ 44, ฉบับที่ 5, หน้า 1064–1071 (พฤศจิกายน 1982)
-
ผู้เขียน: 1. M. E. Alvarez (New Mexico State University, USA) 2. R. T. O’Brien (New Mexico State University, USA)
บทคัดย่อ
คลอรีนไดออกไซด์และไอโอดีนทำให้ไวรัสโปลิโอไม่ทำงานได้อย่างมีประสิทธิภาพมากขึ้นที่ pH 10.0 มากกว่าที่ pH 6.0 การวิเคราะห์การตกตะกอนของไวรัสที่ถูกทำให้ไม่ทำงานโดยคลอรีนไดออกไซด์ และไอโอดีนที่ pH 10.0 แสดงให้เห็นว่า RNA ของไวรัสแยกออกจากแคปซิด ส่งผลให้ไวริออนเปลี่ยนจากโครงสร้าง 156S เป็นอนุภาค 80S RNA ที่ปล่อยออกมาจากไวรัสที่ถูกทำให้ไม่ทำงานโดยทั้งคลอรีนไดออกไซด์และไอโอดีนตกตะกอนร่วมกันกับ RNA ของไวรัส 35S ที่สมบูรณ์ ทั้งคลอรีนไดออกไซด์และไอโอดีนทำปฏิกิริยากับโปรตีนแคปซิดของไวรัสโปลิโอและเปลี่ยนค่า pI จาก pH 7.0 เป็น pH 5.8
อย่างไรก็ตามกลไกการทำให้ไวรัสโปลิโอไม่ทำงานโดยคลอรีนไดออกไซด์และไอโอดีนนั้น พบว่าแตกต่างกัน ไอโอดีนทำให้ไวรัสไม่ทำงานโดยทำให้ความสามารถในการดูดซับไปยังเซลล์ HeLa ลดลง ในขณะที่ไวรัสที่ถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์สามารถดูดซับ แทรกซึม และเริ่มต้นการปลดเปลือกได้ตามปกติ การวิเคราะห์การตกตะกอนของสารสกัดจากเซลล์ HeLa ที่ติดเชื้อไวรัสที่ถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์แสดงให้เห็นว่าการรวมตัวของ [14C]ยูริดีนใน RNA ของไวรัสใหม่ลดลง ดังนั้นเราจึงสรุปได้ว่าคลอรีนไดออกไซด์ทำให้ไวรัสโปลิโอไม่ทำงานโดยทำปฏิกิริยากับ RNA ของไวรัสและทำให้ความสามารถของจีโนมไวรัสในการทำหน้าที่เป็นแม่แบบสำหรับการสังเคราะห์ RNA ลดลง
บทนำ
ความสำคัญของการประเมินตัวแทนที่ให้ทางเลือกอื่นแทนคลอรีนในการฆ่าเชื้อน้ำและน้ำเสียเป็นที่ประจักษ์ชัด หนึ่งในปัจจัยหลักที่กระตุ้นความสนใจในสารฆ่าเชื้อทางเลือกคือคลอรีนสามารถทำปฏิกิริยากับสารอินทรีย์เพื่อสร้างสารประกอบที่อาจเป็นอันตรายได้ นอกจากนี้ ยังมีรายงานว่ามีการแยกเอนเทอโรไวรัสที่ทนต่อคลอรีนได้จากน้ำดื่มที่ผ่านการบำบัดแล้ว แม้ว่ากลไกการยับยั้งไวรัสโดยฮาโลเจนจะยังไม่เป็นที่เข้าใจดีนัก แต่ก็มีการเสนอแนะว่าสารประกอบที่ทำลายกิจกรรมทางชีวภาพของเอนเทอโรไวรัสโดยการทำลาย RNA จะมีประสิทธิภาพเหนือกว่าคลอรีนในฐานะสารฆ่าเชื้อ สารฆ่าเชื้อไวรัสสองชนิดที่ยังไม่ได้รับการศึกษาอย่างกว้างขวางในแง่ของกลไกการยับยั้งไวรัสคือคลอรีนไดออกไซด์และไอโอดีน คลอรีนไดออกไซด์ได้รับการพิสูจน์แล้วว่ามีประสิทธิภาพอย่างน้อยเท่ากับคลอรีนในฐานะสารฆ่าเชื้อ
แม้ว่าไอโอดีนจะยังไม่ได้รับการศึกษาอย่างกว้างขวางในฐานะสารฆ่าไวรัส แต่ประสิทธิภาพของมันในฐานะสารฆ่าแบคทีเรียและไวรัสได้รับการยอมรับแล้ว (5, 7) ในรายงานนี้ กลไกการยับยั้งไวรัสโปลิโอโดยคลอรีนไดออกไซด์และไอโอดีนได้รับการเปรียบเทียบกัน ผลลัพธ์บ่งชี้ว่าคลอรีนไดออกไซด์
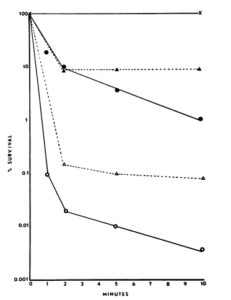
ภาพที่ 1 การทำลายไวรัสโปลิโอด้วยคลอรีนไดออกไซด์ 1.0 มิลลิกรัมต่อลิตร หรือไอโอดีน 2.5 มิลลิกรัมต่อลิตร สัญลักษณ์: 0, คลอรีนไดออกไซด์ที่ pH 6.0; 0, คลอรีนไดออกไซด์ที่ pH 10.0; A, ไอโอดีนที่ pH 6.0; A\, ไอโอดีนที่ pH 10.0; x, กลุ่มควบคุมไวรัสที่ไม่ได้รับการรักษาที่ค่า pH 6.0 และ 10.0
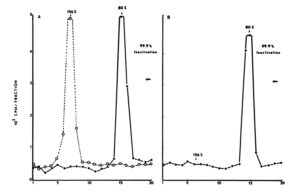
ภาพที่ 2 ผลกระทบของคลอรีนไดออกไซด์และไอโอดีนต่อค่าสัมประสิทธิ์การตกตะกอนของไวรัสโปลิโอที่ติดฉลากแคปซิดที่ pH 10.0 ไวรัสถูกสัมผัสกับคลอรีนไดออกไซด์ 1.0 มิลลิกรัมต่อลิตรเป็นเวลา 1.0 นาที (A) หรือไอโอดีน 2.5 มิลลิกรัมต่อลิตรเป็นเวลา 2.0 นาที (B) จากนั้นนำไปปั่นเหวี่ยงที่ 30,000 รอบต่อนาทีในสารละลายกลีเซอรอลความเข้มข้น 15 ถึง 30% เป็นเวลา 3 ชั่วโมงในโรเตอร์ SW41 เส้นประแสดงถึงโปรไฟล์ของไวรัสควบคุม ทิศทางการตกตะกอนแสดงด้วยลูกศรแนวนอน
เครื่องมือและวิธีการ
การเตรียมไวรัสและสายเซลล์ ไวรัสโปลิโอชนิดที่ 1 (Mahoney) ถูกนำมาใช้ในการศึกษานี้ เราใช้เซลล์ HeLa ชั้นเดียวเพื่อขยายพันธุ์และทดสอบไวรัส วิธีการสำหรับการทดสอบคราบจุลินทรีย์ การติดฉลากด้วยสารกัมมันตรังสี และการทำให้บริสุทธิ์ของสารแขวนลอยของไวรัสได้รับการอธิบายไว้แล้วก่อนหน้านี้
การเตรียมและการวิเคราะห์สารละลายฮาโลเจน คลอรีนไดออกไซด์ถูกสร้างขึ้นและความเข้มข้นของมันถูกกำหนดโดยวิธีการที่อธิบายโดย Roller et al. ความเข้มข้นของคลอรีนไดออกไซด์ที่ใช้ในการทดลองระบุไว้ในข้อความ สารละลายไอโอดีน 2.5% ในเอทานอล-น้ำ 50° ถูกใช้เป็นแหล่งของไอโอดีน ความเข้มข้นของไอโอดีนถูกกำหนดโดยวิธีไดเอทิล-พี-ฟีนิลีนไดอะมีน ซึ่งถูกดัดแปลงสำหรับปริมาตรน้อยโดยการเติมรีเอเจนต์ฮาโลเจนทั้งหมด 0.04 กรัมลงในสารละลายไอโอดีนที่เจือจางอย่างเหมาะสมในปริมาตรสุดท้าย 5.0 มล. ของน้ำกลั่นบริสุทธิ์ ความเข้มข้นของไอโอดีนที่ใช้ในการทดลองการยับยั้งระบุไว้ในข้อความ
การทดลองการทำให้ไวรัสไม่ทำงาน บัฟเฟอร์ฟอสเฟต 0.05 M ที่ปราศจากฮาโลเจน (pH 6.0) และบัฟเฟอร์บอเรต 0.05 M ที่ปราศจากฮาโลเจน (pH 10.0) ถูกนำมาใช้เป็นตัวกลางแขวนลอยสำหรับการทดลองการยับยั้งปริมาตรปฏิกิริยาสุดท้ายมีตั้งแต่ 1.0 ถึง 3.0 มล. และการทดลองการยับยั้งทั้งหมดดำเนินการที่ 25°C เติมสารละลายฮาโลเจนที่มีความเข้มข้นที่ต้องการลงในสารแขวนลอยไวรัสในบัฟเฟอร์ที่มีไวรัส 107 ถึง 108
PFU/มล. เมื่อสิ้นสุดเวลาการสัมผัส ฮาโลเจนที่เหลืออยู่จะถูกยับยั้งโดยการเติมสารละลายโซเดียมไทโอซัลเฟต 0.1% ปริมาณ 0.1 ถึง 0.3 มล.
การตกตะกอนและการแยกโปรตีนด้วยวิธีไอโซอิเล็กทริกโฟกัสของไวรัส ขั้นตอนที่ใช้ในการกำหนดลักษณะการตกตะกอนของไวรัสและส่วนประกอบของไวรัสและเทคนิคการโฟกัสไอโซอิเล็กทริกได้รับการอธิบายไว้ก่อนหน้านี้แล้ว
การจับตัวของ 125I กับไวรัสโปลิโอ ธาตุ 1251 (150 mCi/mmol) ซื้อจาก New England Nuclear Corp. และเจือจางให้มีความเข้มข้น 90,000 cpm/ml (450,000 dpm) ในสารละลายไอโอดีนเข้มข้นที่ไม่มีฉลากซึ่งมีไอโอดีน 25 มก.ต่อลิตร การทดลองการจับและการทำให้ไอโอดีนไม่ทำงานดำเนินการโดยการเติมสารละลายฮาโลเจนเข้มข้น 0.1 มล. ลงในบัฟเฟอร์ 0.9 มล. ที่มีไวรัสโปลิโอ 107 PFU ตามด้วยการวิเคราะห์การตกตะกอนดังที่อธิบายไว้ข้างต้น
การทดลองการดูดซับและการแทรกซึมของไวรัส รวมถึงการถอดเปลือกหุ้มไวรัส การดูดซับของไวรัสที่ถูกทำให้ไม่ทำงานด้วยฮาโลเจนไปยังเซลล์ HeLa ถูกกำหนดโดยการติดเชื้อเซลล์ HeLa แต่ละชั้น (ประมาณ 14 cm2) ด้วยสารละลายไวรัสควบคุมหรือไวรัสที่ถูกทำให้ไม่ทำงานด้วยฮาโลเจนที่ติดฉลากแคปซิด 0.2 มล.หลังจากระยะเวลาการดูดซับ 30 นาทีที่ 37°C ชั้นเซลล์ถูกล้างห้าครั้งด้วยสารละลายบัฟเฟอร์ฟอสเฟตเซลล์ถูกกำจัดออกด้วยทริปซิน-EDTA (GIBCO Laboratories) และสารละลายเซลล์ถูกทำให้เย็นลงที่ 4°C โดยการเติมสารละลายบัฟเฟอร์ฟอสเฟตในปริมาณเท่ากัน เซลล์ถูกตกตะกอนโดยการปั่นเหวี่ยงที่ 8,000 รอบต่อนาทีเป็นเวลา 20 นาที ตะกอนถูกแขวนลอยในโซเดียมโดเดซิลซัลเฟต 0.01% 0.4 มล. และเซลล์ถูกทำลายโดยการใช้คลื่นเสียงที่ 30 วัตต์เป็นเวลา 10 วินาที
เซลล์แขวนลอยที่แตกตัวแล้วแต่ละตัวอย่างถูกเติมลงในค็อกเทลเรืองแสง 10.0 มิลลิลิตร และปริมาณกัมมันตภาพรังสีในแต่ละตัวอย่างถูกนับด้วยเครื่องสเปกโทรเมตรเรืองแสงแบบของเหลว การดูดซับของไวรัสเข้าสู่เซลล์ถูกกำหนดโดยการวัดกัมมันตภาพรังสีที่เกี่ยวข้องกับเซลล์การทดลองการแทรกซึมและการปลดเปลือกของไวรัสถูกดำเนินการในลักษณะเดียวกัน ยกเว้นว่าไวรัสถูกปล่อยให้มีปฏิสัมพันธ์กับเซลล์นานถึง 60 นาทีที่อุณหภูมิ 37°C หลังจากที่เซลล์ถูกนำออกและแตกตัวตามที่อธิบายไว้ข้างต้น ตัวอย่างถูกวางลงบนสารละลายกลีเซอรอลที่มีความเข้มข้น 15 ถึง 30% และปั่นเหวี่ยงเป็นเวลา 3 ชั่วโมงที่ 30,000 รอบต่อนาทีในโรเตอร์ SW41 ที่อุณหภูมิ 4°C สารละลายที่มีความเข้มข้นถูกแยกส่วน และส่วนต่างๆ ถูกวิเคราะห์โดยสเปกโทรเมตรีเรืองแสงแบบของเหลว
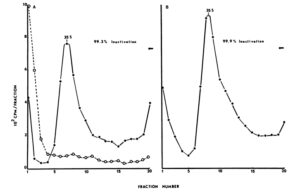
ภาพที่ 3 ผลกระทบของคลอรีนไดออกไซด์และไอโอดีนที่ pH 10.0 ต่อลักษณะการตกตะกอนของ RNA ของไวรัสโปลิโอ ไวรัสที่มี RNA ที่ติดฉลากถูกสัมผัสกับคลอรีนไดออกไซด์ 1.0 มิลลิกรัมต่อลิตร เป็นเวลา 1.0 นาที (A) หรือไอโอดีน 2.5 มิลลิกรัมต่อลิตร เป็นเวลา 2.0 นาที (B) จากนั้นสารละลายไวรัสถูกปั่นเหวี่ยงที่ 65,000 รอบต่อนาที ในกลีเซอรอลไล่ระดับความเข้มข้น 5 ถึง 30% เป็นเวลา 90 นาที ในโรเตอร์ SW65 โปรไฟล์ไวรัสควบคุมแสดงด้วยเส้นประ ทิศทางการตกตะกอนแสดงด้วยลูกศรแนวนอน
ผลกระทบของคลอรีนไดออกไซด์ต่อการสังเคราะห์ RNA ของไวรัสโปลิโอ เซลล์ HeLa แต่ละชั้น (14 cm²) ถูกติดเชื้อด้วยตัวอย่างไวรัสควบคุมหรือไวรัสที่ถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์ 0.5 มล.
หลังจาก 30 นาที เติมสารละลายอาหารเลี้ยงเซลล์พื้นฐาน (minimal essential medium) 5.0 มล. ที่มีซีรั่มลูกวัวแรกเกิด 5% และบ่มเพาะที่อุณหภูมิ 37°C เป็นเวลา 90 นาที จากนั้นเปลี่ยนสารละลายอาหารเลี้ยงเซลล์เป็นสารละลายอาหารเลี้ยงเซลล์พื้นฐาน (minimal essential medium) 5.0 มล. ที่มีซีรั่มลูกวัวแรกเกิด 5%, แอคติโนไมซิน ดี 5.0 ไมโครกรัมต่อมล. และยูริดีน [“4C] 0.5 ไมโครคูรี (53 มิลลิคูรี/มิลลิโมล กิจกรรมจำเพาะ) ต่อมล. บ่มเพาะเซลล์เป็นเวลา 3 ชั่วโมงที่อุณหภูมิ 37°C เพื่อให้ยูริดีน [“4C] ถูกรวมเข้ากับโมเลกุล RNA ของไวรัสใหม่สารละลายที่มี [“4C]uridine ถูกเททิ้ง ชั้นเซลล์ถูกล้าง 5 ครั้ง ด้วยสารละลายบัฟเฟอร์ฟอสเฟต และเซลล์ถูกแยกออกด้วยทริปซินและปั่นเหวี่ยงตามที่อธิบายไว้ข้างต้น
หลังจากแขวนตะกอนในบัฟเฟอร์ 0.3 มล. (0.005 M Tris, 0.0005 M EDTA, 0.05 M NaCl, pH 7.5) เติมโซเดียมโดเดซิลซัลเฟตจนมีความเข้มข้นสุดท้าย 0.01% เนื่องจากเซลล์ถูกทำลายโดยการรักษานี้ ขั้นตอนการใช้คลื่นเสียงจึงถูกละเว้นเพื่อหลีกเลี่ยงการแตกหักที่อาจเกิดขึ้นของโมเลกุล RNA ของไวรัสที่สังเคราะห์ขึ้นใหม่ เซลล์ที่ถูกทำลายแล้วถูกวางลงบนกราเดียนต์กลีเซอรอล 5 ถึง 30% ที่เตรียมไว้ล่วงหน้า ซึ่งถูกปั่นเหวี่ยงที่ 40,000 รอบต่อนาที เป็นเวลา 5 ชั่วโมง ที่ 4°C ในโรเตอร์ SW41 กราเดียนต์ ถูกแยกส่วน และจำนวนรวมต่อนาทีในทุกส่วนถูกกำหนดโดยสเปกโทรเมตรีการเรืองแสงของเหลว
ผลลัพธ์
ผลของค่า pH ต่อการยับยั้ง มีรายงานว่าคลอรีนไดออกไซด์มีประสิทธิภาพในการฆ่าเชื้อไวรัสได้ดีกว่าที่ค่า pH ด่าง ข้อมูลของเราสอดคล้องกับผลการค้นพบเหล่านี้: เราพบว่าคลอรีนไดออกไซด์ที่ความเข้มข้น 1.0 มก./ลิตร สามารถยับยั้งไวรัสโปลิโอได้อย่างมีประสิทธิภาพมากกว่าที่ค่า pH 10.0 มากกว่าที่ค่า pH 6.0 (รูปที่ 1) เช่นเดียวกับคลอรีนไดออกไซด์ ไอโอดีนก็มีฤทธิ์ฆ่าเชื้อไวรัสได้ดีกว่าที่ค่า pH 10.0 มากกว่าที่ค่า pH 6.0 อย่างไรก็ตาม ผลลัพธ์บ่งชี้ว่าคลอรีนไดออกไซด์มีประสิทธิภาพในการฆ่าเชื้อไวรัสมากกว่าไอโอดีน
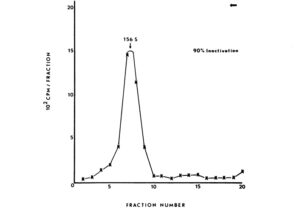
ภาพที่ 4 ผลกระทบของคลอรีนไดออกไซด์และไอโอดีนต่อค่าสัมประสิทธิ์การตกตะกอนของไวรัสโปลิโอที่มีแคปซิดที่ติดฉลากที่ pH 6.0 ไวรัสถูกสัมผัสกับคลอรีนไดออกไซด์ 1.0 มิลลิกรัมต่อลิตร (0) หรือไอโอดีน 2.5 มิลลิกรัมต่อลิตร (x) เป็นเวลา 2.0 นาที จากนั้นนำไปปั่นเหวี่ยงที่ 30,000 รอบต่อนาทีในสารละลายกลีเซอรอลความเข้มข้น 15 ถึง 30% เป็นเวลา 3 ชั่วโมงในโรเตอร์ SW41 ทิศทางการตกตะกอนแสดงด้วยลูกศรแนวนอน
ผลกระทบของคลอรีนไดออกไซด์และไอโอดีนต่อองค์ประกอบของไวรัส เราสังเกตเห็นผลกระทบต่อโครงสร้างของไวรัสที่คล้ายกับที่เคยรายงานไว้ก่อนหน้านี้สำหรับคลอรีน: การทำให้ไวรัสโปลิโอไม่ทำงานโดยคลอรีนไดออกไซด์ 1.0 มิลลิกรัมต่อลิตร หรือไอโอดีน 2.5 มิลลิกรัมต่อลิตร ที่ pH 10.0 ส่งผลให้ RNA แยกออกจากแคปซิด และการเปลี่ยนแปลงของไวริออนจากโครงสร้าง 156S เป็นอนุภาค 80S (ภาพที่ 2) RNA ที่ปล่อยออกมาจากไวรัสที่ถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์หรือไอโอดีนจะตกตะกอนในตำแหน่งเดียวกับ RNA ของไวรัส 35S (ภาพที่ 3) ที่ pH 6.0 การสัมผัสของไวรัสโปลิโอกับคลอรีนไดออกไซด์ 1.0 มิลลิกรัมต่อลิตร หรือไอโอดีน 2.5 มิลลิกรัมต่อลิตร เป็นเวลา 2.0 นาที ไม่ส่งผลให้เกิดการสูญเสีย RNA จากแคปซิด และไวรัสตกตะกอนเป็นโครงสร้าง 156S
แม้ว่าประชากรไวรัส 90% จะถูกทำให้ไม่ทำงาน (ภาพที่ 4) ก่อนหน้านี้มีรายงานเกี่ยวกับคลอรีนว่าการแยกส่วนประกอบของไวรัสไม่สัมพันธ์กับการทำให้ไม่ทำงาน ผลลัพธ์เหล่านี้บ่งชี้ว่าการสูญเสีย RNA จากแคปซิดของไวรัสโปลิโอไม่ใช่สาเหตุของการทำให้ไม่ทำงาน ดังนั้น การทดลองเกี่ยวกับลักษณะการทำให้ไวรัสไม่ทำงานโดยคลอรีนไดออกไซด์และไอโอดีนจึงทำภายใต้สภาวะที่ลดความเสียหายต่อโครงสร้างของไวรัสให้น้อยที่สุด สำหรับการทดสอบไอโอดีน การทดลองทำด้วยสารละลายที่มีฮาโลเจน <1.0 มิลลิกรัมต่อลิตร ที่ pH 10.0 สำหรับการทดสอบคลอรีนไดออกไซด์ การทดลองดำเนินการโดยใช้สารละลายฮาโลเจน 1.0 มิลลิกรัมต่อลิตร ที่ pH 6.0 ซึ่งอัตราการยับยั้งจะช้าลง (ภาพที่ 1) เนื่องจากความเข้มข้นของคลอรีนไดออกไซด์น้อยกว่า 1.0 มิลลิกรัมต่อลิตรนั้นยากที่จะกำหนดได้อย่างน่าเชื่อถือ
นอกจากนี้ การเตรียมไวรัสที่ถูกยับยั้งแล้วจะถูกปั่นเหวี่ยงในสารละลายกลีเซอรอลที่มีความเข้มข้น 15 ถึง 30% และส่วนที่มีอนุภาค 156S เท่านั้นจะถูกนำมาใช้ วิธีที่ไวต่อการเปลี่ยนแปลงของแคปซิดคือการโฟกัสไอโซอิเล็กทริก ดังนั้น ค่า pl ของไวรัสที่ถูกยับยั้งจึงถูกเปรียบเทียบกับค่า pl ของไวรัสที่ติดเชื้อ ค่า pl ของไวรัสที่ถูกยับยั้งด้วยคลอรีนไดออกไซด์และไอโอดีนมีการเปลี่ยนแปลงอย่างถาวรจาก pH 7.0 เป็น pH 5.8 (ภาพที่ 5) ตามที่ Mandel ระบุว่า ไวรัสโปลิโอที่ผ่านการให้ความร้อนซึ่งมีค่า pl ที่เสถียรที่ pH 4.5 ไม่สามารถดูดซับเข้าสู่เซลล์โฮสต์ได้ ดังนั้น การดูดซับของไวรัสที่มีค่า pl เปลี่ยนแปลงไปยังเซลล์ HeLa จึงถูกนำมาเปรียบเทียบกับการดูดซับของไวรัสควบคุม ไวรัสที่ถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์ดูดซับเข้าสู่เซลล์ HeLa ได้อย่างมีประสิทธิภาพเช่นเดียวกับไวรัสควบคุม (ตาราง 1)
ในทางตรงกันข้ามกับผลลัพธ์เหล่านี้ ข้อมูลแสดงให้เห็นอย่างชัดเจนว่าไวรัสที่ถูกทำให้ไม่ทำงานด้วยไอโอดีนมีศักยภาพในการดูดซับที่ลดลง และการดูดซับที่ลดลงนั้นสัมพันธ์กับปริมาณของการทำให้ไม่ทำงาน ดังนั้น คลอรีนไดออกไซด์และไอโอดีนจึงทำให้ไวรัสโปลิโอไม่ทำงานด้วยกลไกที่แตกต่างกัน แม้ว่าผลกระทบต่อค่า pl จะคล้ายกันก็ตาม
เนื่องจากผลกระทบของไอโอดีนต่อการดูดซับของไวรัสโปลิโอไปยังเซลล์เจ้าบ้าน จึงเป็นที่น่าสนใจที่จะตรวจสอบว่าไอโอดีนเข้าไปเกี่ยวข้องกับอนุภาคไวรัสหรือไม่ ดังนั้นจึงมีการเติม 1251 ลงในสารละลายไอโอดีนที่ใช้ในการทำให้ไวรัสโปลิโอที่ไม่มีฉลากไม่ทำงาน หลังจากที่ไวรัสสัมผัสกับฮาโลเจนแล้ว ตัวอย่างจะถูกวิเคราะห์โดยการปั่นเหวี่ยงแบบโซนในสารละลายกลีเซอรอลความเข้มข้น 15 ถึง 30% ตามที่อธิบายไว้ข้างต้น ผลลัพธ์ของการทดลองเหล่านี้แสดงในภาพที่ 6 ซึ่งแสดงให้เห็นว่าไม่มี 1251 เข้าไปเกี่ยวข้องกับไวรัส
เนื่องจากไวรัสที่ถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์ดูดซับเข้ากับเซลล์ HeLa ได้อย่างมีประสิทธิภาพเช่นเดียวกับไวรัสควบคุม จึงได้ทำการทดลองเพื่อกำหนดความสามารถของไวรัสที่ถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์ในการแทรกซึมเข้าไปในเซลล์ HeLa และเริ่มต้นกระบวนการปลดเปลือกหุ้ม โปรไฟล์การไล่ระดับของเซลล์ที่แตกตัวซึ่งติดเชื้อไวรัสควบคุมหรือไวรัสที่ได้รับการบำบัดด้วยคลอรีนไดออกไซด์แสดงอยู่ในภาพที่ 7 และเห็นได้ชัดว่าไม่มีความแตกต่างระหว่างไวรัสควบคุมและไวรัสที่ถูกทำให้ไม่ทำงาน ในการทดลองเหล่านี้ บทความที่แก้ไขเบื้องต้นและบทความที่แก้ไขเพิ่มเติมที่อธิบายโดย DeSena และ Torian ได้รับการสังเกตในโปรไฟล์การไล่ระดับของเซลล์ที่ติดเชื้อไวรัสควบคุมหรือไวรัสที่ถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์
ตารางที่ 1 ผลกระทบของคลอรีนไดออกไซด์และไอโอดีนต่อการดูดซับไวรัสโปลิโอเข้าสู่เซลล์ HeLa

a. เซลล์ HeLa ถูกติดเชื้อด้วยไวรัสที่มีแคปซิดที่ติดฉลากการดูดซับถูกกำหนดโดยการวัดกัมมันตภาพรังสีของไวรัสที่เกี่ยวข้องกับเซลล์เจ้าบ้าน
b. แสดงเป็นค่าสัมพัทธ์กับการดูดซับไวรัสในกลุ่มควบคุมที่ 100 กิโลจูล
c. แสดงเป็นค่าสัมพัทธ์เมื่อเทียบกับการลดลงของการดูดซับไวรัสในกลุ่มควบคุมเป็น 0%
d. เปอร์เซ็นต์การลดลงของ PFU หลังจากการสัมผัสกับความเข้มข้นของฮาโลเจนที่ระบุ
เนื่องจากไม่พบความแตกต่างในการดูดซับ การแทรกซึม หรือการถอดเปลือกหุ้มระหว่างไวรัสที่ได้รับการบำบัดด้วยคลอรีนไดออกไซด์และไวรัสควบคุม จึงได้พิจารณาความเป็นไปได้ที่คลอรีนไดออกไซด์ทำปฏิกิริยากับ RNA ของไวรัส แม้ว่า RNA ที่ปล่อยออกมาจากไวรัสที่ถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์จะพบว่าตกตะกอนร่วมกับ RNA ของไวรัสที่สมบูรณ์ (ภาพที่ 2) แต่ก็ยังมีความเป็นไปได้ที่โมเลกุลอาจได้รับความเสียหายที่ไม่สามารถตรวจพบได้ด้วยการวิเคราะห์การตกตะกอน ดังนั้นจึงได้ทำการทดลองเพื่อตรวจสอบความสามารถของ RNA
จากไวรัสที่ถูกทำให้ไม่ทำงานในการชี้นำการรวมตัวของ [14C]ยูริดีนเข้าสู่ RNA ของไวรัสใหม่ ไวรัสควบคุมหรือไวรัสที่ถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์ถูกปล่อยให้ดูดซับกับเซลล์ HeLa แทรกซึม ถอดเปลือกหุ้ม และเริ่มต้นการจำลองแบบ RNA แอคติโนไมซิน ดี ถูกเติมในเวลาเดียวกันกับ [14C]ยูริดีน เพื่อหยุดการสังเคราะห์ RNA ที่ชี้นำโดย DNA จึงมั่นใจได้ว่าฉลากกัมมันตรังสีจะถูกรวมเข้ากับ RNA ของไวรัส เซลล์ที่ติดเชื้อถูกทำลาย และ RNA ของไวรัสที่สังเคราะห์ขึ้นใหม่ซึ่งมี [14C]ยูริดีน จะถูกวิเคราะห์ โดยการแยกส่วนตามอัตราและสเปกโทรเมตรีการเรืองแสงของเหลว พบว่ามีการรวม [14C]ยูริดีนเข้าไปในโมเลกุล RNA ใหม่น้อยกว่าในตัวอย่างที่ได้รับการบำบัดด้วยคลอรีนไดออกไซด์ เมื่อเทียบกับกลุ่มควบคุม (ตาราง 2) นอกจากนี้ เปอร์เซ็นต์การลดลง (กำหนดโดยจำนวนนับทั้งหมดต่อนาทีที่รวมเข้าไปใน RNA ของไวรัส) มีความสัมพันธ์ที่ดีพอสมควรกับค่าเปอร์เซ็นต์การไม่ทำงาน
การอภิปราย
ผลลัพธ์ที่นำเสนอในรายงานนี้แสดงให้เห็นว่าการแยก RNA ออกจากแคปซิดของไวรัสโปลิโอเกิดขึ้นภายใต้สภาวะที่ทำให้คลอรีนไดออกไซด์และไอโอดีนสามารถยับยั้งได้อย่างมีประสิทธิภาพมากขึ้น ปรากฏการณ์เดียวกันนี้ยังได้รับการรายงานเกี่ยวกับการยับยั้งไวรัสโปลิโอโดยคลอรีนและโบรมีนคลอไรด์ ดังนั้น ภายใต้สภาวะที่เหมาะสม การแยกส่วนประกอบของไวรัสดูเหมือนจะเป็นปรากฏการณ์ทั่วไปของการยับยั้งเอนเทอโรไวรัสโดยฮาโลเจน อย่างไรก็ตาม ในทุกกรณี การแยกส่วนประกอบของไวรัสดูเหมือนจะไม่ใช่สาเหตุของการยับยั้งไวรัส
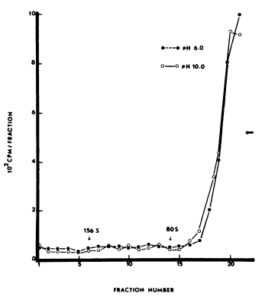
ภาพที่ 6 การจับตัวของ 125I กับไวรัสโปลิโอที่ถูกทำให้ไม่ทำงานด้วยไอโอดีน ไวรัสถูกแขวนลอยในสารละลายไอโอดีน 2.5 มิลลิกรัมต่อลิตรที่มี 1251 อยู่ สารละลายไวรัสถูกปั่นเหวี่ยงในกลีเซอรอลไล่ระดับ 15 ถึง 30°
ที่ 30,000 รอบต่อนาที เป็นเวลา 3 ชั่วโมง ที่ 4°C ในโรเตอร์ SW41 ตำแหน่งของอนุภาค 156S และ 80S แสดงไว้ ทิศทางการตกตะกอนแสดงด้วยลูกศรแนวนอน
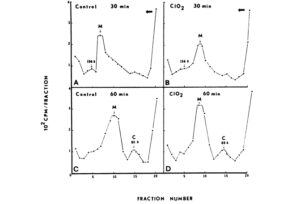
ภาพที่ 7 ผลของคลอรีนไดออกไซด์ต่อการปลดเปลือกของไวรัสโปลิโอที่มีแคปซิดติดฉลากในเซลล์ HeLa สารละลายไวรัสถูกทำให้ไม่ทำงาน 90% ในสารละลายคลอรีนไดออกไซด์ 1.0 มิลลิกรัมต่อลิตร ที่ pH 6.0 เป็นเวลา 2.0 นาที เซลล์ HeLa ถูกติดเชื้อด้วยไวรัสควบคุมหรือไวรัสที่ไม่ทำงาน และในเวลาที่กำหนด เซลล์จะถูกทำให้แตกตัว และสารสกัดจากเซลล์จะถูกปั่นเหวี่ยงในสารละลายกลีเซอรอลที่มีความเข้มข้นไล่ระดับ 15 ถึง 30% เป็นเวลา 3 ชั่วโมง ที่ 30,000 รอบต่อนาที ในโรเตอร์ SW41 ตำแหน่งของอนุภาคที่ถูกดัดแปลงในระยะแรก (M) และอนุภาคที่ถูกดัดแปลงเพิ่มเติม (C) แสดงไว้ ทิศทางการตกตะกอนแสดงด้วยลูกศรแนวนอน
พบว่าไอโอดีนและคลอรีนไดออกไซด์สามารถยับยั้งไวรัสโปลิโอได้อย่างมีประสิทธิภาพมากขึ้นที่ pH 10.0 มากกว่าที่ pH 6.0 ลักษณะของสารประกอบที่มีฤทธิ์มากที่สุดในการฆ่าเชื้อยังไม่ได้มีการศึกษาอย่างละเอียด อย่างไรก็ตาม มีรายงานว่าคลอรีนไดออกไซด์ยังคงไม่แตกตัวในสารละลายในน้ำที่ค่า pH ตั้งแต่ 4.0 ถึง 8.4 ในสารละลายด่าง มันจะแตกตัวเป็นคลอไรต์ (C102-) และคลอเรต (Cd03-) ผ่านปฏิกิริยาต่อไปนี้: 2C102 + 20H- = H20 + C102- + C103- เนื่องจากผลิตภัณฑ์สุดท้ายที่เกิดขึ้นจากการออกซิเดชันของสารอินทรีย์โดยคลอรีนไดออกไซด์ที่ไม่แตกตัวคือไอออน C102- จึงเป็นไปได้ว่า C103- เป็นสารประกอบที่มีฤทธิ์มากที่สุดในการยับยั้งไวรัสโปลิโอที่ระดับ pH เป็นด่าง
อย่างไรก็ตาม ตามที่ Chen ระบุ ปริมาณของ C102- หรือ C103- ที่เกิดขึ้นจากการสลายตัวของ C102 ที่ pH 10 นั้นมีน้อยกว่า 5% ยังไม่ชัดเจนในขณะนี้ว่าปริมาณของคลอไรต์หรือคลอเรตนี้เพียงพอที่จะอธิบายการเพิ่มขึ้นของอัตราการยับยั้งไวรัสโปลิโอที่สังเกตได้ที่ pH 10.0 หรือไม่ คำอธิบายทางเลือกอื่นคือ pH ที่สูงขึ้นจะเพิ่มความไวของไวรัสต่อการโจมตีของ C102 ในสารละลายไอโอดีนที่ pH 10.0 ไอโอดีนมากกว่า 88% อยู่ในรูปของกรดไฮโปไอโอดัส (HIO) ในขณะที่ที่ pH 6.0 ไอโอดีน 90% อยู่ในรูปของไอโอดีนธาตุ ดังนั้น ดูเหมือนว่าไอโอดีนชนิดที่ออกฤทธิ์มากที่สุดในการยับยั้งไวรัสคือโมเลกุล HIO
ดังนั้นจึงไม่น่าแปลกใจที่คลอรีนไดออกไซด์ และไอโอดีนทำให้ไวรัสโปลิโอไม่ทำงานด้วยกลไกที่แตกต่างกัน ผลลัพธ์ของเราบ่งชี้ว่าเมื่อ HIO เป็นสารที่ทำให้ไวรัสไม่ทำงาน ความสามารถของไวรัสในการดูดซับไปยังเซลล์โฮสต์จะลดลง เนื่องจากค่าเปอร์เซ็นต์การทำให้ไม่ทำงานมีความสัมพันธ์กันกับเปอร์เซ็นต์การลดลงของความสามารถในการดูดซับ เราจึงเสนอว่า HIO ทำปฏิกิริยากับเปลือกโปรตีนของไวรัสและไม่ใช่กับ RNA
ข้อเสนอนี้สอดคล้องกับผลการค้นพบของ Hsu ซึ่งรายงานว่า RNA ของไวรัสโปลิโอและฟาจ f2 ทนต่อไอโอดีนได้อย่างสมบูรณ์ ปฏิกิริยาของ HIO กับเปลือกโปรตีนของไวรัสโปลิโอดูเหมือนจะเป็นแบบออกซิเดชันมากกว่าแบบแทนที่ เนื่องจากเราไม่พบหลักฐานการจับตัวของ 1251 กับไวรัสโปลิโอ ไอโอดีนได้รับการพิสูจน์แล้วว่าออกฤทธิ์ต่อโปรตีนและไวรัสอื่นๆ โดยการออกซิเดชันของกลุ่มซัลฟ์ไฮดริล ซึ่งส่งผลให้การจับกับฮาโลเจนเกิดขึ้นน้อยหรือไม่เกิดขึ้นเลย
ตารางที่ 2 การรวมตัวของ [“4C]ยูริดีนเข้าสู่ RNA ของไวรัสในเซลล์ HeLa ที่ติดเชื้อโปลิโอไวรัสควบคุมหรือโปลิโอไวรัสที่ถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์ ในที่ที่มีแอคติโนไมซิน Da
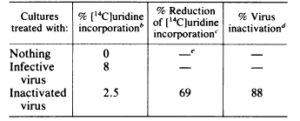
a. สารละลายโปลิโอไวรัสถูกทำให้ไม่ทำงานด้วยคลอรีนไดออกไซด์ก่อนที่จะติดเชื้อเซลล์ HeLa เราเติมแอคติโนไมซิน ดี 5 กรัมต่อมิลลิลิตร และ [‘4C]ยูริดีนลงในเซลล์เพาะเลี้ยงที่ติดเชื้อพร้อมกัน
b. กำหนดจากอัตราส่วนจำนวนนับต่อนาทีของ [4C]ยูริดีนที่รวมเข้ากับ RNA:จำนวนนับทั้งหมดต่อนาทีของ [‘4C]ยูริดีนที่เพิ่มเข้ามา
c. แสดงเป็นเปอร์เซ็นต์ของ [‘4C]ยูริดีนที่ถูกรวมเข้าโดยเซลล์ที่ติดเชื้อไวรัสที่ไม่ทำงาน / เปอร์เซ็นต์ของ [‘4C]ยูริดีนที่ถูกรวมเข้าโดยเซลล์ที่ติดเชื้อไวรัสที่ก่อให้เกิดการติดเชื้อ
d.เปอร์เซ็นต์การลดลงของ PFU โดยคลอรีนไดออกไซด์ e-, ลดลง 0%
Brigano และคณะแนะนำว่าคลอรีนไดออกไซด์ที่ pH 7.0 ทำให้ไวรัสไม่ทำงานโดยการทำให้โปรตีนหุ้มเสียสภาพ อย่างไรก็ตาม สมมติฐานนี้อิงจากการวิเคราะห์ทางอุณหพลศาสตร์ของเส้นโค้งการทำให้ไม่ทำงานมากกว่าการวิเคราะห์โครงสร้างและหน้าที่ของไวรัสที่ไม่ทำงาน ผลลัพธ์ของเราสำหรับการทำให้ไม่ทำงานที่ pH 6.0 บ่งชี้ว่า แม้ว่าคลอรีนไดออกไซด์จะทำปฏิกิริยากับโปรตีนหุ้มและเปลี่ยน pl แต่เป้าหมายที่สำคัญดูเหมือนจะเป็นRNA ของไวรัส ซึ่งมีความสามารถน้อยกว่าในการทำหน้าที่เป็นแม่แบบสำหรับการจำลองแบบ RNA ของไวรัส ความเป็นไปได้ที่กลไกการทำให้ไวรัสโปลิโอไม่ทำงานที่ pH 10.0 แตกต่างจากกลไกสำหรับ
การทำให้ไม่ทำงานที่ pH 6.0 ไม่สามารถตัดทิ้งได้ด้วยผลลัพธ์ในปัจจุบัน
มีการเสนอแนะว่าสารประกอบฆ่าเชื้อไวรัสที่มีประสิทธิภาพมากที่สุดที่ใช้ในการฆ่าเชื้อในน้ำควรทำให้จีโนมของไวรัสไม่ทำงาน ดังนั้น ผลลัพธ์ของเราจึงบ่งชี้ว่าคลอรีนไดออกไซด์อาจเป็นสารฆ่าเชื้อหลักหรือรองที่ดี เนื่องจาก RNA ของไวรัสดูเหมือนจะเป็นเป้าหมายสำคัญที่ pH 6.0 เห็นได้ชัดว่าจำเป็นต้องมีการศึกษาเพิ่มเติมเกี่ยวกับลักษณะของการทำให้ไวรัสไม่ทำงานโดยสารประกอบฮาโลเจน หากต้องการพัฒนาสารฆ่าเชื้อไวรัสที่มีประสิทธิภาพมากขึ้น
กิตติกรรมประกาศ
งานวิจัยนี้ได้รับการสนับสนุนเงินทุนจากสถาบันวิจัยทรัพยากรน้ำแห่งรัฐนิวเม็กซิโก โดยสำนักงานวิจัยและเทคโนโลยีน้ำ กระทรวงมหาดไทย สหรัฐอเมริกา ตามที่ได้รับอนุญาตภายใต้พระราชบัญญัติวิจัยทรัพยากรน้ำ ค.ศ. 1964 กฎหมายมหาชน 88-379 ภายใต้โครงการ A066
เอกสารอ้างอิง
1. Alvarez, M. E. และ R. T. O’Brien. 1982. ผลกระทบของความเข้มข้นของคลอรีนต่อโครงสร้างของไวรัสโปลิโอ Appl. Environ. Microbiol. 43:237-239.
2. Benarde, M. A., B. M. Israel, V. P. Olivieri และ M. L. Granstrom. 1965. ประสิทธิภาพของคลอรีนไดออกไซด์ในฐานะสารฆ่าเชื้อแบคทีเรีย. Appi. Microbiol. 13:776-780.
3. Black, A. P., W. C. Thomas, R. N. Kinman, W. P. Bonner, M. A. Keirn, J. J. Smith และ A. A. Jabero. 1968. ไอโอดีนสำหรับการฆ่าเชื้อในน้ำ. J. Am. Water Works Assoc. 60:69-83.
4. Brigano, F. A. O., P. V. Scarpino, S. Cronier และ M. L. Zink. 1979. ผลกระทบของอนุภาคต่อการยับยั้งเชื้อเอนเทอโรไวรัสในน้ำโดยคลอรีนไดออกไซด์, หน้า 86-92. ใน A. D. Venosa (บรรณาธิการ), ความก้าวหน้าในการฆ่าเชื้อน้ำเสียเทคโนโลยี. เอกสารเผยแพร่ของสำนักงานคุ้มครองสิ่งแวดล้อม หมายเลข EPA-600/9-79-018. สำนักงานคุ้มครองสิ่งแวดล้อมซินซินเนติ โอไฮโอ.
5. Chang, S. L. และ J. C. Morris. 1953. ไอโอดีนธาตุเป็นสารฆ่าเชื้อสำหรับน้ำดื่ม. Ind. Eng. Chem. 45:1009-1012.
6. Chen, T. 1967. การหาปริมาณไมโครของคลอเรต คลอไรต์ ไฮโปคลอไรต์ และคลอไรด์ในเปอร์คลอเรตโดยวิธีสเปกโทรโฟโตเมตริก. Anal. Chem. 39:804-813.
7. Cramer, W. N., K. Kawata และ C. W. Kruse. 1976. การคลอริเนชันและการไอโอดีเนชันของไวรัสโปลิโอและ f2. J. Water Pollut. Control Fed. 48:61-76.
8. DeSena, J. และ B. Torian. 1980. การศึกษาเกี่ยวกับการลอกเปลือกของไวรัสโปลิโอในหลอดทดลอง Virology 104:149-163.
9. Dodgen, H. และ H. Taube. 1949. การแลกเปลี่ยนคลอรีนไดออกไซด์กับไอออนคลอไรต์และกับคลอรีนในสถานะออกซิเดชันอื่นๆ J. Am. Chem. Soc. 71:2501-2504.
10. สำนักงานคุ้มครองสิ่งแวดล้อม. 1979. เคมีของสารฆ่าเชื้อในน้ำ: ปฏิกิริยาและผลิตภัณฑ์ เอกสารเผยแพร่ของสำนักงานคุ้มครองสิ่งแวดล้อม หมายเลข PB-292-776. สำนักงานคุ้มครองสิ่งแวดล้อม วอชิงตัน ดี.ซี.
11. Fraenkel-Conrat, H. 1955. ปฏิกิริยาของไวรัสโมเสกยาสูบกับไอโอดีน J. Biol. Chem. 217:373-381.
12. บริษัท Hach Chemical. 1975. ขั้นตอนการวิเคราะห์น้ำและน้ำเสีย ฉบับที่ 2 หน้า 54. บริษัท Hach Chemical, Ames, Iowa.
13. Hsu, Y. 1964. ความต้านทานของ RNA ที่ติดเชื้อและ DNA ที่เปลี่ยนแปลงต่อไอโอดีนซึ่งทำให้ฟาจ f2 และเซลล์ไม่ทำงาน Nature (London) 203:152-153.
14. Keswick, B. H., R. S. Fujioka และ P. C. Loh. 1981. กลไกการทำให้ไวรัสโปลิโอไม่ทำงานโดยโบรมีนคลอไรด์ Appl. Environ. Microbiol. 42:824-829.
15. Mandel, B. 1971. การจำแนกลักษณะของไวรัสโปลิโอชนิดที่ 1 โดยการวิเคราะห์ด้วยอิเล็กโทรโฟเรซิส Virology 44:554-568.
16. Myhrstad, J. A. และ J. E. Samdal. 1969. พฤติกรรมและการหาปริมาณของคลอรีนไดออกไซด์ J. Am. Water Works Assoc. 61:205-208.
17. O’Brien, R. T. และ J. Newman. 1979. การเปลี่ยนแปลงโครงสร้างและองค์ประกอบที่เกี่ยวข้องกับการยับยั้งไวรัสโปลิโอด้วยคลอรีน Appl. Environ. Microbiol. 38:1034-1039.
18. Roller, S. D., V. P. Olivieri และ K. Kawata. 1980. โหมดของการยับยั้งแบคทีเรียด้วยคลอรีนไดออกไซด์ Water Res. 14:635-641.
19. Scarpino, P. V., F. A. 0. Brigano, S. Cronier และ M. L. Zink. 1979. ผลกระทบของอนุภาคต่อการฆ่าเชื้อเอนเทอโรไวรัสในน้ำด้วยคลอรีนไดออกไซด์ เอกสารเผยแพร่ของสำนักงานคุ้มครองสิ่งแวดล้อม หมายเลข EPA-600/2-79-054 สำนักงานคุ้มครองสิ่งแวดล้อม ซินซินเนติ โอไฮโอ
20. Shaffer, P. T. B., T. G. Metcalf และ 0. J. Sproul. 1980. ความต้านทานต่อคลอรีนของเชื้อโปลิโอไวรัสที่แยกได้จากน้ำดื่ม Appl. Environ. Microbiol. 40:1115-1121.
21. Tenno, K. M., R. S. Fujioka และ P. C. Loh. 1979. กลไกการยับยั้งไวรัสโปลิโอโดยกรดไฮโปคลอรัส หน้า 665-675 ใน R. Jolley, W. A. Brungs และ R. B. Cumming (บรรณาธิการ) รายงานการประชุมครั้งที่สามเรื่อง การคลอรีนน้ำ: ผลกระทบต่อสิ่งแวดล้อมและผลกระทบต่อสุขภาพ Ann Arbor Science Publishers, Inc., Ann Arbor, Mich.
22. Yeager, J. G. และ R. T. O’Brien. 1979. การเปลี่ยนแปลงโครงสร้างที่เกี่ยวข้องกับการยับยั้งไวรัสโปลิโอในดิน Appl. Environ. Microbiol. 38:702-709.