หน้าหลักนี้ประกอบด้วยเอกสารฉบับแปลของบทความวิชาการต้นฉบับ อย่างไรก็ตาม เรา ได้จัดทำสรุปเนื้อหาที่สำคัญแบบย่อยง่ายไว้ให้ผู้อ่านได้ศึกษาเป็นลำดับแรก เพื่อให้เข้าใจภาพรวมของงานวิจัยชิ้นนี้ได้อย่างรวดเร็ว หากท่านมีความสนใจในรายละเอียดเชิงลึกหรือข้อมูลทางสถิติเพิ่มเติม ท่านสามารถเลือกอ่านเอกสารฉบับเต็มได้ทั้งในรูปแบบภาษาอังกฤษ (Original) ได้ที่ลิงก์นี้: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC546889/ หรือหากต้องการอ่านฉบับภาษาไทย (Translated) เราได้จัดทำบทแปลไว้ให้แล้วในหน้านี้ (ล่างสุด)
บทความวิจัยนี้เป็นการศึกษาเกี่ยวกับความคงทนและการยับยั้งเชื้อไวรัสโคโรนาที่ก่อโรคซาร์ส (SARS-CoV) ในสภาวะแวดล้อมต่าง ๆ และการใช้สารฆ่าเชื้อ ผลการทดลองพบว่าไวรัส SARS-CoV สามารถมีชีวิตรอดในอุจจาระและปัสสาวะได้นานถึง 1-2 วันที่อุณหภูมิห้อง และอยู่ได้นานกว่านั้นในอุณหภูมิที่ต่ำกว่า อย่างไรก็ตาม ไวรัสชนิดนี้มีความไวสูงต่อสารฆ่าเชื้อหลายชนิด โดยเฉพาะ คลอรีน (Chlorine) และ คลอรีนไดออกไซด์ (Chlorine Dioxide) ซึ่งสามารถยับยั้งเชื้อได้อย่างสมบูรณ์ในระดับความเข้มข้นที่เหมาะสมภายในระยะเวลาอันสั้น การศึกษานี้เน้นย้ำถึงความสำคัญของการจัดการน้ำเสียและการฆ่าเชื้อในโรงพยาบาล เพื่อป้องกันการแพร่ระบาดของไวรัสผ่านระบบทางเดินอาหารและสิ่งแวดล้อม
ข้อมูลการเผยแพร่
-
ชื่อบทความ: Persistence in environment and resistance to disinfectants of Severe Acute Respiratory Syndrome coronavirus (การคงอยู่ของไวรัสโคโรนาซาร์สในสิ่งแวดล้อมและความต้านทานต่อสารฆ่าเชื้อ)
-
วารสารที่ตีพิมพ์: Antiviral Therapy, เล่มที่ 10, ฉบับที่ 6, หน้า 669–676 (ปี 2005)
-
ผู้เขียน: 1. Bing-Sheng Wang 2. Chao-Xian Li 3. Fu-Huan Chao 4. Min Wang 5. Mao-Long Zhang 6. Xian-Long Shen 7. Zhi-Gang Cai 8. Jun-Wen Li (และคณะ จาก Institute of Health and Environmental Medicine, Tianjin, China)
บทคัดย่อ
มีการนำเสนอข้อมูลการอยู่รอดของเชื้อ Escherichia coli สายพันธุ์ที่พบในอุจจาระ เมื่อสัมผัสกับคลอรีนไดออกไซด์ 3 ระดับความเข้มข้น ที่อุณหภูมิ 4 ระดับ สมการปฏิกิริยาอันดับหนึ่งของ Chick ถูกขยายไปสู่แบบจำลองอันดับ n เทียม การปรับเส้นโค้งแบบไม่เชิงเส้นด้วยวิธี least squares ของข้อมูลการอยู่รอดให้เข้ากับแบบจำลองอันดับ n นั้นดำเนินการบนคอมพิวเตอร์อนาล็อก พบว่าข้อมูลเป็นไปตามจลนศาสตร์อันดับเศษส่วนเมื่อเทียบกับความเข้มข้นของการอยู่รอด โดยมีพลังงานกระตุ้นปรากฏ 12,000 แคลอรี/โมล การทดลองเบื้องต้นสนับสนุนสมมติฐานที่ว่ากลไกการฆ่าเชื้อด้วยคลอรีนไดออกไซด์เกิดขึ้นผ่านการรบกวนการสังเคราะห์โปรตีน
บทนำ
แม้ว่าโดยทั่วไปแล้ว Joseph Lister จะถือได้ว่าเป็นผู้ริเริ่มขั้นตอนการฆ่าเชื้อโรคเชิงปฏิบัติ แต่บทความคลาสสิกของ Kronig และ Paul เป็นผู้แรกที่อธิบายขั้นตอนเชิงปริมาณสำหรับการศึกษาการฆ่าเชื้อโรค สิบปีต่อมา Madsen และ Nyman ตามด้วย Chick อีกหนึ่งปีต่อมา ได้สร้างแบบจำลองทางคณิตศาสตร์สำหรับการฆ่าเชื้อโรคทางเคมีของประชากรจุลินทรีย์ บทความทั้งสองฉบับนี้ได้เสนอความคล้ายคลึงกันระหว่างความเร็วของการฆ่าเชื้อโรคของจุลินทรีย์กับปฏิกิริยาโมเลกุลเดี่ยวหรือปฏิกิริยาอันดับหนึ่ง ซึ่งยังคงเป็นแบบจำลองสำหรับการวิจัยทั้งหมดในภายหลัง
ในช่วง 50 ปีที่ผ่านมา มีการรายงานการปรับปรุงเทคนิค และมีการตั้งสมมติฐานเกี่ยวกับกลไกการทำลายจุลินทรีย์ ในปี 1946 Green และ Stumpf เสนอว่าคลอรีนทำให้จุลินทรีย์ตายโดยการยับยั้งเอนไซม์ที่จำเป็นสำหรับการออกซิเดชันของกลูโคส Knox และคณะ แนะนำว่าเอนไซม์ไตรเอส-ฟอสเฟตดีไฮโดรจีเนสเป็นเป้าหมายหลักของการฆ่าเชื้อด้วยคลอรีน อย่างไรก็ตาม จนถึงปัจจุบัน ยังไม่มีหลักฐานทางชีววิทยาโดยตรงของทฤษฎีใดๆ ดังที่ Wyss เพิ่งกล่าวไว้เมื่อเร็วๆ นี้ ว่า “สาขาการฆ่าเชื้อเป็นสาขาที่ค่อยเป็นค่อยไป” งานวิจัยที่อธิบายไว้ในที่นี้เสนอวิธีการทางคณิตศาสตร์ที่ปรับปรุงแล้วสำหรับการฆ่าเชื้อทางเคมีของประชากรแบคทีเรีย อันเป็นผลมาจากขั้นตอนการสุ่มตัวอย่างที่เป็นเอกลักษณ์และรวดเร็ว สารละลายที่ปราศจากสารอินทรีย์ การหาปริมาณด้วยสเปกโทรโฟโตเมตรีของปริมาณสารฆ่าเชื้อในปริมาณต่ำ (เศษส่วนของมิลลิกรัมต่อลิตร) และทฤษฎีและการออกแบบเครื่องปฏิกรณ์เคมี
นำเสนอส่วนหนึ่งในการประชุมวิชาการนานาชาติด้านจุลชีววิทยาครั้งที่ 9 ณ กรุงมอสโก สหภาพโซเวียต ระหว่างวันที่ 24-30 กรกฎาคม 1966
นอกจากนี้ ผลการทดลองทางชีววิทยาที่เสริมการตีความทางคณิตศาสตร์ของเส้นโค้งอัตราชี้ให้เห็นถึงกลไกของรอยโรคที่ร้ายแรง การตรวจสอบที่อธิบายไว้ในที่นี้เป็นผลสืบเนื่องโดยตรงจากรายงานก่อนหน้านี้โดย Benarde et al. (1) ซึ่งรายงานการฆ่าอย่างมีนัยสำคัญที่ระดับความเข้มข้นน้อยกว่า 30 นาที จุดสิ้นสุดที่มักใช้ในการศึกษาการฆ่าเชื้อโรค ซึ่งดูเหมือนจะบ่งชี้ว่าเป้าหมายหลักได้รับผลกระทบจาก C102 สมมติฐานนี้จึงนำไปสู่การออกแบบอุปกรณ์ที่จะช่วยให้สามารถกำหนดเปอร์เซ็นต์การรอดชีวิตหลังจากช่วงเวลาที่วัดเป็นวินาที ด้วยประสิทธิภาพที่พิสูจน์แล้วของอุปกรณ์นี้ จึงได้ดำเนินการตรวจสอบผลกระทบของอุณหภูมิต่อประสิทธิภาพของการฆ่าเชื้อโรคในชุดนี้ ใช้ค่าคงที่ต่อไปนี้: pH 6.5; ความหนาแน่นของเซลล์ 15,000 ต่อมิลลิลิตร; และตัวทำละลายที่ปราศจากสารอินทรีย์ ตัวแปรคือความเข้มข้นของ CG02 อุณหภูมิ และเวลาสัมผัส
เครื่องมือและวิธีการ
ขั้นตอนการเตรียมน้ำกลั่นปราศจากสารอินทรีย์ (OFD) และเครื่องแก้ว การสร้างสารละลาย C102 บริสุทธิ์ในน้ำ การหยุดปฏิกิริยาการฆ่าเชื้อ การล้างเซลล์แบคทีเรีย และการปรับความหนาแน่นให้เป็นมาตรฐาน ดำเนินการต่อเนื่องตามที่รายงานไว้ก่อนหน้านี้ เพื่อให้ได้ตัวอย่างในช่วงเวลาสั้นๆ เพียง 5 วินาที ชุดอุปกรณ์ปฏิกิริยาจำเป็นต้องมีการดัดแปลงอย่างมาก อุปกรณ์เดิมประกอบด้วยเข็มฉีดยาสองอัน แต่ละอันมีชุดวาล์วแบบบานพับสองทาง ทำให้สามารถดูดและจ่ายตัวอย่างจากภาชนะปฏิกิริยาได้อย่างรวดเร็ว แต่ไม่สามารถดำเนินการได้เร็วพอที่จะนำตัวอย่างออกในช่วงเวลา 5 วินาที เพื่อให้ได้การสุ่มตัวอย่างที่รวดเร็วเช่นนั้น จึงได้ออกแบบระบบความดันแบบปิดเพื่อใช้งานภายในอ่างน้ำที่มีอุณหภูมิคงที่
ภาพที่ 1 แสดงภาพรวมของอุปกรณ์ทั้งหมด อ่างน้ำที่บรรจุภาชนะปฏิกิริยาและสเปกโตรโฟโตมิเตอร์ที่ใช้งานร่วมกับอุปกรณ์สุ่มตัวอย่างแสดงไว้ในภาพ ภาพที่ 2 แสดงชุดประกอบทั้งหมดที่พร้อมใช้งาน ภาพที่ 3 เป็นแผนภาพแสดงส่วนประกอบที่สำคัญทั้งหมดของระบบความดันในระบบถูกสร้างขึ้นโดยการเติมน้ำประปาลงในขวดกรองในระบบปิด และใช้ (i) เพื่อบังคับสารละลาย Cl02 เข้าไปในภาชนะปฏิกิริยาที่มีสารแขวนลอยของแบคทีเรียอย่างรวดเร็ว และ (ii) เพื่อบังคับตัวอย่างจากภาชนะปฏิกิริยาเข้าไปในคิวเวตต์ของสเปกโตรโฟโตมิเตอร์และเข้าไปในหลอดตัวอย่างแบคทีเรีย
การผสมสารแขวนลอยของแบคทีเรียและสารละลาย Cl02 นั้นรวดเร็วและทั่วถึงเนื่องจากความดันที่ใช้ในการบังคับสารละลาย Cl02 เข้าไปในภาชนะปฏิกิริยา หน่วยปลอดเชื้อของภาชนะปฏิกิริยาและกรวยแยกถูกใช้สำหรับการทดลองแต่ละครั้ง ตัวอย่างแบคทีเรียถูกเก็บรวบรวมในหลอดทดลองปลอดเชื้อที่มีสารละลายโซเดียมไทโอซัลเฟต (Na2S2O3) ปลอดเชื้อ การเก็บตัวอย่างแบคทีเรียเกิดขึ้นหลังจากสัมผัสกันเป็นเวลา 5, 10, 15, 20, 25, 30, 60 และ 300 วินาที ตัวอย่างสำหรับเครื่องสเปกโทรโฟโตมิเตอร์ถูกเก็บหลังจากผสมครั้งแรก 3 วินาที บันทึกการเปลี่ยนแปลงความเข้มข้นของ C102 ตลอดช่วงเวลาทดสอบ 5 นาที

ภาพที่ 1 ภาพรวมของชุดอุปกรณ์ปฏิกิริยา

ภาพที่ 2 ชุดประกอบปฏิกิริยาพร้อมใช้งาน
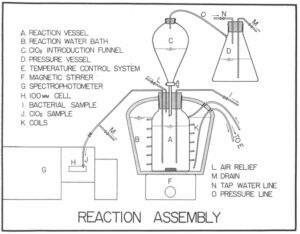
ภาพที่ 3 แผนภาพแสดงส่วนประกอบสำคัญของชุดประกอบปฏิกิริยา
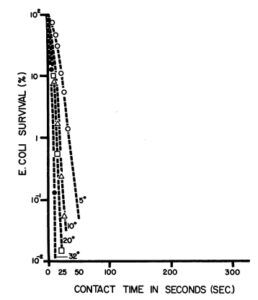
เวลาสัมผัส (วินาที)
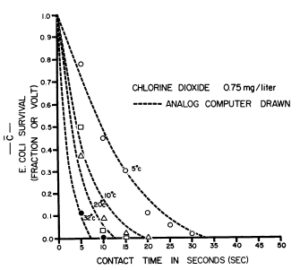
ภาพที่ 4 ผลของอุณหภูมิที่มีต่อการฆ่าเชื้อด้วย 0.75 มิลลิกรัมของคลอรีนไดออกไซด์ต่อลิตร (pH 6.5; IS,O00 เซลล์ต่อมิลลิลิตร)
อุปกรณ์แก้วทั้งหมด สารละลายบัฟเฟอร์ OFD และสารละลาย C102 ถูกเก็บไว้ที่อุณหภูมิของการทดลองก่อนและจนถึงขณะใช้งานอุณหภูมิของวัสดุเหล่านี้และของภาชนะปฏิกิริยาถูกรักษาไว้ภายใน 10.1 องศาเซลเซียส การทดลองแต่ละครั้งทำซ้ำ 3 ครั้ง โดยใช้ความเข้มข้นของ C102 ดังต่อไปนี้: 0.25, 0.50 และ 0.75 มิลลิกรัม/ลิตร ความเข้มข้นเริ่มต้นของสารละลาย C102 เหล่านี้ถูกเตรียมให้มีความเข้มข้นเป็นสองเท่าเพื่อชดเชยการเจือจาง 1:1 ที่ได้จากการผสมปริมาตรเท่ากันของสารแขวนลอยเซลล์และสารละลาย C102 ความเข้มข้นของสารละลายแต่ละชนิดได้รับการตรวจสอบด้วยเครื่องสเปกโทรโฟโตมิเตอร์ก่อนเริ่มการทดลองแต่ละครั้ง
ผลลัพธ์
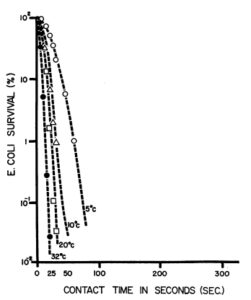
ภาพที่ 4 แสดงกราฟการอยู่รอดเทียบกับเวลาและอุณหภูมิ เมื่อใช้ C102 ที่ความเข้มข้น 0.75 มิลลิกรัมต่อลิตร เห็นได้ชัดว่าประสิทธิภาพในการฆ่าเชื้อแปรผันตรงกับอุณหภูมิ ความสัมพันธ์ที่คล้ายกันนี้พบได้ที่ความเข้มข้น 0.50 และ 0.25 มิลลิกรัมต่อลิตร (ภาพที่ 5 และ 6) เพื่อให้ได้ผลการฆ่าเชื้อ 99% ความเข้มข้น 0.25 มิลลิกรัมต่อลิตร ต้องใช้เวลา 110 วินาทีที่ 5 องศาเซลเซียส 74 วินาทีที่ 10 องศาเซลเซียส 41 วินาทีที่ 20 องศาเซลเซียส และ 16 วินาทีที่ 30 องศาเซลเซียส ซึ่งเร็วกว่าที่ 5 องศาเซลเซียสเกือบสี่เท่า ที่ระดับ 99.9% เวลาที่ใช้ในการฆ่าเชื้อระหว่าง 5 ถึง 30 องศาเซลเซียสเพิ่มขึ้นเป็นห้าเท่า (21 วินาทีที่ 30 องศาเซลเซียส เทียบกับ 150 วินาทีที่ 5 องศาเซลเซียส)
ในช่วงอุณหภูมิ Qlo เดียวกัน คือ 20 ถึง 30 องศาเซลเซียส ค่า Qio ที่คำนวณได้ (โดยอิงจากระดับการฆ่าเชื้อ 30%) คือ 1.67 สำหรับ 0.5 มิลลิกรัม/ลิตร และ 1.23 สำหรับ 0.75 มิลลิกรัม/ลิตร ในช่วงอุณหภูมิ 10 ถึง 20 องศาเซลเซียส ค่า Qlo คือ 1.06 สำหรับทั้ง 0.50 และ 0.75 มิลลิกรัม/ลิตร ค่า Qlo แตกต่างกันไปตามปริมาณยาและอุณหภูมิ ดังนั้น เราจึงต้องระมัดระวังในการใช้ Qlo เป็นดัชนีของอัตราการเกิดปฏิกิริยาที่สัมพันธ์กัน การเพิ่มความเข้มข้นของ C102 มีแนวโน้มที่จะลดเวลาที่จำเป็นสำหรับการฆ่าเชื้อลงอย่างเห็นได้ชัด ที่ระดับ 99% 0.75 มิลลิกรัม/ลิตร ใช้เวลาเพียง 14 วินาทีที่ 30 องศาเซลเซียส เทียบกับ 60 วินาทีที่ 5 องศาเซลเซียส นอกจากนี้ยังเห็นได้ชัดว่ากราฟเหล่านี้ไม่ได้ให้เส้นตรง ซึ่งบ่งชี้ถึงความเบี่ยงเบนจากปฏิกิริยาอันดับหนึ่งแบบง่ายๆ ดังนั้น เพื่อให้ได้ลำดับปฏิกิริยาที่ดีที่สุด จึงจำเป็นต้องใช้วิธีการรักษาที่ซับซ้อนยิ่งขึ้น
จากข้อมูลเหล่านี้ จะเป็นประโยชน์ในการพัฒนาแบบจำลองทางคณิตศาสตร์ที่วิศวกรชีวภาพจะสามารถนำไปใช้ในการออกแบบอุปกรณ์ฆ่าเชื้อได้ ในแบบจำลองเหล่านี้ ความกังวลมักอยู่ที่การหาปริมาณพารามิเตอร์จลนศาสตร์ที่ไม่เป็นเชิงเส้นเหล่านี้ เพื่อจุดประสงค์นี้ เป็นที่พึงปรารถนาที่จะอาศัยแนวทางแบบคลาสสิกที่เชื่อมโยงข้อมูลอัตราการเกิดปฏิกิริยาเคมีที่ซับซ้อนกับอุณหภูมิและความเข้มข้น Chick แนะนำการคำนวณประเภทนี้ ซึ่งถูกนำมาใช้ตลอด 60 ปีที่ผ่านมา อย่างไรก็ตาม ในช่วง 10 ปีที่ผ่านมา มีความก้าวหน้าในแบบจำลองจลนศาสตร์เกิดขึ้น
แบบจำลองจลนศาสตร์ อัตราโดยรวมของการฆ่าเชื้อแบคทีเรีย Escherichia coli ด้วยคลอรีนไดออกไซด์ได้รับอิทธิพลจากปัจจัยพื้นฐานอย่างน้อยสามประการ ได้แก่ (i) การถ่ายเทมวลของ C102 ในของเหลวไปยังส่วนต่อประสานของเหลวของ E. coli (ii) การดูดซับทางเคมีของสารฆ่าเชื้อที่ศูนย์กลางการทำงานที่เลือกบนพื้นผิวเซลล์ และ (iii) การแพร่กระจายบนพื้นผิวและภายในพื้นผิวของสารเชิงซ้อนที่ถูกดูดซับทางเคมีที่ถูกกระตุ้นพร้อมกับการโจมตีทางเคมีต่อองค์ประกอบของเซลล์ การอธิบายกลไกการฆ่าเชื้อจากข้อมูลจลนศาสตร์นั้นค่อนข้างยากลำบากเนื่องจากความเป็นไปได้ที่หลายขั้นตอนอาจเป็นตัวควบคุมอัตรา ดังนั้นจึงเป็นสิ่งสำคัญที่จะต้องพิจารณาก่อนที่จะใช้แบบจำลองจลนศาสตร์ว่าขั้นตอนทางกายภาพ เช่น การถ่ายเทมวลหรือการแพร่กระจายภายในพื้นผิว หรือขั้นตอนทางเคมี เช่น การโจมตีทางเคมีต่อองค์ประกอบของเซลล์ เป็นตัวควบคุมอัตรา มิฉะนั้น การปรับเส้นโค้งให้เข้ากับข้อมูลจะกลายเป็นงานที่ไร้ความหมาย
เนื่องจากกระบวนการทางเคมีส่วนใหญ่มีความไวต่ออุณหภูมิอย่างมาก ซึ่งแตกต่างจากกระบวนการถ่ายเทมวลหรือการแพร่กระจายทางกายภาพล้วนๆ การกำหนดขั้นตอนควบคุมอัตราจึงสามารถทำได้ง่ายขึ้นโดยการสังเกตผลของอุณหภูมิที่เพิ่มขึ้นต่ออัตราการฆ่าเชื้อโดยรวม ในการศึกษาครั้งนี้ พบว่าอุณหภูมิมีผลอย่างมาก ซึ่งชี้ให้เห็นเป็นสมมติฐานเบื้องต้นว่าความต้านทานทางเคมีเป็นตัวควบคุมอัตราการฆ่าเชื้อโดยรวม นอกจากนี้ การกวนส่วนผสมที่ทำปฏิกิริยาอย่างเพียงพอทำให้การถ่ายเทมวลในเฟสของเหลวไม่ใช่ขั้นตอนควบคุมอัตราอีกต่อไป ข้อเท็จจริงเชิงปรากฏการณ์เหล่านี้และสมมติฐานของกลไกควบคุมอัตราทางเคมีทำหน้าที่เป็นจุดเริ่มต้นที่สะดวกสำหรับการสร้างแบบจำลองจลนศาสตร์ที่มีความหมาย
หากถือว่ากฎของมวลสารใช้ได้กับปฏิกิริยาชีวเคมีในลักษณะเดียวกับที่ใช้กับปฏิกิริยาในเฟสของเหลวที่เป็นเนื้อเดียวกันแล้ว สำหรับแบบจำลองเสมือนโมเลกุลเดี่ยว นิพจน์จลนศาสตร์จะกลายเป็น
![]()
สำหรับระบบ E. coli ที่ศึกษา สมการที่ 1 ระบุว่าอัตราการหายไปของเซลล์ E. coli ต่อหน่วยปริมาตรต่อหน่วยเวลาในเครื่องปฏิกรณ์เป็นสัดส่วนกับความเข้มข้น (มวลที่ใช้งาน) ของเซลล์ที่มีอยู่ในระบบ ณ เวลาใด ๆ โดยที่ระบบ ในที่นี้คือส่วนผสมของเหลวในเครื่องปฏิกรณ์ ณ เวลาใด ๆ หากปริมาตรของระบบเกือบคงที่ ซึ่งจะเป็นกรณีสำหรับเครื่องปฏิกรณ์แบบแบทช์ที่ไม่มีการนำตัวอย่างออก สมการที่ 1 จะกลายเป็น
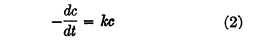
ซึ่งเป็นการแสดงออกตาม “กฎของชิก” แบบคลาสสิกสำหรับการฆ่าเชื้อโรค หากลำดับไม่ใช่ลำดับที่หนึ่งแบบง่ายๆ สมการที่ 2 จะต้องได้รับการแก้ไขให้เหมาะสม ตัวอย่างเช่น
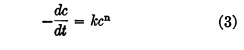
โดยที่ n คือจำนวนจริงใดๆ
ทีนี้ลองพิจารณากรณีทั่วไปที่การนำตัวอย่างออกจากระบบอย่างต่อเนื่องทำให้ปริมาตรเปลี่ยนแปลงไปตามกฎการลดลงของปริมาตร V = V(t) สมการที่ 3 จะกลายเป็น
![]()
ซึ่งลดลงเหลือ
![]()
เห็นได้ชัดว่า กรณีที่ปริมาตรคงที่จะเหมือนกับกรณีที่ปริมาตรแปรผัน โดยมีเงื่อนไขว่าต้องใช้ตัวแปรความเข้มข้นตลอดทั้งกรณี
ตามหลักปรัชญา “ชิคเคียน” เป็นเรื่องปกติที่จะเปรียบเทียบสมการที่ 3 ดังนี้:
![]()
โดยที่ N = จำนวน ไม่ใช่ความเข้มข้น ของเซลล์ที่เหลือรอดในระบบ ดำเนินการเช่นเดียวกับกรณีปริมาตรแปรผัน สมการที่ 6 จะกลายเป็น
![]()
สมการที่ 7 ไม่เหมือนกับสมการที่ 5 เลย และยิ่งไปกว่านั้น ค่า k จากทั้งสองสมการนั้นแตกต่างกันโดยพื้นฐานเนื่องจากหน่วยและรูปแบบทางคณิตศาสตร์ของสมการเชิงอนุพันธ์ แม้ว่าปริมาตรจะคงที่ สมการที่ 5 และ 7
ก็ยังคงแตกต่างกันและกำหนดค่า k ที่แตกต่างกัน ความสัมพันธ์ระหว่างพารามิเตอร์ k ทั้งสองสำหรับระบบปริมาตรแปรผันคือ
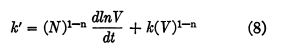
เป็นเรื่องที่น่าสงสัยจริงๆ ว่าทำไม Chick ยกตัวอย่างเช่น ยืนยันที่จะใช้ N ซึ่งเป็นจำนวนเซลล์ที่มีชีวิตในระบบ ในสมการ 1 เป็นมวลที่ออกฤทธิ์ ยิ่งไปกว่านั้นน่าสงสัยยิ่งกว่าคือข้อเท็จจริงที่ว่านักทดลองหลายคนที่ไม่รู้
หลังจาก Chick เห็นได้ชัดว่าใช้ c แทน N เมื่อคำนวณ k ข้อสรุปที่จะดึงมาจากข้อสังเกตเหล่านี้ 5 แสดงถึงแบบจำลอง c น้อยที่สุดของกฎทางเคมีของ n ความสัมพันธ์โดยอิงจาก N ตรงข้ามเพราะ V(t) ต้องถูก kn อธิบายทางคณิตศาสตร์
เวลาสัมผัส (วินาที)
ภาพที่ 5 ผลของอุณหภูมิที่มีต่อการฆ่าเชื้อด้วยคลอรีนไดออกไซด์ 0.50 มิลลิกรัมต่อลิตร (pH 6.5; 15,000 เซลล์ต่อมิลลิลิตร)
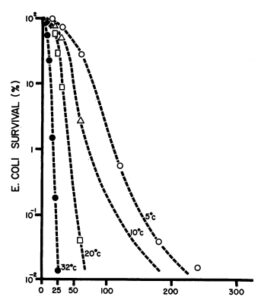
ภาพที่ 6 ผลของอุณหภูมิ 0.25 มิลลิกรัมของคลอรีนไดออกไซด์ต่อเซลล์ต่อมิลลิลิตร)
จุดเน้นในเอกสารนี้ไม่ได้อยู่ที่การปรับเส้นโค้งให้เข้ากับข้อมูลหรือความเหมาะสมของเส้นโค้ง แต่เน้นที่เกณฑ์สำหรับการพัฒนาสมการอัตรา สมการที่ 3 เป็นรูปแบบหนึ่งของกฎการกระทำมวลแบบคลาสสิก ในขณะที่สมการที่ 13 ไม่มีพื้นฐานเช่นนั้น และดังนั้นจึงมีความน่าเชื่อถือน้อยกว่าสมการที่ 3
ในการปรับเส้นโค้ง เราสามารถค้นพบนิพจน์อัตราทางคณิตศาสตร์ได้หลายแบบที่มีความเหมาะสมเท่ากันเสมอ สมการที่ 5 ควรถูกมองว่าเป็นเพียงจุดเริ่มต้นที่ทฤษฎีในอนาคตสามารถต่อยอดได้
การประมาณค่าพารามิเตอร์ โปรดทราบว่าเราตระหนักดีว่าข้อมูลการทดลองของเราอาจไม่จำเป็นต้องใช้การวิเคราะห์ทางสถิติที่ซับซ้อน เทคนิคการปรับเส้นโค้ง และการสร้างแบบจำลองจลนศาสตร์โดยละเอียด รวมถึงการอธิบายกลไก เราสนใจเป็นหลักในการแสดงวิธีการที่ไม่ใช่เชิงเส้นที่สามารถใช้ได้กับข้อมูลประเภทนี้
สำหรับค่าอุณหภูมิและความเข้มข้นของคลอรีนไดออกไซด์เริ่มต้นที่คงที่ พารามิเตอร์ที่ไม่ทราบค่าในสมการที่ 5, & และ n สามารถประมาณได้จากการวิเคราะห์ “ข้อผิดพลาดกำลังสองน้อยที่สุด” เกณฑ์นี้อิงตามรูปแบบเชิงเส้น คือ
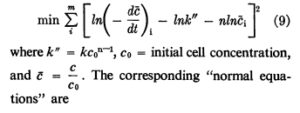
![]()
และ
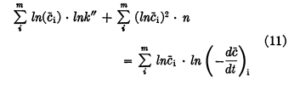
การประมาณค่าพารามิเตอร์จากสมการ 10 และ 11 ใช้เพื่อระบุจุดเริ่มต้นของกริด ซึ่งสามารถเริ่มต้นการค้นหาแบบไม่เชิงเส้นบนคอมพิวเตอร์อนาล็อกได้ แน่นอนว่า k” และ a สามารถประมาณค่าได้จากการวิเคราะห์ “กำลังสองน้อยที่สุด” แบบไม่เชิงเส้นบนคอมพิวเตอร์ดิจิทัล แต่ขั้นตอนนี้จะต้องใช้เทคนิคการค้นหาแบบไม่เชิงเส้น ซึ่งในความเป็นจริงแล้วเทียบเท่ากันในเชิง “ศิลปะ” กับขั้นตอนการประมาณค่าพารามิเตอร์สองขั้นตอน
ที่อธิบายไว้ข้างต้นสำหรับคอมพิวเตอร์อนาล็อก
![]()
โดยภาพที่ 7 และผลลัพธ์สรุปไว้ในตารางที่ 1 และในภาพที่ 8 และ 9 เกณฑ์ความเหมาะสมในภาพที่ 8 และ 9 อิงตามค่าความคลาดเคลื่อนกำลังสองต่ำสุดระหว่างเส้นโค้งอะนาล็อกและจุดทดลอง ผลลัพธ์บ่งชี้ว่าลำดับปฏิกิริยาเมื่อเทียบกับเวลาสัมผัสจะแปรผันตามทั้งอุณหภูมิและความเข้มข้นของ ClO นอกจากนี้ ผลลัพธ์เชิงตัวเลขจากการวิเคราะห์กำลังสองน้อยที่สุดแบบเชิงเส้นไม่สอดคล้องกับค่าคอมพิวเตอร์แบบอนาล็อกเลย ยกเว้นที่อุณหภูมิ 32 องศาเซลเซียส ค่าของ a ถูกคงที่ไว้ที่ค่าที่คำนวณได้จาก 10 และ 11
เนื่องจากพบว่าข้อผิดพลาดในการปรับเส้นโค้งมีความไวต่อ k มากกว่า n ซึ่งยังเป็นพื้นฐานสำหรับการเปรียบเทียบค่า & จากสองวิธีการวิเคราะห์ที่แตกต่างกัน เนื่องจากพบว่า a มีความสำคัญค่อนข้างน้อย จึงได้ลองสร้างกราฟพลังงานกระตุ้นแบบ Arrhenius โดยสมมติว่าความแปรปรวนในลำดับของปฏิกิริยาไม่ได้ทำให้การประมาณค่าพลังงานกระตุ้นไม่ถูกต้อง ผลลัพธ์จากการวิเคราะห์นี้แสดงให้เห็นว่าพลังงานกระตุ้นคือ 12,000 แคลอรี/โมล โดยไม่ขึ้นอยู่กับความเข้มข้นของ ClO
แบบจำลองจลนศาสตร์ สมการที่ 5 พร้อมค่าพารามิเตอร์จากตารางที่ 1 ชี้ให้เห็นแนวทางสำหรับการวิจัยในอนาคตในด้านการฆ่าเชื้อด้วย ClO ก่อนอื่น สมมติว่า C102 เป็นส่วนประกอบที่ทำปฏิกิริยามากเกินไป ซึ่งการเปลี่ยนแปลงความเข้มข้นตามเวลาการฆ่าเชื้อจะไม่เปลี่ยนแปลงอย่างมีนัยสำคัญเท่ากับความเข้มข้นของ E. coli เงื่อนไขนี้ทำให้สมการที่ 5 เป็นสูตรอันดับเทียม n
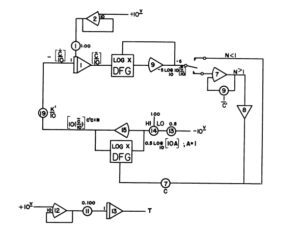
ฐานเวลาแกนแอ็กซิสซา = 5 วินาที/นิ้ว สำหรับเครื่องพล็อตเตอร์ X-Y
ฐานแกนออร์ดิเนต = 1 โวลต์เต็มสเกล
ภาพที่ 7 แผนภาพคอมพิวเตอร์อนาล็อกแบบย่อส่วนสำหรับสมการที่ 54
ตารางที่ 1 สรุปผลการปรับเส้นโค้งจากสมการ
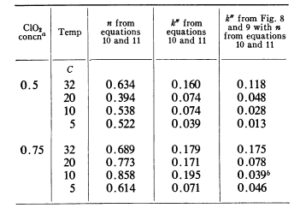
ข้อมูลที่ 0.25 มิลลิกรัม/ลิตร ไม่ได้ถูกนำมาพิจารณา เนื่องจากดูเหมือนว่าจะไม่เป็นไปตามกฎอัตรากำลัง
ข้อมูลที่น่าสงสัยนี้ไม่สอดคล้องกับแนวโน้มของอุณหภูมิ
ภาพที่ 8 ผลของอุณหภูมิที่มีต่อการฆ่าเชื้อด้วยคลอรีนไดออกไซด์ 0.75 มิลลิกรัมต่อลิตร
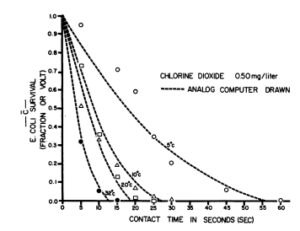
ภาพที่ 9 ผลของอุณหภูมิที่มีต่อการฆ่าเชื้อด้วยคลอรีนไดออกไซด์ 0.50 มิลลิกรัมต่อลิตร
งานวิจัยในอนาคตควรมีเป้าหมายเพื่อชี้แจงผลกระทบของการรวมความเข้มข้นของ C102 ในแบบจำลองจลนศาสตร์ต่อการปรับเส้นโค้งให้เข้ากับข้อมูล นอกจากนี้ ควรพิจารณาลำดับของปฏิกิริยาโดยสัมพันธ์กับความเข้มข้นเริ่มต้นของเซลล์ E. coli เพื่อตรวจสอบว่าสารตัวกลางของปฏิกิริยายับยั้งอัตราการฆ่าเชื้อหรือไม่ หรือว่ากลไกแบบเร่งปฏิกิริยาด้วยตนเองมีบทบาทสำคัญ ผลกระทบของอุณหภูมิที่รุนแรงที่สังเกตได้ในการศึกษานี้ได้ชี้ให้เห็นถึงลักษณะทางเคมีของอัตราการฆ่าเชื้อแล้ว ตรงข้ามกับขั้นตอนการควบคุมทางกายภาพล้วนๆ พลังงานกระตุ้น 12,000 แคลอรี/โมลนั้นสมเหตุสมผลอย่างแน่นอน หากสมมติฐานเรื่องลำดับของปฏิกิริยาที่แปรผันได้ไม่ส่งผลกระทบต่อ E ค่าของพลังงานกระตุ้นที่รายงานไว้ในที่นี้สะท้อนถึงพลังงานกระตุ้นที่แท้จริงได้ดีกว่าค่าที่รายงานโดยทั่วไปโดยอิงจากสมการจลนศาสตร์ต่อไปนี้:
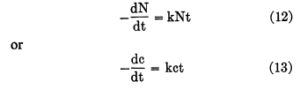
การศึกษาทางชีววิทยาเกี่ยวกับกลไก การพัฒนาแบบจำลองจลนศาสตร์นั้นตั้งอยู่บนสมมติฐานที่ว่าจลนศาสตร์อันดับ n เทียมสามารถอธิบายอัตราการเกิดปฏิกิริยาและการพึ่งพาอุณหภูมิได้ แบบจำลองนี้พยายามอธิบายกลไกโดยรวม อย่างไรก็ตาม ขั้นตอนแต่ละขั้นตอนที่ประกอบกันเป็นกลไกโดยรวมยังคงต้องได้รับการอธิบายให้กระจ่าง ด้วยเหตุนี้ จึงมีการพยายามค้นหาเส้นทางทางชีววิทยาที่ C102 ใช้ ซึ่งอาจอธิบายขั้นตอนที่ควบคุมอัตราได้
ความเร็วในการฆ่าเชื้อที่สั้นกว่าค่าที่รายงานไว้ก่อนหน้านี้มาก และคุณสมบัติการออกซิไดซ์ที่รุนแรงของ C102 ชี้ให้เห็นว่าการทำลายผนังเซลล์ของแบคทีเรียด้วยสารเคมีน่าจะเป็นกลไกหลัก หากผนังเซลล์ถูกทำลายอย่างรุนแรง โปรตีนและกรดนิวคลีอิกควรจะถูกปล่อยออกมาในตัวทำละลายในปริมาณที่เพียงพอที่จะทำให้เกิดยอดลักษณะเฉพาะในบริเวณ 260 และ 280 ไมโครเมตรในการวิเคราะห์ด้วยสเปกโทรโฟโตเมตรี เพื่อตรวจสอบข้อเท็จจริงของยอดโปรตีนและกรดนิวคลีอิก เซลล์ที่ล้างแล้วแต่ไม่ได้รับการบำบัดจะถูกทำลายด้วยกลไกในเครื่องกำเนิดคลื่นเสียง การตอบสนองมีขนาดใหญ่พอที่จะทำให้ปากกาหลุดออกจากกราฟ เมื่อเจือจางในอัตราส่วน 1:10 จะพบยอดที่ 260 และ 280 ไมโครเมตร ณ จุดนี้ จึงเติม C102 ลงในสารละลาย จากการวิเคราะห์เพิ่มเติม ไม่พบการเปลี่ยนแปลงใดๆ ในร่องรอยการทดลอง ซึ่งบ่งชี้ว่าไม่มีปฏิกิริยาที่สามารถพิสูจน์ได้ระหว่าง C102 โปรตีน หรือกรดนิวคลีอิก
เซลล์จำนวนมากถูกแขวนลอยในบัฟเฟอร์ฟอสเฟต OFD (pH 6.5) เซลล์เหล่านี้ถูกปั่นเหวี่ยงและล้างสามครั้ง เซลล์ที่ล้างแล้วได้รับการบำบัดด้วย C102 เป็นเวลา 5 นาที จากนั้นถูกปั่นเหวี่ยงจนเป็นตะกอน เหลือของเหลวใสอยู่ด้านบน ตัวอย่างของสารละลายใสถูกใส่ในคิวเวตต์ขนาด 10 ซม. เพื่อทำการวิเคราะห์ความยาวของเส้นทางแสงที่เพิ่มขึ้นทำให้ความไวเพิ่มขึ้น 10 เท่า การไม่มีจุดสูงสุดของการดูดกลืนแสงในบริเวณ 260 และ 280 mA บ่งชี้ว่าโปรตีนและกรดนิวคลีอิกไม่ได้ถูกปล่อยออกมาจากเซลล์ สรุปได้ว่า C102 ไม่ทำให้เกิดการรั่วไหลของสารภายในเซลล์ และเห็นได้ชัดว่าไม่ได้ออกซิไดซ์สารโปรตีนให้กลายเป็นผลิตภัณฑ์อื่น ในช่วงเวลานี้ เราได้เรียนรู้เกี่ยวกับงานของ Bringmann ซึ่งรายงานในปี 1953 ซึ่งแสดงให้เห็นผ่านภาพถ่ายอิเล็กตรอนไมโครสโคปว่าไม่มีการเปลี่ยนแปลงที่มองเห็นได้ ในความสมบูรณ์ของผนังเซลล์เกิดขึ้นกับเซลล์ที่ได้รับการบำบัดด้วยคลอรีน
จากนั้นเส้นโค้งการฆ่าเชื้อของเราก็ถูกนำเสนอต่อ Robert J. Kuchler ภาควิชาแบคทีริโอวิทยา มหาวิทยาลัยรัตเกอร์ส เขาแนะนำว่าการทำลายใน 5 ถึง 10 วินาทีนั้นเป็นเวลาประมาณเดียวกับที่จำเป็นสำหรับการสังเคราะห์โปรตีน และรอยโรคที่ทำให้ตายในช่วงเวลานั้นอาจเกิดจากการโจมตีเป้าหมายหลัก เช่น การสังเคราะห์โปรตีน Haggis ตั้งข้อสังเกตว่าการสังเคราะห์โมเลกุลฮีโมโกลบินหนึ่งโมเลกุลต้องใช้เวลา 5 ถึง 10 วินาที
เพื่อทดสอบสมมติฐานที่ว่าการสังเคราะห์โปรตีนอาจเกี่ยวข้องฟีนิลอะลานีนที่ติดฉลาก 4C ถูกเติมลงในอาหารเลี้ยงเชื้อขั้นต่ำที่จำเป็นของ Braun (MEM) สำหรับ E. coli ซึ่งมีเซลล์ประมาณ 109 เซลล์ ในอ่างน้ำแข็ง จากนั้นจึงนำไปวางในอ่างน้ำ 37 องศาเซลเซียสทันทีและปล่อยให้บ่ม ในช่วงเวลาต่างๆ จะนำตัวอย่างออกมาและเติมลงในกรดไตรคลอโรอะซิติกที่ร้อนเพื่อตกตะกอนโปรตีน จากนั้นจึงเติมคลอรีนไดออกไซด์ลงในระบบ และนำตัวอย่างออกมาอีกครั้งในช่วงเวลาต่างๆ เพื่อเติมลงในกรดไตรคลอโรอะซิติก จำนวนโปรตีนที่มี 4C แสดงให้เห็นความแตกต่างอย่างมาก ในการสังเคราะห์โปรตีนระหว่างเซลล์ที่ได้รับการรักษาด้วย C102 และ MEM
เพื่อยืนยันข้อสังเกตนี้อย่างแน่ชัด จึงได้ทำการทดลองครั้งที่สอง ในครั้งนี้ ได้เติมวาไลน์ที่ติดฉลาก 4C ลงในเซลล์ในอ่างน้ำแข็ง เพื่อให้ได้ข้อมูลที่มีความหมายเกี่ยวกับอัตราการสังเคราะห์โปรตีน ทั้งที่มีและไม่มีการรักษาด้วย C102 จึงได้ออกแบบอุปกรณ์ที่อนุญาตให้ดึงตัวอย่างออกมาทุกๆ 10 วินาที จากผลการทดลองนี้ (ภาพที่ 10) เห็นได้ชัดว่า C102 ยับยั้งการสังเคราะห์โปรตีนอย่างมาก และเห็นได้ชัดว่าเกิดขึ้นอย่างฉับพลัน ไม่พบช่วงเวลาหน่วง สิ่งนี้บ่งชี้ว่าความเสียหายร้ายแรงเกี่ยวข้องโดยตรงกับการสังเคราะห์โปรตีน มากกว่าการทำให้ระบบเอนไซม์ในกระบวนการสลายกลูโคสไม่ทำงาน ซึ่งในกรณีนั้น จะมีการสังเคราะห์โปรตีนได้เพียงพอที่จะทำให้เกิดช่วงเวลาหน่วง
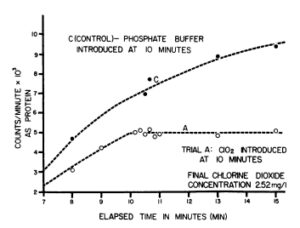
ภาพที่ 10 ผลกระทบของคลอรีนไดออกไซด์ต่อการสังเคราะห์โปรตีน
มีความเป็นไปได้หลายประการ เช่น การยับยั้งการก่อตัวของอะมิโนเอซิลอะดีนิเลต หรือการยับยั้งการกระตุ้นกรดอะมิโน ขั้นตอนทั้งสองนี้อาจถือได้ว่าเป็นความเป็นไปได้หนึ่งอย่าง และจะแสดงได้ดังนี้:

อาจเกิดจากการยับยั้งการทำงานของ mRNA ซึ่งป้องกันการแปลข้อมูลที่เข้ารหัสคำอธิบายที่สี่ที่ดูเหมือนจะเป็นเชิงโครงสร้างมากกว่าเชิงหน้าที่ คือ การทำลายไรโบโซมโดย C102 อย่างไรก็ตาม การพิจารณาภาพที่ 10 ทำให้ตัดความเป็นไปได้นี้ออกไป การทำลายไรโบโซมควรทำให้จำนวนลดลงเนื่องจากสารภายในเซลล์รั่วไหลเข้าสู่ตัวทำละลายโดยรอบ ดังนั้น การยับยั้งกระบวนการทำงานจึงดูเหมือนเป็นไปได้มากที่สุด
การทดลองสำคัญที่ต้องดำเนินการในขณะนี้เพื่อพิสูจน์โดยตรงอย่างแน่ชัดถึงตำแหน่งของรอยโรคที่ร้ายแรงนั้น จำเป็นต้องใช้ระบบที่ปราศจากเซลล์ โดยใช้ไรโบโซมที่ได้จากโฮโมจีเนตที่ถูกทำลายของ E. coli การทดลองนี้กำลังดำเนินการอยู่ และจะรายงานผลในวันหนึ่งในภายหลัง
มีการดำเนินการขั้นหนึ่งเพื่อกำหนดผลกระทบของ C102 ต่อส่วนประกอบของเซลล์ที่เกี่ยวข้องกับการสังเคราะห์โปรตีน และสามารถรายงานได้ในขณะนี้ กรดอะมิโนทั้งหกชนิด (ฮิสติดีน แอสพาราจีน ฟีนิลอะลานีน อาร์จินีน โพรลีน และลิวซีน) ถูกบำบัดด้วย C102 เป็นเวลา 30 นาที นำตัวอย่างออกมาและหยดลงบนกระดาษกรอง Whatman หมายเลข 1 (ขนาด 8 x 8 นิ้ว) โครมาโทแกรมถูกพัฒนาในห้องแซนด์วิชของ Eastman ด้วยบิวทานอล-กรดอะซิติก-น้ำ (4:1:5) ตรวจจับกรดอะมิโนด้วยนินไฮดริน 0.5% ในบิวทานอล ตัวอย่างกรดอะมิโนแต่ละชนิดที่ไม่ได้รับการบำบัดถูกวางบนกระดาษกรองข้างๆ ตัวอย่างที่ได้รับการบำบัด จากจุดที่สังเกตได้ทั้งกรดอะมิโนที่ผ่านการบำบัดและไม่ผ่านการบำบัด พบว่าขนาด สี และความเข้มค่อนข้างคล้ายกัน
นอกจากนี้ ค่า RF ก็ดูเหมือนจะเท่ากัน ชุดกรดอะมิโนชุดที่สองได้รับการบำบัดด้วย C102 และตัวอย่างถูกนำออกมาทุกๆ 30 วินาที เป็นเวลา 5 นาที เนื่องจาก C102 ระเหยได้ จึงไม่มีสารตกค้างบนกระดาษหลังจากจุดแห้งแล้ว อีกครั้ง ค่า RF ขนาด ความเข้ม และสีของจุดไม่เปลี่ยนแปลงตามเวลา จากชุดการทดลองนี้ สรุปได้ว่า C102 ดูเหมือนจะไม่ทำปฏิกิริยากับกรดอะมิโนมากพอที่จะเปลี่ยนแปลงโครงสร้างลักษณะเฉพาะของพวกมัน ดังนั้น เราจึงไม่คาดหวังว่าจะมีปฏิกิริยาของกรดอะมิโนที่ปราศจาก C102 ภายในเซลล์ ซึ่งเป็นการตัดความเป็นไปได้นี้ออกไปในฐานะสาเหตุของการยับยั้งการสังเคราะห์โปรตีน
เราเชื่อว่าความสามารถในการเก็บตัวอย่างทุกๆ 5 วินาที ร่วมกับตัวทำละลายที่ปราศจากสารอินทรีย์ ทำให้เราสามารถสังเกตเห็นการทำลายแบคทีเรียที่รวดเร็วเป็นพิเศษ ซึ่งนำไปสู่การทดลองหลายชุดที่ระบุกลไกการฆ่าเชื้อของ C102 เราเชื่อว่านี่เป็นครั้งแรกที่มีการสาธิตเรื่องนี้ และหวังว่านักวิจัยคนอื่นๆ จะทำการศึกษาในสาขาการวิจัยด้านการฆ่าเชื้อที่สำคัญนี้ต่อไป
กิตติกรรมประกาศ
เราขอแสดงความขอบคุณสำหรับการคำนวณแบบอนาล็อกที่ดำเนินการโดย A. F. Burkart และ R. W. Bradshaw ภาควิชาวิศวกรรมเคมี
การวิจัยนี้ได้รับการสนับสนุนโดยเงินทุนที่ไม่จำกัดจาก Olin Corp. และโดยทุนฝึกอบรมบริการสาธารณสุข PHT-1-61A
เอกสารอ้างอิง
1. BENARDE, M. A., B. M. ISRAEL, V. P. OLIVIERI, และ M. L. GRANSTROM. 1965. ประสิทธิภาพของคลอรีนไดออกไซด์ในฐานะสารฆ่าเชื้อแบคทีเรีย Appl. Microbiol. 13:776-780.
2. BRAUN, W. 1953. พันธุศาสตร์ของแบคทีเรีย W. B.Saunders & Co., London.
3. BRINGMANN, G. 1953. ผลการศึกษาด้วยกล้องจุลทรรศน์อิเล็กตรอนเกี่ยวกับการออกฤทธิ์ของคลอรีน โบรมีน ไอโอดีน ทองแดง เงิน และไฮโดรเจนเปอร์ออกไซด์ต่อ E. coli. Z. Hyg. Infektionskrankh. 138:155-166.
4. CHICK, H. 1908. การตรวจสอบกฎของการฆ่าเชื้อโรค. J. Hyg. 8:92-157.
5. GREEN, D. C. และ P. K. STUMPF. 1946. บันทึกเกี่ยวกับวิธีการทางเอนไซม์ในการประมาณค่าคลอรีน.J. Am. Water Works Assoc. 38:1306-1308.
6. HAGGIS, G. H. [บรรณาธิการ]. 1965. บทนำสู่ชีววิทยาระดับโมเลกุล การสังเคราะห์โปรตีน (บทที่12). John Wiley & Sons, Inc., ลอนดอน.
7. KNOX, W. E., P. K. STUMPF, D. E. GREEN และ V. H. AUERBACH. 1948. การยับยั้งเอนไซม์ซัลฟ์ไฮดริลเป็นพื้นฐานของการออกฤทธิ์ฆ่าเชื้อแบคทีเรียของคลอรีน. เจ.แบคทีริโอล. 55:451-458.
8. KRONIG, B. และ T. PAUL. 1897. พื้นฐานทางเคมีสำหรับทฤษฎีปฏิกิริยาพิษ และการฆ่าเชื้อโรค Z. Hyg. Infektionskrankh.25:1-112.
9. MADSEN, T. และ M. NYMAN. 1907. เกี่ยวกับทฤษฎีของการฆ่าเชื้อโรค I. Z. Hyg. Infektionskrankh.57:388-404.
10. WYss, 0. 1961. แง่มุมทางทฤษฎีของการฆ่าเชื้อโรค โดยคลอรีน Proc. Rudolfs Research Conf. อันตรายต่อสุขภาพของประชาชนจากมลพิษจุลินทรีย์ของน้ำ Rutgers – The State Univ., New Brunswick, N.J., หน้า 400-418.