หน้าหลักนี้ประกอบด้วยเอกสารฉบับแปลของบทความวิชาการต้นฉบับ อย่างไรก็ตาม เรา ได้จัดทำสรุปเนื้อหาที่สำคัญแบบย่อยง่ายไว้ให้ผู้อ่านได้ศึกษาเป็นลำดับแรก เพื่อให้เข้าใจภาพรวมของงานวิจัยชิ้นนี้ได้อย่างรวดเร็ว หากท่านมีความสนใจในรายละเอียดเชิงลึกหรือข้อมูลทางสถิติเพิ่มเติม ท่านสามารถเลือกอ่านเอกสารฉบับเต็มได้ทั้งในรูปแบบภาษาอังกฤษ (Original) ได้ที่ลิงก์นี้: https://www.sciencedirect.com/science/article/pii/S0891584923005014หรือหากต้องการอ่านฉบับภาษาไทย (Translated) เราได้จัดทำบทแปลไว้ให้แล้วในหน้านี้ (ล่างสุด)
บทความวิจัยเรื่องนี้ นำเสนอแนวคิดว่า ความเป็นพิษของโปรตีนหนาม (Spike Protein) ทั้งจากการติดเชื้อ SARS-CoV-2 และจากวัคซีน มีกลไกสำคัญมาจาก “ปรากฏการณ์การสลับสภาวะรีดอกซ์” (Redox Shift) ซึ่งส่งผลให้เซลล์เกิดความผิดปกติในการเผาผลาญ พลังงานในไมโตคอนเดรียลดลง และเกิดภาวะที่เรียกว่า “Warburg Effect” (การเปลี่ยนไปใช้กระบวนการสร้างพลังงานแบบไม่ใช้ออกซิเจนแม้จะมีออกซิเจนเพียงพอ) ภาวะดังกล่าวทำให้เซลล์เปลี่ยนจากกระบวนการสลาย (Catabolism) ไปสู่กระบวนการสร้าง (Anabolism) อย่างต่อเนื่อง นำไปสู่การอักเสบเรื้อรัง กลุ่มอาการพายุไซโตไกน์ (Cytokine Storm) และความเหนื่อยล้าเรื้อรัง
โดยคณะผู้วิจัยได้เสนอแนวทางการรักษาใหม่โดยการใช้สารที่ช่วยปรับสมดุลรีดอกซ์และกระตุ้นการทำงานของไมโตคอนเดรีย เช่น เมทิลีนบลู (Methylene Blue), กรดอัลฟาไลโปอิก (Alpha Lipoic Acid) และคลอรีนไดออกไซด์ (Chlorine Dioxide) เพื่อช่วยย้อนกลับกระบวนการที่ผิดปกติและลดผลกระทบระยะยาวจากโปรตีนหนาม
ข้อมูลการเผยแพร่
-
ชื่อบทความ: Toxicity of the spike protein of COVID-19 is a redox shift phenomenon: A novel therapeutic approach
-
วารสารที่ตีพิมพ์: Free Radical Biology and Medicine, เล่มที่ 206, หน้า 106–110 (ปี 2023)
-
ผู้เขียน: 1. Laurent Schwartz (Assistance Publique des Hôpitaux de Paris, ฝรั่งเศส) 2. Manuel Aparicio-Alonso (Centro Médico Jurica, เม็กซิโก) 3. Marc Henry (Université de Strasbourg, ฝรั่งเศส) 4. Miroslav Radman (Mediterranean Institute for Life Sciences, โครเอเชีย) 5. Romain Attal (Cité des Sciences et de l’Industrie, ฝรั่งเศส) 6. Ashraf Bakkar (October University for Modern Sciences and Arts, อียิปต์)
ข้อมูลบทความ
คำสำคัญ
โปรตีนสไปค์, เมทิลีนบลู, ศักยภาพรีดอกซ์, โควิด-19 ระยะยาว, คลอรีนไดออกไซด์
บทคัดย่อ
ก่อนหน้านี้เราได้แสดงให้เห็นแล้วว่าโรคส่วนใหญ่แสดงให้เห็นถึงรูปแบบของการสร้างสารเนื่องจากความบกพร่องของไมโตคอนเดรีย: ในโรคมะเร็ง จะมีการสร้างเซลล์ลูก ในโรคอัลไซเมอร์ จะมีการสร้างคราบอะไมลอยด์ ในการอักเสบ จะมีการสร้างไซโตไคน์และลิมโฟไคน์ การติดเชื้อโควิด-19 มีรูปแบบที่คล้ายคลึงกัน ผลกระทบระยะยาว ได้แก่ การเปลี่ยนแปลงของปฏิกิริยาออกซิเดชัน-รีดักชัน และการสร้างสารในเซลล์อันเป็นผลมาจากปรากฏการณ์วาร์เบิร์กและการทำงานผิดปกติของไมโทคอนเดรีย การสร้างสารอย่างต่อเนื่องนี้จะนำไปสู่พายุไซโตไคน์ ความเหนื่อยล้าเรื้อรัง การอักเสบเรื้อรัง หรือโรคทางระบบประสาทเสื่อม ยาเช่น กรดไลโปอิก และเมทิลีนบลู ได้แสดงให้เห็นว่าสามารถเพิ่มกิจกรรมของไมโทคอนเดรีย บรรเทาปรากฏการณ์วาร์เบิร์ก และเพิ่มการสลายสาร ในทำนองเดียวกัน การใช้เมทิลีนบลู คลอรีนไดออกไซด์ และกรดไลโปอิกร่วมกันอาจช่วยลดผลกระทบระยะยาวของโควิด-19 โดยการกระตุ้นการสลายสาร
ผู้ป่วยโควิด-19 อาจประสบกับภาวะแทรกซ้อนหลังระยะเฉียบพลัน และอาการบางอย่างอาจคงอยู่เป็นเวลาหลายเดือน อาการเหล่านี้อาจเป็นผลมาจากภาวะขาดออกซิเจนที่เกิดจากโควิด-19 การลดลงของปริมาณเลือดที่หัวใจสูบฉีด อาการปวดกล้ามเนื้อ หรืออาการที่คล้ายกับโรคไข้สมองอักเสบหรือกลุ่มอาการอ่อนเพลียเรื้อรัง ผลข้างเคียงระยะยาวอื่นๆ อาจรวมถึงภาวะแทรกซ้อนของระบบหัวใจและหลอดเลือด เช่น โรคหลอดเลือดสมองหรือกล้ามเนื้อหัวใจตาย โรคอัลไซเมอร์ โรคครอยซ์เฟลด์-จาคอบ และมะเร็ง ในบทความนี้ เราเสนอแนะอย่างยิ่งว่าอาการเหล่านี้เป็นผลโดยตรงจากความไม่สมดุลของรีดอกซ์ ซึ่งเป็นผลมาจากการลดลงของผลผลิตพลังงานโดยไมโตคอนเดรีย
ก่อนหน้านี้เราได้แสดงให้เห็นแล้วว่าการเปลี่ยนแปลงทางเมตาบอลิซึมมีบทบาทสำคัญในโรคต่างๆ มีความผิดปกติของไมโตคอนเดรียอย่างเห็นได้ชัดและระดับแลคเตทที่เพิ่มขึ้น ซึ่งเป็นลักษณะสำคัญของการเปลี่ยนแปลงการเผาผลาญและปรากฏการณ์วาร์เบิร์กในหลายโรค ในโรคมะเร็ง การเปลี่ยนแปลงการเผาผลาญพลังงานถือเป็นลักษณะเด่นที่รู้จักกันดี มีรายงานข้อมูลการทดลองที่ชัดเจนในโรคอื่นๆ เช่น โรคหัวใจ โรคภูมิต้านตนเองบางชนิด โรคอัลไซเมอร์ และโรคพาร์กินสัน สุดท้ายนี้ พบว่ากิจกรรมของแลคเตทดีไฮโดรจีเนส (LDH) เพิ่มขึ้นในผู้ป่วย COVID-19 และอาจกระตุ้นไกลโคไลซิส คล้ายกับปรากฏการณ์วาร์เบิร์ก เพื่อเปลี่ยนทิศทางเชื้อเพลิงและผลิตสารตัวกลางอะนาโบลิก ดังนั้น เกือบทุกโรคจึงมีอะนาโบลิซึมเพิ่มขึ้น
เพื่อรักษาสภาวะสมดุล เซลล์ของเราต้องปลดปล่อยเอนโทรปีออกมา ไม่ว่าจะเป็นในรูปของ CO2, H2O และความร้อน (แคตาโบลิซึม) หรือในรูปของโมเลกุลขนาดใหญ่ (อะนาโบลิซึม) ดังนั้น การแบ่งเซลล์จึงเป็นวิธีที่ซับซ้อนที่สุดในการปลดปล่อยเอนโทรปี การเปลี่ยนจากแคตาโบลิซึมไปสู่อะนาโบลิซึมนั้นเกิดจากการเปลี่ยนแปลงของรีดอกซ์ ซึ่งวัดได้จากอัตราส่วนที่สูงขึ้นของ [NADH]/[NAD+], [NADPH]/[NADP+] หรือ
[FADH2]/[FAD]
เป้าหมายของบทความนี้คือการตั้งสมมติฐานว่าภาวะแทรกซ้อนระยะสั้นและระยะยาวของโควิด-19 เป็นผลมาจากการเปลี่ยนแปลงของปฏิกิริยาออกซิเดชัน-รีดักชันและการสร้างสารในลักษณะเดียวกัน อันเนื่องมาจากสภาพแวดล้อมของเซลล์ที่ลดลงซึ่งเกิดจากโปรตีนหนามของไวรัสแต่เดิม
1. การจับกันของโปรตีนหนามกับเอนไซม์แองจิโอเทนซินคอนเวอร์ติงเอนไซม์ 2 (ACE2) เป็นปรากฏการณ์รีดอกซ์
เพื่อเริ่มต้นการติดเชื้อ โปรตีนหนามของไวรัสจะจับกับตัวรับ ACE2 ของเซลล์เจ้าบ้าน ได้มีการพิสูจน์แล้วว่าโปรตีน S และ ACE2 มีพันธะไดซัลไฟด์ภายในโมเลกุลและมีหมู่ซิสเทอีน (Cys) จำนวนมาก เมื่อพันธะไดซัลไฟด์ของทั้ง ACE2 และโปรตีนหนามของ SARS-CoV-2 ซึ่งจับกับ ACE2 ถูกแปลงเป็นกลุ่มไทออล พบว่าความสามารถในการจับลดลงอย่างมาก โปรตีนหนามมีหมู่ซิสเทอีน 40 หมู่ ซึ่งบางส่วนช่วยเสริมความเสถียรของการเชื่อมต่อกับตัวรับ ACE2 ของโฮสต์ พบว่าคู่ Cys480-Cys488 ของโปรตีนหนามมีส่วนเกี่ยวข้องโดยตรงในการจับกับตัวรับ ACE2 หมู่ซิสเทอีนเฉพาะของโปรตีน ACE2 ของโฮสต์ยังมีบทบาทสำคัญในการโต้ตอบระหว่างโปรตีนทั้งสองด้วย ที่ส่วนต่อประสานไดเมอร์ Cys133 และ Cys141 สร้างพันธะไดซัลไฟด์ซึ่งเกี่ยวข้องกับความไวต่อ COVID-19
หมู่ซิสเทอีน (Cys) ในโปรตีน S และ ACE2 มีอยู่มากมาย ซึ่งมีส่วนร่วมในพันธะไดซัลไฟด์ภายในโมเลกุล เมื่อพันธะไดซัลไฟด์ทั้งหมดของ ACE2 และโปรตีนหนามของ SARS-CoV/CoV-2 ถูกแปลงเป็นกลุ่มไทออล ความสัมพันธ์ในการจับตัวจะลดลงอย่างมาก ดังนั้นพันธะไดซัลไฟด์ภายในโมเลกุลจึงมีความสำคัญ ในความเป็นจริง การมีอยู่ของไดซัลไฟด์ที่มีฤทธิ์รีดอกซ์ใน ACE2 ซึ่งเป็นโดเมนการโต้ตอบของโปรตีน S และบริเวณพับคล้ายเฟอร์เรดอกซินใน ACE2 ชี้ให้เห็นอย่างชัดเจนว่าสมดุลรีดอกซ์มีบทบาทสำคัญในการพัฒนาและความรุนแรงของ COVID-19
2. โควิด-19 มีความรุนแรงมากขึ้นในสภาพแวดล้อมที่จำกัด เช่น ในผู้สูงอายุ
รูปแบบที่รุนแรงของโควิด-19 มักจำกัดอยู่ในกลุ่มประชากรย่อยที่กำหนดไว้อย่างชัดเจน ผู้ที่มีความเสี่ยงสูง ได้แก่ ผู้สูงอายุ ผู้ป่วยที่เป็นโรคเมตาบอลิกซินโดรม เช่น โรคอ้วน หรือผู้ที่เป็นโรคเรื้อรัง เช่น มะเร็งหรือการอักเสบ การสูงอายุเกี่ยวข้องกับการควบคุมสมดุลของรีดอกซ์ที่ไม่ดี เช่น ภาวะสมดุลของไทออล/ไดซัลไฟด์ของอวัยวะทั้งหมด ซึ่งนำไปสู่การเพิ่มขึ้นของเส้นทางการอักเสบและพังผืด
ยิ่งไปกว่านั้น การลดลงของสมดุลไทออล/ไดซัลไฟด์ตามอายุจะยิ่งรวดเร็วขึ้นในโรคอักเสบและโรคแก่ก่อนวัย สิ่งนี้อธิบายได้บางส่วนถึงสภาพแวดล้อมภายนอกเซลล์ที่ลดลงในผู้สูงอายุและความเสี่ยงต่อการติดเชื้อโควิด-19 ที่เพิ่มขึ้น
3. พายุไซโตไคน์เป็นปรากฏการณ์รีดอกซ์
การตอบสนองการอักเสบเฉียบพลันที่ควบคุมได้นั้นจำเป็นต่อการต่อสู้กับการติดเชื้อ อย่างไรก็ตาม หากกระบวนการอักเสบกลายเป็นเรื้อรัง อาจนำไปสู่ผลเสียทั้งในระดับท้องถิ่นและทั่วร่างกาย เนื้อเยื่อที่อักเสบจะมีระดับของสารออกซิเจนที่ว่องไว (ROS) และสารไนโตรเจนที่ว่องไว (RNS) สูงขึ้น ซึ่งเกิดขึ้นระหว่างการระเบิดของการหายใจของเซลล์ภูมิคุ้มกัน การส่งสัญญาณรีดอกซ์จะปรับการตอบสนองการอักเสบอย่างเข้มงวด และความเครียดจากออกซิเดชันได้รับการรายงานในผู้ป่วยโควิด-19 เฉียบพลัน
มีหลักฐานจำนวนมากที่บ่งชี้ว่าความไม่สมดุลของ iMeBalance ในเส้นทางการส่งสัญญาณรีดอกซ์อาจมีส่วนทำให้เกิดการติดเชื้อและการพัฒนาของพายุไซโตไคน์ในผู้ป่วย COVID-19 เนื่องจากการส่งสัญญาณรีดอกซ์มีบทบาทสำคัญในการควบคุมการทำงานของภูมิคุ้มกัน และการอักเสบ และการหยุดชะงักของการส่งสัญญาณนี้อาจนำไปสู่การผลิตไซโตไคน์มากเกินไปและการกระตุ้นระบบภูมิคุ้มกัน นอกจากนี้ การศึกษายังพบว่าผู้ป่วย COVID-19 ที่มีอาการรุนแรง มีระดับของตัวบ่งชี้ความเครียดออกซิเดชันสูงกว่าและระดับสารต้านอนุมูลอิสระต่ำกว่า ยิ่งไปกว่านั้น ความเครียดออกซิเดชันสามารถกระตุ้น NLRP3 อินฟลามาโซม ซึ่งเป็นโปรตีนเชิงซ้อนที่มีบทบาทสำคัญในพายุไซโตไคน์
สมดุลรีดอกซ์และการอักเสบเป็นกระบวนการที่ขึ้นต่อกัน การอักเสบนำไปสู่การก่อตัวของ ROS และ RNS ในขณะที่สมดุลรีดอกซ์ส่งผลให้เกิดความเสียหายต่อเซลล์ ซึ่งจะกระตุ้นให้เกิดการตอบสนองต่อการอักเสบ การบาดเจ็บของเซลล์เยื่อบุผนังหลอดเลือดใน COVID-19 ทำให้เกิดการบาดเจ็บที่ปอด โรคหลอดลมตีบ และการอักเสบเรื้อรัง เส้นทางการอักเสบเหล่านี้ถูกควบคุมโดยไมโทคอนเดรียของเยื่อบุผนังหลอดเลือดผ่าน mtROS อย่างไรก็ตาม mtROS ที่สูงขึ้นอย่างต่อเนื่องจะกระตุ้นการทำงานผิดปกติของเยื่อบุผนังหลอดเลือดและการอักเสบ ซึ่งส่งผลให้เกิดวงจรที่เลวร้ายที่เกี่ยวข้องกับ ROS การอักเสบ และการทำงานผิดปกติของไมโทคอนเดรีย ไมโทคอนเดรียที่เสียหายซึ่งปล่อย ROS จะกระตุ้นการอักเสบผ่าน NLRP3 inflammasome ซึ่งมีส่วนร่วมในการปล่อย IL-1β และ IL-18
ระดับไทออลลดลงในซีรั่มของผู้ป่วยโควิด-19 ซึ่งนำไปสู่การสะสมของ ROS และ RNS โดยการเหนี่ยวนำให้เกิดความผิดปกติของไมโทคอนเดรียและการผลิตไซโตไคน์ที่ก่อให้เกิดการอักเสบ ไซโตไคน์เหล่านี้ทำหน้าที่เป็นโมเลกุลส่งสัญญาณเพื่อดึงดูดเซลล์ภูมิคุ้มกันไปยังบริเวณที่มีการอักเสบและกระตุ้นการสร้างอนุมูลอิสระ ตัวอย่างเช่น IFNɤ, IL-1ẞ, IL-6 และ TNFα สามารถกระตุ้นการสร้างไนตริกออกไซด์ (NO) ได้ทั้งหมด ไซโตไคน์เหล่านี้ถูกหลั่งออกมาเนื่องจากสภาพแวดล้อมที่ลดลงในระหว่างพายุไซโตไคน์ IL-2 มีการควบคุมขึ้นอย่างมากในผู้ป่วยโควิด-19 และ IL-2 เป็นที่ทราบกันดีว่ากระตุ้นการสร้าง NO ในผู้ป่วยอย่างมีนัยสำคัญ กรดไนตริกยังเป็นตัวกลางสำคัญของภาวะความดันโลหิตต่ำที่เกิดจาก IL-2 และกลุ่มอาการหลอดเลือดรั่ว
นอกจากนี้ ความผิดปกติของไมโทคอนเดรียยังเชื่อมโยงกับการเกิดโรคโควิด-19 แท้จริงแล้ว ความผิดปกติของไมโทคอนเดรียที่เกิดจาก SARS-CoV-2 นำไปสู่ความเสียหายต่อไมโทคอนเดรีย เมื่อการสลายตัวลดลง เอนโทรปีจะถูกปล่อยออกมาผ่านการสร้างใหม่ การติดเชื้อ SARS-CoV-2 ในเม็ดเลือดขาวนำไปสู่การลดลงของการฟอสโฟรีเลชันแบบออกซิเดทีฟ ระดับแลคเตทที่สูงขึ้น ซึ่งเป็นลักษณะเฉพาะของปรากฏการณ์วาร์เบิร์ก ก็มีรายงานพบในผู้ป่วยโควิด-19 ที่มีความเสี่ยงสูงเช่นกัน
4. ภาวะแทรกซ้อนระยะยาวจากโควิด-19
โควิด-19 ก่อให้เกิดหรือทำให้ภาวะหัวใจเสียหายในผู้ป่วยที่ติดเชื้อรุนแรงขึ้นผ่านทางพายุไซโตไคน์, ภาวะเยื่อบุหลอดเลือดผิดปกติ, ภาวะหลอดเลือดอุดตัน หรือภาวะเม็ดเลือดขาวต่ำ การชันสูตรศพผู้ป่วยโควิด-19 พบการแทรกซึมของเซลล์เม็ดเลือดขาวชนิดโมโนนิวเคลียร์ที่ก่อให้เกิดการอักเสบในกล้ามเนื้อหัวใจ ซึ่งยืนยันบทบาทของระบบภูมิคุ้มกันในการทำให้เกิดความเสียหายต่อระบบหัวใจและหลอดเลือดอันเป็นผลมาจากการติดเชื้อโควิด-19
การตอบสนองต่อการอักเสบ ร่วมกับผลกระทบโดยตรงของ SARS ต่ออวัยวะต่างๆ ผ่านทาง ACE2 มีความเกี่ยวข้องกับภาวะไตวาย ความเสียหายต่อตับ และภาวะอวัยวะล้มเหลวหลายระบบ ความเสียหายเฉียบพลันต่อปอดอาจตามมาด้วยภาวะพังผืดในปอดและการทำงานของปอดบกพร่องเรื้อรัง นอกจากนี้ ยังพบว่าการติดเชื้อ SARS-CoV-2 ส่งผลกระทบต่อระบบประสาทส่วนกลางและส่วนปลาย และทำลายเซลล์ประสาท นำไปสู่ภาวะแทรกซ้อนทางระบบประสาทในระยะยาว รวมถึงโรคอัลไซเมอร์ โรคพาร์กินสัน และโรคปลอกประสาทเสื่อมแข็ง
ผลที่ตามมาทั่วไปของ Covid-19 ดูเหมือนจะเป็นอาการอ่อนเพลียเรื้อรัง ซึ่งเป็นโรคทั่วไปที่มีลักษณะเฉพาะคือผลผลิตพลังงานของไมโทคอนเดรียลดลงเนื่องจากฟอสโฟริเลชันแบบออกซิเดชันลดลง ตัวบ่งชี้ความเครียดรีดอกซ์หลายตัว เช่น ระดับสารต้านอนุมูลอิสระที่ต่ำลงและระดับเปอร์ออกไซด์และซูเปอร์ออกไซด์ที่สูงขึ้น มีความเชื่อมโยงกับความรุนแรงของอาการในอาการอ่อนเพลียเรื้อรัง ตัวบ่งชี้เหล่านี้ของความสมดุลรีดอกซ์ยังมีความสัมพันธ์กับความรุนแรงของอาการและระดับกรดแลคติกในโพรงสมองที่สูงขึ้นซึ่งสอดคล้องกับความเครียดออกซิเดชัน การเผาผลาญในสมองลดลง คล้ายกับโรคอัลไซเมอร์ ก็สามารถพบได้เช่นกัน มีการเพิ่มขึ้นของระดับกรดแลคติกในเลือดพร้อมกัน ซึ่งเป็นลักษณะเฉพาะของฟอสโฟริเลชันแบบออกซิเดชันที่ลดลง ศักยภาพของเยื่อหุ้มไมโทคอนเดรีย (ΔΨm) เป็นพารามิเตอร์ที่มักใช้เพื่อกำหนดการทำงานของไมโทคอนเดรีย การลดลงของ ΔΨm มีส่วนเกี่ยวข้องกับโรคที่เกี่ยวข้องกับการอักเสบหลายชนิด มีการลดลงของ ΔΨm ในเม็ดเลือดขาวจากผู้ป่วย Covid-19
ผู้คนจำนวนมากได้รับการฉีดวัคซีน RNA หรือ DNA ซึ่งกระตุ้นการสังเคราะห์โปรตีนหนามของไวรัสในเซลล์มนุษย์ หลายคนประสบกับอาการคล้าย COVID-19 (ลิ่มเลือด การอักเสบรุนแรง การทำลายเนื้อเยื่อ และภาวะอวัยวะล้มเหลว) Xing et al., 2021 ได้ทบทวนการศึกษา 10 เรื่องที่ประเมินผลข้างเคียงระยะสั้นของการฉีดวัคซีน ปฏิกิริยาไม่พึงประสงค์ส่วนใหญ่มีระดับความรุนแรงเล็กน้อยถึงปานกลางและหายไปภายใน 24 ชั่วโมงหลังการฉีดวัคซีน ปฏิกิริยาไม่พึงประสงค์ทางระบบที่พบบ่อยที่สุดคืออาการอ่อนเพลีย มีไข้ หรือปวดเมื่อยตามร่างกาย
แม้ว่าวัคซีนโควิด-19 ที่พัฒนาขึ้นใหม่ควรจะได้รับการพิสูจน์แล้วว่าปลอดภัย แต่บางคนก็ประสบกับผลข้างเคียง ส่วนใหญ่เป็นอาการที่ไม่ร้ายแรง เช่น เวียนศีรษะ อาเจียน หรือมีไข้ชั่วคราว ผลข้างเคียงอื่นๆ ได้แก่ การกระตุ้นการทำงานของไวรัสอีกครั้งในไวรัสอีสุกอีใส หรือตับอักเสบ ภาวะเลือดแข็งตัวผิดปกติ และส่งผลให้เกิดโรคหลอดเลือดสมองและกล้ามเนื้อหัวใจอักเสบหลังจากการฉีดวัคซีนทั้งแบบ DNA และวัคซีนแบบ RNA
ตารางที่ 1 ผลของการรักษาภาวะการเปลี่ยนแปลงรีดอกซ์ด้วยยาที่มุ่งเป้าไปที่ผลของวาร์เบิร์กในโรคต่างๆ
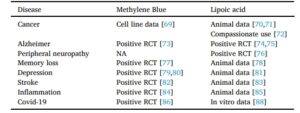
NA: ไม่มีข้อมูล, RCT: การทดลองแบบสุ่มที่มีกลุ่มควบคุมเชิงบวก (ในมนุษย์)
การแข็งตัวของเลือดและการเกิดลิ่มเลือดที่เพิ่มขึ้นนั้นสัมพันธ์กับระดับ ROS ที่สูงขึ้น ROS ที่สะสมเป็นผลมาจากการควบคุมสถานะรีดอกซ์ของการแข็งตัวของเลือดและการเกิดลิ่มเลือด โรค Creutzfeldttt–Jakob มีลักษณะเฉพาะคือการทำลายระบบประสาทอย่างรุนแรงและมีอัตราการเสียชีวิตสูงมาก เมื่อไม่นานมานี้มีรายงานเกี่ยวกับการเพิ่มขึ้นของอุบัติการณ์ของโรค Creutzfeldtt-Jakob ในกลุ่มประชากรที่ได้รับการฉีดวัคซีน โรค Creutzfeldttt-Jakob ซึ่งเป็นการเกิดขึ้นของพรีออน (โปรตีนที่พับผิดรูป) ซึ่งทำลายเซลล์ประสาท ดูเหมือนจะเป็นปรากฏการณ์รีดอกซ์
5. ภาวะแทรกซ้อนระยะยาวจากโควิด-19: การเปลี่ยนแปลงไปสู่กระบวนการสร้างกล้ามเนื้อ
ภาวะแทรกซ้อนระยะยาวของ Covid-19 ชี้ให้เห็นถึงการเปลี่ยนแปลงไปสู่โหมดอะนาโบลิกในเซลล์ ซึ่งอาจมองได้ว่าเป็นภาวะแก่ก่อนวัยชนิดหนึ่ง เช่นเดียวกับใน Covid-19 ความบกพร่องของไมโตคอนเดรียซึ่งเป็นลักษณะเฉพาะของปรากฏการณ์ Warburg นั้นมีอยู่ในเกือบทุกโรคและดูเหมือนจะเป็นคุณลักษณะสำคัญในอาการเด่นส่วนใหญ่ของโรคมะเร็ง
เซลล์ประสาทกินแลคเตทที่ปล่อยออกมาจากเซลล์เกลีย ในระหว่างการอักเสบของสมอง เซลล์เกลียจะอยู่ภายใต้แรงกดดัน พวกมันจะหลั่งกรดแลคติกมากขึ้น ซึ่งเซลล์ประสาทจะดูดซึมเข้าไป การดูดซึมกรดแลคติกที่เพิ่มขึ้นนี้ส่งผลให้เกิดภาวะกรดในเซลล์ประสาท ซึ่งเป็นสัญญาณของการทำงานผิดปกติของไมโทคอนเดรีย โรคอัลไซเมอร์ โรคพาร์กินสัน และโรคฮันติงตัน กล้ามเนื้อหัวใจตาย ภาวะหัวใจล้มเหลว โรคหลอดเลือดสมอง มะเร็ง และความชรา ล้วนเชื่อมโยงกับการอักเสบ การทำงานผิดปกติของไมโทคอนเดรีย และความเข้มข้นของแลคเตทที่เพิ่มขึ้นในของเหลวนอกเซลล์
ในโรคโควิด-19 เช่นเดียวกับการอักเสบใดๆ จะมีการปรับเปลี่ยนกระบวนการเผาผลาญ โดยเซลล์จะอาศัยไกลโคไลซิส เนื่องจากไมโทคอนเดรียทำงานบกพร่อง เซลล์ที่ติดเชื้อจึงไม่สามารถสลายสารได้อย่างมีประสิทธิภาพ มันจะปล่อยกรดแลคติกเข้าสู่กระแสเลือด ระดับแลคเตทในเลือดที่สูงของผู้ป่วยโควิด-19 เป็นตัวบ่งชี้ถึงการพยากรณ์โรคที่ไม่ดี โมเลกุลอื่นๆ จะถูกปล่อยออกมาสู่สภาพแวดล้อมของเซลล์และจะสะสมอยู่รอบๆ เซลล์ที่ติดเชื้อ เช่น ไซโตไคน์และลิมโฟไคน์ซึ่งเป็นสาเหตุของการอักเสบ พบความคล้ายคลึงกันอย่างน่าทึ่งระหว่างมะเร็ง โรคอัลไซเมอร์ และโควิด-19 ซึ่งทั้งหมดเกี่ยวข้องกับผลของวอร์เบิร์ก อย่างไรก็ตาม
งานวิจัยบางชิ้นชี้ให้เห็นถึงบทบาทของการสลายสารในโควิด-19
อย่างไรก็ตาม การศึกษาบางชิ้นแนะนำว่าการสลายสารอาจมีบทบาทในกระบวนการของโรค จากการศึกษาหนึ่งพบว่า ผู้ป่วย COVID-19 ที่มีอาการรุนแรงกว่าจะมีระดับตัวบ่งชี้การสลายตัวของโปรตีน เช่น คอร์ติซอล สูงกว่าผู้ป่วยที่มีอาการไม่รุนแรง มีการเสนอแนะว่าสาเหตุนี้เป็นเพราะร่างกายตอบสนองต่อความเครียดและการอักเสบที่เกิดจากไวรัส ซึ่งทำให้เกิดการสลายตัวของโปรตีนและกล้ามเนื้อมากขึ้น ในการศึกษาอีกฉบับหนึ่ง ผู้ป่วยติดเชื้อไวรัสโคโรนาที่มีอาการหนักแสดงให้เห็นอัตราการสร้างยูเรียและการสลายตัวของโปรตีนที่เร่งขึ้น ซึ่งส่วนใหญ่น่าจะมาจากกล้ามเนื้อ บ่งชี้ถึงภาวะการสลายตัวของโปรตีนที่สูง
6. ยาที่ช่วยบรรเทาอาการของ Warburg อาจมีประสิทธิภาพในการรักษาภาวะแทรกซ้อนระยะยาวจากโควิด-19
โรคมะเร็ง การอักเสบ โรคอัลไซเมอร์ และโรคพาร์กินสัน มีลักษณะร่วมกันอย่างหนึ่งคือ ความไม่สามารถของเซลล์ในการส่งออกเอนโทรปีออกนอกร่างกายในรูปแบบที่ไม่เป็นอันตราย เช่น ความร้อน คาร์บอนไดออกไซด์ และน้ำ ในโรคที่มีลักษณะทางคลินิกแตกต่างกันเหล่านี้ ยาที่มุ่งเป้าไปที่ไมโทคอนเดรียดูเหมือนจะมีประสิทธิภาพในการรักษา (ตารางที่ 1)
กรดไลโปอิกได้รับการทดสอบสำหรับโรคที่เกี่ยวข้องกับความชรา มันช่วยชะลอการพัฒนาของโรคอัลไซเมอร์ และในสัตว์ทดลองดูเหมือนว่าจะช่วยปรับปรุงความจำ ลดผลกระทบจากโรคหลอดเลือดสมอง ลดการอักเสบ และชะลอการเติบโตของมะเร็ง
เมทิลีนบลู (MEB) ได้รับการพิสูจน์แล้วว่ามีประสิทธิภาพในการรักษามาลาเรีย โรคเรื้อน และวัณโรค ยาส่วนใหญ่ที่สังเคราะห์ขึ้นระหว่างปี 1920 และ 1950 มาจากผลิตภัณฑ์หลักนี้ นอกจากนี้ MEB ยังช่วยบรรเทา
ผลกระทบของ Warburg ปรับปรุงความจำ มีฤทธิ์ในการรักษาภาวะซึมเศร้า และลดความรุนแรงของโรคหลอดเลือดสมองตีบ
ในกรณีของ Covid-19 พบว่า MEB สามารถยับยั้งการจำลองแบบของ SARS-Cov-2 ในหลอดทดลองได้ พบว่าผู้ป่วย Covid-19 ที่ได้รับการรักษาด้วย MEB มีระยะเวลาการพักรักษาตัวในโรงพยาบาลและอัตราการเสียชีวิตลดลงอย่างมีนัยสำคัญ
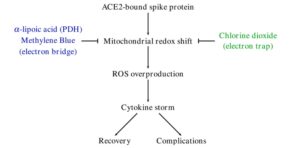
ภาพที่ 1 กลไกที่เสนอซึ่งกรดอัลฟาไลโปอิก (ALA) เมทิลีนบลู (MeB) และคลอรีนไดออกไซด์ออกฤทธิ์ในการรักษา COVID-19 และภาวะแทรกซ้อนหลังระยะเฉียบพลัน ALA จับคู่กับเอนไซม์ไพรูเวตดีไฮโดรจีเนสคอมเพล็กซ์ (PDH); MeB ทำหน้าที่เป็นสะพานอิเล็กตรอนระหว่างตัวให้ (FADH2, FMNH, NADH) และโมเลกุลตัวรับ เช่น ออกซิเจน และโมเลกุล ClO2 ดักจับอิเล็กตรอนห้าตัว ทำให้เป็นกับดักอิเล็กตรอนแบบครั้งเดียว
คลอรีนไดออกไซด์อาจถูกแนะนำให้ใช้เป็นวิธีการรักษา COVID-19 ได้เช่นกัน เนื่องจากมีความสัมพันธ์กับอิเล็กตรอนอย่างมาก และความจริงที่ว่ามันสลายตัวอย่างรวดเร็วเป็นไอออนคลอไรด์และน้ำ นอกจากนี้ยังเป็นสารต้านไวรัสที่มีศักยภาพต่อ SARS-CoV-2 อีกด้วย คลอรีนไดออกไซด์และเมทิลีนบลูมีกลไกการออกฤทธิ์ที่แตกต่างกัน (ภาพที่ 1) ในด้านหนึ่ง MeB เป็นโมเลกุลตัวรับ-ตัวให้: MeB+ สามารถรับอิเล็กตรอนคู่หนึ่ง
(ของอะตอม H) และ MeBH สามารถปล่อยอิเล็กตรอนคู่นี้ได้ง่าย ดังนั้น MeB จึงถูกนำกลับมาใช้ใหม่บางส่วนเหมือนตัวเร่งปฏิกิริยา ในอีกด้านหนึ่ง เลขออกซิเดชันของคลอรีนใน ClO2 คือ +IV และเปลี่ยนเป็น –I ใน Cl- ซึ่งมีความเสถียร และถูกขับออกจากร่างกายมนุษย์ ดังนั้นโมเลกุล ClO2 แต่ละโมเลกุลจึงดักจับอิเล็กตรอนห้าตัวในกระบวนการนี้ ดังนั้น ClO2 จึงเป็นกับดักอิเล็กตรอนแบบครั้งเดียว ในขณะที่ MeB ทำหน้าที่เป็นสะพานอิเล็กตรอนระหว่างผู้ให้ (FADH2, FMNH, NADH) และผู้รับ (คอมเพล็กซ์ IV ของ ETC หรือออกซิเจนเอง) ในฐานะโคเอนไซม์ของไพรูเวทดีไฮโดรจีเนส (PDH) กรดอัลฟา-ไลโปอิก (ALA) เริ่มต้นการสร้างอะเซทิล-CoA เพื่อป้อนเข้าสู่รอบ TCA ดังนั้น ALA จึงช่วยเพิ่มการสลายตัวของคาร์บอนรอบ TCA และด้วยเหตุนี้จึงอาจลดผลกระทบของ Warburg และส่งผลให้การผลิตแลคเตทลดลง เมทิลีนบลูมีบทบาทคล้ายกันหลังจากรอบ TCA โดยการนำอิเล็กตรอนไปยังคอมเพล็กซ์ IV ของห่วงโซ่การขนส่งอิเล็กตรอน คลอรีนไดออกไซด์ยังช่วยลดการเปลี่ยนแปลงรีดอกซ์โดยการรับอิเล็กตรอนส่วนเกินที่ถูกพาไปโดย Cl- และน้ำ
บทสรุป
ในกรณีของโควิด-19 เช่นเดียวกับโรคอื่นๆ เอนโทรปีบางส่วนไม่สามารถส่งออกไปในรูปแบบที่ไม่เป็นอันตราย เช่น ความร้อน น้ำ และคาร์บอนไดออกไซด์ (การสลายตัว) และจะถูกปล่อยออกมาในโมเลกุลชีวภาพขนาดใหญ่ (การสร้าง) ยาเช่นกรดไลโปอิกและ MeB ซึ่งมุ่งเป้าไปที่กระบวนการเผาผลาญ จะช่วยลดการเปลี่ยนแปลงของปฏิกิริยาออกซิเดชัน-รีดักชันโดยการเพิ่มการสลายตัว เป็นไปได้ว่าการรักษาโดยใช้ MeB คลอรีนไดออกไซด์ และกรดไลโปอิก จะช่วยลดภาวะแทรกซ้อนระยะยาวของโควิด-19 ที่เกิดจากโปรตีนหนามของไวรัส SARS-Cov-2
เอกสารอ้างอิง
[1] B.D. Paul, M.D. Lemle, A.L. Komaroff, S.H. Snyder, Redox iMeBalance เชื่อมโยง COVID19 และโรคไข้สมองอักเสบกล้ามเนื้อ/กลุ่มอาการอ่อนเพลียเรื้อรัง, Proc. Natl. Acad. Sci.U. S. A. 118 (34) (2021).
[2] B. Long, W.J. Brady, A. Koyfman, M. Gottlieb, ภาวะแทรกซ้อนทางหัวใจและหลอดเลือดใน COVID-19, Am. J. Emerg. Med. 38 (7) (2020) 1504–1507.
[3] A. Filatov, P. Sharma, F. Hindi, P.S. Espinosa, ภาวะแทรกซ้อนทางระบบประสาทของโรคติดเชื้อไวรัสโคโรนา (COVID-19): โรคไข้สมองอักเสบ, Cureus 12 (3) (2020), e7352.
[4] G. Saini, R. Aneja, มะเร็งเป็นผลสืบเนื่องที่อาจเกิดขึ้นจากภาวะลองโควิด-19, Bioessays 43 (6) (2021), e2000331.
[5] L. Schwartz, M. Henry, K.O. Alfarouk, S.J. Reshkin, M. Radman, การเปลี่ยนแปลงทางเมตาบอลิซึมเป็นลักษณะเด่นของโรคทั่วไปส่วนใหญ่: การแสวงหาความเป็นเอกภาพที่อยู่เบื้องหลัง, Int. J. Mol. Sci. 22 (8) (2021).
[6] L. Schwartz, A. Devin, F. Bouillaud, M. Henry, เอนโทรปีเป็นแรงขับเคลื่อนของการเกิดโรค: ความพยายามในการจำแนกโรคตามกฎของฟิสิกส์, Substantia 4 (2) (2020).
[7] D. Hanahan, R.A. Weinberg, ลักษณะเด่นของมะเร็ง: รุ่นต่อไป, Cell 144 (5) (2011) 646–674.
[8] E. Calva, A. Mujica, R. Nunez, K. Aoki, A. Bisteni, D. Sodi-Pallares, การเปลี่ยนแปลงทางชีวเคมีของไมโตคอนเดรียและสารละลายกลูโคส-KCl-อินซูลินในภาวะกล้ามเนื้อหัวใจขาดเลือด, Am. J.Physiol. 211 (1) (1966) 71–76.
[9] R.J. Henning, M.H. Weil, F. Weiner, แลคเตทในเลือดเป็นตัวบ่งชี้การพยากรณ์โรคของการรอดชีวิตในผู้ป่วยที่มีภาวะกล้ามเนื้อหัวใจขาดเลือดเฉียบพลัน, Circ. Shock 9 (3) (1982) 307–315.
[10] G. Reimer, แอนติบอดีต่อต้านแอนติเจนนิวเคลียร์ นิวคลีโอลาร์ และไมโตคอนเดรียในโรคหนังแข็งทั่วร่างกาย (scleroderma), Rheum. Dis. Clin. N. Am. 16 (1) (1990) 169–183.
[11] S.K. Yang, H.R. Zhang, S.P. Shi, Y.Q. Zhu, N. Song, Q. Dai, W. Zhang, M. Gui, H. Zhang, บทบาทของไมโตคอนเดรียในโรคแพ้ภูมิตัวเองชนิดทั่วร่างกาย: ภาพรวมของกลไกการเกิดโรคต่างๆ, Curr. Med. Chem. 27 (20) (2020) 3346–3361.
[12] L.M. McCaffrey, A. Petelin, B.A. Cunha, โรคแพ้ภูมิตัวเองชนิดลูปัส (SLE) สมองอักเสบเทียบกับเยื่อหุ้มสมองอักเสบจากเชื้อ Listeria monocytogenes ในผู้ป่วยโรคแพ้ภูมิตัวเองชนิดลูปัสที่ได้รับการรักษาด้วยคอร์ติโคสเตียรอยด์เรื้อรัง: การวินิจฉัยความสำคัญของระดับกรดแลคติกในน้ำไขสันหลัง (CSF) Heart Lung 41 (4) (2012) 394–397.
[13] Z. Daniil, O.S. คอตซิอู, เอ. แกรมมาติโกปูลอส, เอส. เปเลติดู, เอช. กกิก้า, เอฟ. มัลลี, เค. อันโตนิอู, อี. วาซามิดี, ซ. มามูริส, เค. กูร์กูเลียนิส, อี. ซิฟา, การตรวจจับการกลายพันธุ์ของยีนที่ถ่ายโอนไมโตคอนเดรีย RNA (mt-tRNA) ในผู้ป่วยที่ไม่ทราบสาเหตุพังผืดในปอดและ Sarcoidosis, Mitochondrion 43 (2018) 43–52
(14) เจ. ทาเรจา, เอช. ทัลวาร์, ซี. เบาเออร์เฟลด์, L.I. กรอสแมน, เค. จาง, พี. ทรานชิดา, L. Samavati, HIF-1alpha ควบคุม IL-1beta และ IL-17 ใน Sarcoidosis, Elife 8 (2019)
[15] J.T. Newington, R.A. Harris, R.C. Cumming, การประเมินการเผาผลาญในโรคอัลไซเมอร์ใหม่จากมุมมองของแบบจำลองการขนส่งแลคเตทระหว่างเซลล์แอสโทรไซต์และเซลล์ประสาท, J Neurodegener Dis 2013 (2013), 234572.
[16] A.G. Vlassenko, M.E. Raichle, หน้าที่ของไกลโคไลซิสแบบแอโรบิกในสมองและโรคอัลไซเมอร์, Clin Transl Imaging 3 (1) (2015) 27–37.
[17] L. Traxler, J.R. Herdy, D. Stefanoni, S. Eichhorner, S. Pelucchi, A. Szucs, A. Santagostino, Y. Kim, R.K. Agarwal, J.C.M. Schlachetzki, C.K. กระจก, J. Lagerwall, D. Galasko, F.H. Gage, A. D’Alessandro, J. Mertens, เหมือน Warburg การเปลี่ยนแปลงทางเมตาบอลิซึมเป็นสาเหตุให้เกิดความเสื่อมของเส้นประสาทในโรคอัลไซเมอร์ประปรายโรคเมตาบอลิซึมของเซลล์ 34 (9) (2022) 1248–1263 จ.6
(18) พี. กอนซาเลซ-โรดริเกซ, อี. ซามเปเซ, เค.เอ. สเตาท์, เจ.เอ็น. กุซมาน, อี. อิลิจิช, บี. ยัง, T. Tkatch, M.A. Stavarache, D.L. Wokosin, L. Gao, M.G. แคปลิตต์, เจ. โลเปซ-บาร์เนโอ, พี.ที. ชูมัคเกอร์, ดีเจ. Surmeier, การหยุดชะงักของคอมเพล็กซ์ I ของไมโตคอนเดรียทำให้เกิดโรคพาร์กินสันแบบก้าวหน้า Nature 599 (7886) (2021) 650–656
[19] P. Icard, H. Lincet, Z. Wu, A. Coquerel, P. Forgez, M. Alifano, L. Fournel, บทบาทสำคัญของผล Warburg ในการจำลองแบบของ SARS-CoV-2 และการตอบสนองการอักเสบที่เกี่ยวข้อง Biochimie 180 (2021) 169–177
[20] L. Szarpak, K. Ruetzler, K. Safiejko, M. Hampel, M. Pruc, L. Kanczuga-Koda, K. J. Filipiak, M.J. Jaguszewski, ระดับแลคเตทดีไฮโดรจีเนสเป็นตัวบ่งชี้ความรุนแรงของ COVID-19 Am. J. Emerg. Med. 45 (2021) 638–639.
[21] A. Thirupathi, Y. Gu, Z. Radak, R.A. Pinho, สถานะรีดอกซ์เป็นหลักสำคัญของ SARSCoV-2 และโฮสต์ในการสร้างโอกาสในการรักษา, Antioxidants 11 (10) (2022).
[22] D. Giustarini, A. Santucci, D. Bartolini, F. Galli, R. Rossi, การลดลงของสมดุลไทออล-ไดซัลไฟด์นอกเซลล์ที่ขึ้นอยู่กับอายุและบทบาทของมันในการติดเชื้อ SARS-CoV-2, Redox Biol. 41 (2021), 101902.
[23] J. Singh, R.S. Dhindsa, V. Misra, B. Singh, ความสามารถในการติดเชื้อของ SARS-CoV2 อาจถูกปรับเปลี่ยนโดยสถานะรีดอกซ์ของโฮสต์, Comput. Struct. Biotechnol. J. 18 (2020) 3705–3711.
[24] S. Hati, S. Bhattacharyya, ผลกระทบของสมดุลไทออล-ไดซัลไฟด์ต่อการจับกันของโปรตีนหนามของโควิด-19 กับตัวรับเอนไซม์แองจิโอเทนซินคอนเวอร์ติง 2, ACS Omega 5 (26) (2020) 16292–16298.
[25] J. Lan, J. Ge, J. Yu, S. Shan, H. Zhou, S. Fan, Q. Zhang, X. Shi, Q. Wang, L. Zhang, X. Wang, โครงสร้างของโดเมนการจับตัวรับสไปค์ของ SARS-CoV-2 ที่จับกับตัวรับ ACE2, Nature 581 (7807) (2020) 215–220, 19 R.
[26] R. Yan, Y. Zhang, Y. Li, L. Xia, Y. Guo, Q. Zhou, พื้นฐานโครงสร้างสำหรับการรับรู้ของ SARS-CoV-2 โดย ACE2 ของมนุษย์แบบเต็มความยาว, Science 367 (6485) (2020) 1444–1448.
[27] A.S. LeRoy, B. Robles, L.S. Kilpela, L.M. Garcini, การเสียชีวิตท่ามกลางการระบาดของ COVID-19: ข้อควรพิจารณาตามบริบทและคำแนะนำทางคลินิก, Psychol Trauma 12 (S1) (2020) S98–S99.
[28] Y. Lei, K. Wang, L. Deng, Y. Chen, E.C. Nice, C. Huang, การควบคุมรีดอกซ์ของการอักเสบ: องค์ประกอบเก่า เรื่องราวใหม่, Med. Res. Rev. 35 (2) (2015) 306–340.
[29] P. Checconi, M. De Angelis, M.E. Marcocci, A. Fraternale, M. Magnani, A.T. Palamara, L. Nencioni, สารปรับเปลี่ยนรีดอกซ์ในการรักษาการติดเชื้อไวรัส, Int. J. Mol. Sci. 21 (11) (2020).
[30] D. Zendelovska, E. Atanasovska, M. Petrushevska, K. Spasovska, M. Stevanovikj, I. Demiri, N. Labachevski, การประเมินเครื่องหมายความเครียดออกซิเดชันในผู้ป่วยที่เข้ารับการรักษาในโรงพยาบาลที่มี COVID-19 ระดับปานกลางและรุนแรง Rom. J. Intern. Med. 59 (4) (2021) 375–383
[31] A. Nasi, S. McArdle, G. Gaudernack, G. Westman, C. Melief, J. Rockberg, R. Arens, D. Kouretas, J. Sjolin, S. Mangsbo, สารออกซิเจนที่ออกฤทธิ์เป็นตัวเริ่มต้นของการตอบสนองภูมิคุ้มกันโดยกำเนิดที่เป็นพิษต่อ SARS-CoV-2 ในประชากรสูงอายุพิจารณา N-acetylcysteine เป็นการแทรกแซงการรักษาในระยะเริ่มต้น Toxicol Rep 7 (2020) 768–771.
[32] R. Zhou, A.S. Yazdi, P. Menu, J. Tschopp, บทบาทของไมโตคอนเดรียในการกระตุ้น NLRP3 inflammasome Nature 469 (7329) (2011) 221–225.
[33] J. Muri, M. Kopf, การควบคุมรีดอกซ์ของการเผาผลาญภูมิคุ้มกัน Nat. Rev. Immunol. 21 (6) (2021) 363–381.
[34] M. Mittal, M.R. Siddiqui, K. Tran, S.P. Reddy, A.B. Malik, สารออกซิเจนที่ออกฤทธิ์ในการอักเสบและการบาดเจ็บของเนื้อเยื่อ, Antioxidants Redox Signal. 20 (7) (2014) 1126–1167.
[35] S.K. Biswas, ความสัมพันธ์ระหว่างความเครียดออกซิเดชันและการอักเสบอธิบายความขัดแย้งของสารต้านอนุมูลอิสระได้หรือไม่? Oxid. Med. Cell. Longev. 2016 (2016), 5698931.
[36] R. Chang, A. Mamun, A. Dominic, N.T. Le, ความผิดปกติของเยื่อบุหลอดเลือดที่เกิดจาก SARS-CoV-2: บทบาทที่เป็นไปได้ของความเครียดออกซิเดชันเรื้อรัง, Front. Physiol. 11 (2020), 605908.
(37) เจ. ซาเลห์, ซี. เพย์สซอนโนซ์, เค.เค. Singh, M. Edeas, Mitochondria และ microbiota ความผิดปกติในการเกิดโรค COVID-19, Mitochondrion 54 (2020) 1–7
(38) เอ็ม. กูเมนู, ดี. ซาริเจียนนิส, เอ. ทซัตซาคิส, โอ. อเนสตี, เอ.โอ. โดเซีย, ดี. เพทราคิส, ดี. ซูคาลาส, ร. คอสต์ตอฟฟ์, วี. ราคิทสกี้, D.A. สแปนดิดอส, เอ็ม. แอสชเนอร์, ดี. คาลิน่า, โควิด-19 ในอิตาลีตอนเหนือ: ภาพรวมเชิงบูรณาการของปัจจัยที่อาจมีอิทธิพลการระบาดเพิ่มขึ้นอย่างรวดเร็ว (ทบทวน) โมล ยา ตัวแทน 22 (1) (2020) 20–32
(39) ดี. ซาดาโตมิ, เค. นากาชิโอยะ, เอส. มามิยะ, เอส. ฮอนดะ, วาย. คาเมยามะ, วาย. ยามามูระ, S. Tanimura, K. Takeda, ฟังก์ชันไมโตคอนเดรียเป็นสิ่งจำเป็นสำหรับการกระตุ้นการอักเสบของ NLRP3 ที่เกิดจาก ATP นอกเซลล์, J. Biochem 161 (6) (2017) 503–512.
[40] เจ. วู รับมือกับความเสียหายจากอนุมูลอิสระในโควิด-19 ไนตริกออกไซด์ 102 (2020) 39–41.
(41) J.M. Gostner, K. Becker, D. Fuchs, R. Sucher, การควบคุมรีดอกซ์ของระบบภูมิคุ้มกันการตอบสนอง ตัวแทนรีดอกซ์ 18 (3) (2013) 88–94
[42] Y.Q. Xie, H. Arik, L. Wei, Y. Zheng, H. Suh, D.J. Irvine, L. Tang, นาโนเจลอินเตอร์ลิวคิน-2 ที่ตอบสนองต่อรีดอกซ์ ส่งเสริมการแพร่กระจายและการแยกตัวของเซลล์ T ที่ตอบสนองต่อเนื้องอกโดยเฉพาะและปลอดภัย สารตั้งต้นความจำ, Biomater. Sci. 7 (4) (2019) 1345–1357.
[43] P. Prasun, COVID-19: มุมมองไมโตคอนเดรีย, DNA Cell Biol. 40 (6) (2021) 713–719.
[44] เคโอ อัลฟารุก, S.T.S. อัลฮูฟี, เอ. ฮิฟนี, แอล. ชวาตซ์, เอ.เอส. อัลกาห์ตานี, S.B.เอ็ม. อาเหม็ด A.M. อัลกาห์ตานี, เอส.เอส. อัลกาห์ตานี, อ.เค. มุดดาธีร์, เอช. อาลี, เอ.เอช.เอช. บาชีร์ M.E. อิบราฮิม, M.R. Greco, R.A. คาร์โดน, เอส. ฮาร์กวินดีย์, เอส.เจ. เรชคิน, ออฟไมโตคอนเดรียกับโควิด-19, เจ. เอนไซม์. ยับยั้ง ยา เคมี. 36 (1) (2021)
1258–1267.
[45] ส.ดี. อูนูดูร์ธี, พี. ลูธรา, อาร์.เจ.ซี. โบส, เจ.อาร์. แม็กคาร์ธี, M.I. Kontaridis, การอักเสบของหัวใจใน COVID-19: บทเรียนจากภาวะหัวใจล้มเหลว, Life Sci. 260 (2020), 118482.
[46] S. Zaim, J.H. Chong, V. Sankaranarayanan, A. Harky, COVID-19 และการตอบสนองของอวัยวะหลายระบบ, Curr. Probl. Cardiol. 45 (8) (2020), 100618.
[47] F. Wang, R.M. Kream, G.B. Stefano, ผลกระทบระยะยาวของระบบทางเดินหายใจและระบบประสาทจาก COVID-19, Med. Sci. Mon. Int. Med. J. Exp. Clin. Res. 26 (2020), e928996.
[48] R.K. Kaundal, A.K. Kalvala, A. Kumar, ผลกระทบทางระบบประสาทของ COVID-19: บทบาทของสมดุลรีดอกซ์และการทำงานผิดปกติของไมโตคอนเดรีย, Mol. Neurobiol. 58 (9) (2021) 4575–4587.
[49] T. Rudroff, C.D. Workman, L.L.B. Ponto, การถ่ายภาพ (18)F-FDG-PET สำหรับการเปลี่ยนแปลงของสมองและกล้ามเนื้อโครงร่างหลัง COVID-19, Viruses 13 (11) (2021).
[50] G. Carpene, D. Onorato, R. Nocini, G. Fortunato, J.G. Rizk, B.M. Henry, G. Lippi, ความเข้มข้นของแลคเตทในเลือดใน COVID-19: การทบทวนวรรณกรรมอย่างเป็นระบบ, Clin.Chem. Lab. Med. 60 (3) (2022) 332–337.
[51] เค.เจ.จี. ดิแอซ-เรเซนดิซ, เอ.บี. เบนิเตซ-ตรินิแดด, C.E. Covantes-Rosales, G.A. ToledoIbarra, P.C. ออร์ติซ-ลาซาเรโน, D.A. Giron-Perez, A.Y. บูเอโน-ดูรัน, D.A. เปเรซ-ดิแอซ, อาร์จี บาร์เซลอส-การ์เซีย มิชิแกน Giron-Perez การสูญเสียศักยภาพของไมโตคอนเดรีย meMeBrane (DeltaPsi(m)) ในเม็ดเลือดขาวเป็นผลสืบเนื่องหลังโควิด-19, J. Leukoc ไบโอล 112 (1) (2022) 23–29.
(52) เค. ซิง, X.Y. Tu, M. Liu, Z.W. เหลียง เจ.เอ็น. เฉิน เจ.เจ. หลี่ แอล.จี. เจียง เอฟ.คิว. ซิง Y. Jiang ประสิทธิภาพและความปลอดภัยของวัคซีนป้องกันโควิด-19: การทบทวนอย่างเป็นระบบ จงกัวดังไดเอ้อเค่อซาจือ 23 (3) (2021) 221–228
(53) เจ.เอช. Kim, F. Marks, J.D. Clemens มองให้ไกลกว่าการทดลองวัคซีนป้องกันโควิด-19 ระยะที่ 3 แนท. ยา 27 (2) (2021) 205–211.
(54) T.T. Shimabukuro อัปเดตความปลอดภัยของวัคซีนป้องกันโควิด-19 ปี 2021
(55) เค. คัตซิกาส ไทรแอนทาฟิลลิดิส, พี. เจียนอส, ไอ.ที. มีอัน, จี. เคิร์ตโซนิส, เค.เอส. Kechagias, การกระตุ้นการทำงานของไวรัสอีสุกอีใสหลังการฉีดวัคซีนโควิด-19: การทบทวนอย่างเป็นระบบของรายงานกรณีศึกษา, Vaccines 9 (9) (2021).
[56] R. Lensen, M.G. Netea, F.R. Rosendaal, การกระตุ้นการทำงานของไวรัสตับอักเสบซีหลังการฉีดวัคซีนโควิด-19 – รายงานกรณีศึกษา, Int. Med. Case Rep. J. 14 (2021) 573–576.
[57] S. Aghabaklou, S.M. Razavi, P. Mohammadi, S. Gholamin, A. Mowla, ภาวะแทรกซ้อนจากการแข็งตัวของเลือดในสมองหลังการฉีดวัคซีนเวกเตอร์อะดีโนไวรัสโควิด-19: การทบทวนอย่างเป็นระบบ, J. Neurol. Res. 11 (5) (2021) 69–76.
[58] M. De Michele, J. Kahan, I. Berto, O.G. Schiavo, M. Iacobucci, D. Toni, A.E. Merkler, ภาวะแทรกซ้อนของหลอดเลือดสมองจาก COVID-19 และ COVID-19 การฉีดวัคซีน, Circ. Res. 130 (8) (2022) 1187–1203.
[59] A. Gorlach, การควบคุมรีดอกซ์ของกระบวนการแข็งตัวของเลือด, Antioxidants Redox Signal. 7 (9-10) (2005) 1398–1404.
[60] D. Gregg, D.D. de Carvalho, H. Kovacic, อินทิกรินและการแข็งตัวของเลือด: บทบาทของ ROS/การส่งสัญญาณรีดอกซ์? Antioxidants Redox Signal. 6 (4) (2004) 757–764.
[61] S. Serine, H. Sungurtekin, โรค Creutzfeldttt-Jakob หลังจากการฉีดวัคซีน COVID-19, 2020
[62] N. Singh, A. Singh, D. Das, M.L. Mohan, การควบคุมรีดอกซ์ของพรีออนและโรค การเกิดโรค, Antioxidants Redox Signal. 12 (11) (2010) 1271–1294.
[63] E. Duan, K. Garry, L.I. Horwitz, H. Weerahandi, “ฉันไม่เหมือนเดิมอีกต่อไปแล้ว”: การวิเคราะห์เชิงคุณภาพของผู้รอดชีวิตจาก COVID-19, Int. J. Behav. Med. (2022) 1–10.
[64] L. Schwartz, C.T. Supuran, K.O. Alfarouk, ผลกระทบของ Warburg และลักษณะเด่นของมะเร็ง, Anti Cancer Agents Med. Chem. 17 (2) (2017) 164–170.
[65] L. Schwartz, A. Devin, F. Bouillaud, M. Henry, เอนโทรปีเป็นแรงขับเคลื่อนของการเกิดโรค: ความพยายามในการจำแนกโรคตามกฎของฟิสิกส์, Substantia 4 (2) (2020).
[66] D.C. Wallace, ไมโตคอนเดรียและมะเร็ง: Warburg กล่าวถึง, Cold Spring Harbor Symp. Quant. Biol. 70 (2005) 363–374.
[67] N. Amiri-Dashatan, M. Koushki, N. Parsamanesh, H. Chiti, ความเข้มข้นของคอร์ติซอลในซีรั่ม และความรุนแรงของ COVID-19: การทบทวนอย่างเป็นระบบและการวิเคราะห์เมตา, J. Invest. Med. 70 (3) (2022) 766–772.
[68] J. Uribarri, O. El Shamy, S. Sharma, J. Winston, การบาดเจ็บของไตเฉียบพลันที่เกี่ยวข้องกับ COVID-19 และอัตราการสลายโปรตีนที่วัดได้: ผลกระทบที่อาจเกิดขึ้นจากพายุไซโตไคน์ต่อการสลายโปรตีนของกล้ามเนื้อ, Kidney Med 3 (1) (2021) 60–63 e1.
[69] E. Poteet, G.R. Choudhury, A. Winters, W. Li, M.G. Ryou, R. Liu, L. Tang, A. Ghorpade, Y. Wen, F. Yuan, S.T. Keir, H. Yan, D.D. Bigner, J.W. Simpkins, S.H. Yang, การย้อนกลับผลของ Warburg เป็นการรักษาสำหรับ glioblastoma, J. Biol.Chem. 288 (13) (2013) 9153–9164.
[70] P.M. Bingham, S.D. Stuart, Z. Zachar, กรดไลโปอิกและอนาล็อกของกรดไลโปอิกในมะเร็งการเผาผลาญและเคมีบำบัด, Expet Rev. Clin. Pharmacol. 7 (6) (2014) 837–846.
[71] R. Abolhassani, E. Berg, G. Tenenbaum, M. Israel, การยับยั้ง Scot และ ketolysis ลดการเติบโตของเนื้องอกและการอักเสบในแบบจำลองมะเร็ง Lewis, JJ Oncol Clin Res 3 (2022) 1–2.
[72] L. Schwartz, L. Buhler, P. Icard, H. Lincet, J.M. Steyaert, การรักษาทางเมตาบอลิซึมของมะเร็ง: ผลลัพธ์เบื้องต้นของชุดกรณีศึกษาเชิงคาดการณ์, Anticancer Res. 34 (2) (2014) 973–980.
[73] R.H. Schirmer, H. Adler, M. Pickhardt, E. Mandelkow, เพื่อไม่ให้เราลืมคุณ — เมทิลีนบลู, Neurobiol. Aging 32 (12) (2011), 2325-e7.
[74] K. Hager, M. Kenklies, J. McAfoose, J. Engel, G. Munch, กรดอัลฟา-ไลโปอิกเป็นทางเลือกการรักษาใหม่สำหรับโรคอัลไซเมอร์ — การวิเคราะห์ติดตามผล 48 เดือน, J. Neural. Transm. Suppl (72) (2007) 189–193.
[75] L. Shinto, J. Quinn, T. Montine, H.H. Dodge, W. Woodward, S. Baldauf-Wagner, D. Waichunas, L. Bumgarner, D. Bourdette, L. Silbert, J. Kaye, การทดลองนำร่องแบบสุ่มควบคุมด้วยยาหลอกของกรดไขมันโอเมก้า-3 และกรดอัลฟาไลโปอิกในโรคอัลไซเมอร์, J Alzheimers Dis 38 (1) (2014) 111–120.
[76] G.S. Mijnhout, B.J. Kollen, A. Alkhalaf, N. Kleefstra, H.J. Bilo, กรดอัลฟาไลโปอิกสำหรับโรคเส้นประสาทส่วนปลายที่มีอาการในผู้ป่วยเบาหวาน: การวิเคราะห์เมตาของการทดลองควบคุมแบบสุ่ม, Internet J. Endocrinol. 2012 (2012), 456279.
[77] P. Rodriguez, W. Zhou, D.W. Barrett, W. Altmeyer, J.E. Gutierrez, J. Li, J.L. Lancaster, F. Gonzalez-Lima, T.Q. Duong, การถ่ายภาพ MR เชิงฟังก์ชันแบบสุ่มหลายรูปแบบของผลกระทบของเมทิลีนบลูในสมองมนุษย์, Radiology 281 (2) (2016) 516–526.
[78] J.F. Quinn, J.R. Bussiere, R.S. Hammond, T.J. Montine, E. Henson, R.E. Jones, R.W. Stackman Jr., กรดอัลฟา-ไลโปอิกในอาหารเรื้อรังช่วยลดความบกพร่องในฮิปโปแคมปัสความจำของหนู Tg2576 ที่มีอายุมาก, Neurobiol. Aging 28 (2) (2007) 213–225.
[79] L.A. Zoellner, M. Telch, E.B. Foa, F.J. Farach, C.P. McLean, R. Gallop, E.J. Bluett, A. Cobb, F. Gonzalez-Lima, การเสริมสร้างการเรียนรู้การดับลงในภาวะความเครียดหลังเหตุการณ์สะเทือนใจ
ด้วยการสัมผัสจินตนาการรายวันสั้นๆ และเมทิลีนบลู: การทดลองแบบสุ่มควบคุม, J. Clin. Psychiatry 78 (7) (2017) e782–e789.
[80] M. Alda, M. McKinnon, R. Blagdon, J. Garnham, S. MacLellan, C. O’Donovan, T. Hajek, C. Nair, S. Dursun, G. MacQueen, การรักษาด้วยเมทิลีนบลูสำหรับอาการที่เหลืออยู่ของโรคอารมณ์สองขั้ว: การศึกษาแบบไขว้แบบสุ่ม Br. J. Psychiatry 210 (1) (2017) 54–60.
[81] M.R. Salazar, กรดอัลฟาไลโปอิก: การรักษาแบบใหม่สำหรับภาวะซึมเศร้า Med. Hypotheses 55 (6) (2000) 510–512.
[82] Q. Shen, F. Du, S. Huang, P. Rodriguez, L.T. Watts, T.Q. Duong, ประสิทธิภาพในการปกป้องระบบประสาทของเมทิลีนบลูในโรคหลอดเลือดสมองตีบ: การศึกษาด้วย MRI, PLoS One 8 (11) (2013), e79833.
[83] K.H. Choi, M.S. Park, H.S. Kim, K.T. Kim, H.S. Kim, J.T. Kim, B.C. Kim, M.K. Kim, J.T. Park, K.H. Cho, การรักษาด้วยกรดอัลฟา-ไลโปอิกมีฤทธิ์ฟื้นฟูระบบประสาทและส่งเสริมการฟื้นตัวของการทำงานหลังเกิดโรคหลอดเลือดสมองในหนู, Mol. Brain 8 (2015) 9.
[84] M. Henry, M. Summa, L. Patrick, L. Schwartz, กลุ่มผู้ป่วยมะเร็งที่ไม่มีรายงานผู้ติดเชื้อ SARS-CoV-2: บทบาทการป้องกันที่เป็นไปได้ของเมทิลีนบลู, Substantia, 2020, หน้า 888.
(85) เอฟ.เอ. มูรา, เค.คิว. de Andrade, J.C. dos Santos, มิสซูรี กูลาร์ต กรดไลโปอิก:มัน บทบาทของสารต้านอนุมูลอิสระและต้านการอักเสบและการใช้งานทางคลินิก Curr สูงสุด. ยาเคมี. 15 (5) (2015) 458–483.
(86) ดี. ฮามิดี-อาลัมดาริ, เอส. ฮาฟิซี-โลทฟาบาดี, อ. บาเกรี-โมกฮัดดัม, เอช. ซาฟารี, เอ็ม. มอสดูเรียน, ซ. จาวิดารารับชาฮี, เอ. เปอิวานดิ-ยาซดี, เอ. อาลี-เซราตี, เอ. เซดากัต, F. Poursadegh, F. Barazandeh-Ahmadabadi, M. Agheli-Rad, S.M. Tavousi, S. Vojouhi, S. Amini, M. Amini, S. Majid-Hosseini, A. Tavanaee-Sani, A. Ghiabi, S. Nabavi-Mahalli, N. Morovatdar, O. Rajabi, G. Koliakos, เมทิลีนบลูสำหรับการรักษาผู้ป่วยโควิด-19 ที่เข้ารับการรักษาในโรงพยาบาล: การทดลองทางคลินิกแบบสุ่ม ควบคุม และเปิดเผยผล ระยะที่ 2, Rev. Invest. Clin. 73 (3) (2021) 190–198.
[87] M. Isra¨el, L. Schwartz, การปรับเปลี่ยนกระบวนการเผาผลาญที่พบในมะเร็งทำให้เซลล์เนื้องอก ต้องพึ่งพาสารคีโตนและอ่อนแอต่อการยับยั้ง SCOT, Endocrinol Diabetes Metabol 4 (2020) 14.
[88] M. Gendrot, J. Andreani, I. Duflot, M. Boxberger, M. Le Bideau, J. Mosnier, P. Jardot, I. Fonta, C. Rolland, H. Bogreau, S. Hutter, B. La Scola, B. Pradines, เมทิลีนบลูยับยั้งการจำลองแบบของ SARS-CoV-2 ในหลอดทดลอง, Int. J. Antimicrob. Agents 56 (6) (2020), 106202.
[89] N. Hatanaka, B. Xu, M. Yasugi, H. Morino, H. Tagishi, T. Miura, T. Shibata, S. Yamasaki, คลอรีนไดออกไซด์เป็นสารต้านไวรัสที่มีศักยภาพมากกว่าโซเดียมไฮโปคลอไรต์ต่อ SARS-CoV-2 J. Hosp. Infect. 118 (2021) 20–26.
[90] A. Pullman, B. Pullman, Quantum Biochemistry, Wiley–Interscience, New York, 1963.
[91] 1F. Bouillaud, C. Ransy, M. Moreau, J. Benhaim, A. LoMeBes, P. Haouzi, การบริโภค O(2) ที่เกิดจากเมทิลีนบลูไม่ขึ้นอยู่กับการออกซิเดชั่นฟอสโฟรีเลชั่นของไมโทคอนเดรีย: ผลกระทบต่อเส้นทางการกู้คืนระหว่างการเป็นพิษของไมโทคอนเดรียเฉียบพลัน, Respir. Physiol. Neurobiol. 304 (2022), 103939.
[92] J.A. Mayr, R.G. Feichtinger, F. Tort, A. Ribes, W. Sperl, ข้อบกพร่องในการสังเคราะห์กรดไลโปอิก, J. Inherit. Metab. Dis. 37 (4) (2014) 553–563.
[93] L.G. Korotchkina, S. Sidhu, M.S. Patel, กรด R-lipoic ยับยั้ง pyruvate dehydrogenase kinase ของสัตว์เลี้ยงลูกด้วยนม, Free Radic. Res. 38 (10) (2004) 1083–1092.
[94] J. da Veiga Moreira, L. De Staercke, P. Cesar Martinez-Basilio, S. GauthierThibodeau, L. Montegut, L. Schwartz, M. Jolicoeur, ภาวะความเข้มข้นสูงกระตุ้น Warburg effect ในเซลล์รังไข่ของหนูแฮมสเตอร์จีนและเผยให้เห็นไมโทคอนเดรียที่ลดลง horsepower, Metabolites 11 (6) (2021).