หน้าหลักนี้ประกอบด้วยเอกสารฉบับแปลของบทความวิชาการต้นฉบับ อย่างไรก็ตาม เรา ได้จัดทำสรุปเนื้อหาที่สำคัญแบบย่อยง่ายไว้ให้ผู้อ่านได้ศึกษาเป็นลำดับแรก เพื่อให้เข้าใจภาพรวมของงานวิจัยชิ้นนี้ได้อย่างรวดเร็ว หากท่านมีความสนใจในรายละเอียดเชิงลึกหรือข้อมูลทางสถิติเพิ่มเติม ท่านสามารถเลือกอ่านเอกสารฉบับเต็มได้ทั้งในรูปแบบภาษาอังกฤษ (Original) ได้ที่ลิงก์นี้: https://www.semanticscholar.org/reader/a29e004fec0292d0bddaa0d616e29a529019a34b หรือหากต้องการอ่านฉบับภาษาไทย (Translated) เราได้จัดทำบทแปลไว้ให้แล้วในหน้านี้ (ล่างสุด)
บทความนี้นำเสนอการศึกษาเกี่ยวกับการใช้สารประกอบคลอรีนไดออกไซด์ (ClO2) และคลอไรต์ (Chlorite) เป็นทางเลือกใหม่ในการรักษาแผลเบาหวานที่เท้า (Diabetic Foot Ulcers – DFUs) ซึ่งเป็นปัญหาทางสาธารณสุขที่สำคัญเนื่องจากมีอัตราการเจ็บป่วยและการเสียชีวิตสูง ผู้วิจัยได้นำเสนอกรณีศึกษาของผู้ป่วย 3 รายที่มีแผลเบาหวานที่เท้าและตอบสนองต่อการรักษาด้วยคลอรีนไดออกไซด์อย่างมีนัยสำคัญ โดยกลไกการทำงานที่สำคัญประกอบด้วยการมีฤทธิ์ต้านจุลชีพที่ครอบคลุมกว้างขวางและปลอดภัยเมื่อใช้ในปริมาณต่ำ ช่วยลดระดับน้ำตาลในเลือดและภาวะน้ำตาลในเลือดสูง ซึ่งส่งผลดีต่อระบบหลอดเลือดโดยการเพิ่มการสร้างหลอดเลือดใหม่ (Angiogenesis) และเพิ่มแรงดันออกซิเจนในเนื้อเยื่อ
นอกจากนี้ สารดังกล่าวยังช่วยลดการอักเสบ ป้องกันการติดเชื้อ และกระตุ้นการสร้างเนื้อเยื่อใหม่ (Granulation tissue) ทำให้แผลหายเร็วขึ้นและฟื้นฟูเนื้อเยื่อให้กลับมาสมบูรณ์ ผลการศึกษาพบว่าผู้ป่วยทั้ง 3 รายมีการหายของแผลอย่างสมบูรณ์หลังการรักษา โดยไม่พบความเป็นพิษต่อระบบร่างกายเมื่อได้รับในโดสที่เหมาะสมตามที่กำหนด
ข้อมูลการเผยแพร่
-
ชื่อบทความ: Chlorine dioxide and chlorite as treatments for diabetic foot (หรือในบางฐานข้อมูลใช้ชื่อว่า Chlorine dioxide treatment for diabetic foot ulcers: Three case studies)
-
ผู้เขียน: Patricia Callisperis, Raul Pineda Aquino, Manuel Aparicio-Alonso, Mitchell Liester
อุบัติการณ์ของโรคเบาหวานทั่วโลกกำลังเพิ่มสูงขึ้น และคาดว่าจะเกิน 10% ภายในปี 2030 แผลที่เท้าเป็นภาวะแทรกซ้อนที่พบบ่อยของโรคเบาหวาน การรักษาแผลที่เท้าจากเบาหวานที่มีอยู่มีประสิทธิภาพเพียง
บางส่วนเท่านั้น และเมื่อแผลเหล่านี้ไม่หาย อาจส่งผลให้ต้องตัดอวัยวะส่วนที่ได้รับผลกระทบออก มีการประมาณการว่ามีการตัดอวัยวะเนื่องจากการติดเชื้อที่เท้าจากเบาหวานเกิดขึ้นทุกๆ 30 วินาทีในที่ใดที่หนึ่งของโลก ดังนั้นจึงจำเป็นต้องมีการรักษาที่มีประสิทธิภาพมากขึ้น หนึ่งในวิธีการรักษาที่เป็นไปได้คือคลอรีนไดออกไซด์ ซึ่งเป็นสารประกอบทางเคมีที่มีแนวโน้มที่ดีในการรักษาแผลที่เท้าจากเบาหวาน
การวิจารณ์วรรณกรรมพบกลไกหลายอย่างที่คลอรีนไดออกไซด์และสารประกอบที่เกี่ยวข้องอย่างคลอไรต์อาจช่วยในการรักษาแผลที่เท้าจากเบาหวาน ซึ่งรวมถึงการลดระดับน้ำตาลในเลือด ลดความเครียดจากออกซิเดชั่น ปรับปรุงภาวะหลอดเลือดผิดปกติ ชะลอการลุกลามของโรคเส้นประสาท ลดการอักเสบ รักษาการติดเชื้อ และปรับปรุงการสมานแผล พบว่าคลอรีนไดออกไซด์และคลอไรต์มีความปลอดภัยและมีประสิทธิภาพเมื่อใช้ในปริมาณต่ำ แนะนำให้ทำการวิจัยเพิ่มเติมเกี่ยวกับประโยชน์ที่เป็นไปได้ของคลอรีนไดออกไซด์และคลอไรต์ในการรักษาแผลที่เท้าของผู้ป่วยเบาหวาน
คำสำคัญ: โรคเบาหวาน, ภาวะเครียดออกซิเดชัน, โรคหลอดเลือด, โรคเส้นประสาท, การติดเชื้อ
บทนำ
โรคเบาหวาน (DM) เป็นโรคทางเมตาบอลิซึมและการอักเสบที่ส่งผลกระทบต่อผู้คนหลายล้านคนทั่วโลก โรคเบาหวานมีลักษณะเฉพาะคือภาวะน้ำตาลในเลือดสูง ซึ่งกระตุ้นวิถีการส่งสัญญาณทางเมตาบอลิซึมที่รับผิดชอบต่อภาวะแทรกซ้อนของโรคเบาหวาน (Volpe et al., 2018) ภาวะแทรกซ้อนที่พบบ่อยอย่างหนึ่งคือการติดเชื้อที่เท้า (Fard et al., 2007)
แผลเบาหวานที่เท้า (DFUs) หมายถึง รอยโรคที่เท้า ซึ่งอาจส่งผลกระทบต่อผิวหนัง เนื้อเยื่ออ่อน และกระดูกในส่วนล่างของร่างกาย ทำให้เกิดการติดเชื้อที่รุนแรงขึ้นในผู้ป่วยเบาหวาน (Ramirez-Acuña et al., 2019) ปัจจัยที่ส่งผลต่อการเกิด DFUs ได้แก่ ภาวะน้ำตาลในเลือดสูง โรคหลอดเลือด โรคเส้นประสาทส่วนปลาย การติดเชื้อ การอักเสบเรื้อรัง และการสมานแผลที่บกพร่อง (Davis et al., 2018; Marston, 2006; Ramirez-Acuña et al., 2019; Singhet al., 2005)
แผลเบาหวานเป็นปัญหาสาธารณสุขระดับโลกที่รุนแรงขึ้นเรื่อยๆ เนื่องจากจำนวนผู้ป่วยโรคเบาหวานเพิ่มขึ้น (Yingsakmongkol et al., 2011) ประมาณการอัตราการแพร่ระบาดของโรคเบาหวานทั่วโลกอยู่ที่ 9.3% (463 ล้านคน) ในปี 2019 และคาดว่าจะเพิ่มขึ้นเป็น 10.2% (578 ล้านคน) ในปี 2030 และ 10.9% (700 ล้านคน) ในปี 2045 (Saeedi et al., 2019)
อุบัติการณ์ของแผลที่เท้าในผู้ป่วยเบาหวานอยู่ที่ 4 ถึง 10% และความเสี่ยงตลอดชีวิตในการเกิดการติดเชื้ออยู่ที่ 25% (Singh et al., 2005; Richard and Schuldiner, 2008) ภาวะแทรกซ้อนที่เท้าเป็นสาเหตุที่พบบ่อยที่สุดของการเจ็บป่วยในผู้ป่วยเบาหวานและเป็นสาเหตุที่พบบ่อยที่สุดของการเข้ารักษาในโรงพยาบาล (Kruse and Edelman, 2006; Lim et al., 2017) ผู้ป่วยเบาหวานหลายรายต้องได้รับการตัดขา ซึ่งส่งผลให้คุณภาพชีวิตแย่ลงมากและมีอัตราการเสียชีวิตภายใน 5 ปีที่ใกล้เคียงหรือแย่กว่ามะเร็งลำไส้ใหญ่ มะเร็งเต้านม และมะเร็งต่อมลูกหมาก (Armstrong et al., 2007)
สมาคมโรคติดเชื้อแห่งอเมริกา (IDSA) แนะนำการรักษาแผลเบาหวานที่เท้าด้วยยาปฏิชีวนะ เพื่อรักษาการติดเชื้อ การทำแผลอย่างเหมาะสมและการลดแรงกดทับที่แผล และการฟื้นฟูหลอดเลือดหากมีภาวะขาดเลือด
(Lipsky et al., 2012) Lim et al. (2017) ยังแนะนำให้ลดระดับน้ำตาลในเลือดด้วย แม้ว่ากลยุทธ์เหล่านี้จะมีประโยชน์ แต่ก็มีประสิทธิภาพเพียงบางส่วนเท่านั้น และแผลเบาหวานที่เท้าที่ไม่หายอาจส่งผลให้ต้องตัดแขนขาข้างที่ได้รับผลกระทบ การตัดแขนขาเกิดขึ้นบ่อยกว่าในผู้ป่วยเบาหวาน 10 ถึง 30 เท่าเมื่อเทียบกับประชากรทั่วไป และมีการประมาณการว่ามีการตัดแขนขาทุกๆ 30 วินาทีสำหรับผู้ป่วยเบาหวานคนใดคนหนึ่งใน
โลก (Richard and Schuldiner, 2008; Singh et al., 2005) อัตราการเสียชีวิตหลังการตัดแขนขาอยู่ที่ 20% ใน 1 ปี 41% ใน 3 ปี และ 63-73% ใน 5 ปี (Apelqvist et al., 1993; Jupiter et al., 2016) ซึ่งเน้นย้ำถึงความสำคัญของการค้นหาวิธีการรักษาแผลเบาหวานที่เท้าที่มีประสิทธิภาพมากขึ้น
คลอรีนไดออกไซด์ (Al-Bayaty et al., 2012; Mawas et al., 2022) และคลอไรต์ (Maraprygsavan et al., 2016; Yingsakmongkol, 2013) ได้รับการแนะนำว่าสามารถช่วยในการรักษาแผลเบาหวานได้
วิธีการ
นี่คือบทความทบทวนเชิงบรรยายที่สำรวจการใช้คลอรีนไดออกไซด์และคลอไรต์ในการรักษาแผลที่เท้าจากโรคเบาหวาน ได้มีการค้นหาเอกสารทางวิชาการเพื่อหาการศึกษาที่ตรวจสอบพยาธิสรีรวิทยาหรือการรักษาแผลที่เท้าจากโรคเบาหวาน รวมถึงการใช้คลอรีนไดออกไซด์หรือคลอไรต์ในการรักษาแผลที่เท้าจากโรคเบาหวานหรือแผลประเภทอื่นๆ ฐานข้อมูล Pubmed, Cochrane และ Google Scholar ถูกค้นหาโดยใช้คำต่อไปนี้: “chlorine dioxide,” “chlorite,” “WF10,” “NP001” “diabetic foot ulcer,” “diabetic foot infection,” “wound healing,” “safety,” และ “pathophysiology” คำเหล่านี้ถูกค้นหาทีละคำและรวมกัน นอกจากนี้ ส่วนอ้างอิงของบทความยังได้รับการตรวจสอบเพื่อหาเอกสารที่มีข้อมูลที่เกี่ยวข้องกับหัวข้อของเรา เราได้รวมการศึกษาในหลอดทดลองและในร่างกายที่เกี่ยวข้องกับทั้งสัตว์และมนุษย์ ข้อมูลจากแหล่งข้อมูลเหล่านี้ที่เกี่ยวข้องกับวัตถุประสงค์ที่กล่าวถึงข้างต้น ได้ถูกนำมารวมไว้ในบทวิจารณ์เชิงบรรยายแล้ว
พยาธิสรีรวิทยาของ DFUS
ในผู้ป่วยโรคเบาหวาน ปัจจัยหลายอย่างเป็นปัจจัยเสี่ยงหรือมีส่วนทำให้เกิดแผลเบาหวาน (ภาพที่ 1) ในภาวะน้ำตาลในเลือดสูง ความเครียดจากออกซิเดชันมีส่วนทำให้เกิดความผิดปกติของหลอดเลือด เส้นประสาท และการทำงานของระบบภูมิคุ้มกันบกพร่อง (Marston, 2006; Markuson et al., 2009) เมื่อเกิดแผลที่ผิวหนังขึ้น ไม่ว่าจะเป็นผลมาจากความผิดปกติของเส้นประสาทส่วนปลายหรือบาดแผลที่เกิดจากอุบัติเหตุ จุลินทรีย์จะเข้าไปอาศัยและเจริญเติบโตในบาดแผล ทำให้เกิดความเสียหายต่อเนื้อเยื่อและกระตุ้นการตอบสนองของร่างกายพร้อมกับการอักเสบ การติดเชื้อทางคลินิกนี้สามารถแพร่กระจายไปยังเนื้อเยื่อรอบข้างได้ (Lipsky et al., 2012)
ภาวะน้ำตาลในเลือดสูง ภาวะเครียดออกซิเดชัน และโรคหลอดเลือด
การสัมผัสกับภาวะน้ำตาลในเลือดสูงเป็นเวลานานเป็นปัจจัยหลักที่ก่อให้เกิดแผลเบาหวาน (Aronson และ Rayfield, 2002) ภาวะน้ำตาลในเลือดสูงทำให้เกิดการเปลี่ยนแปลงหลายอย่างในเนื้อเยื่อหลอดเลือด ซึ่งรวมกันเพื่อเร่งการเกิดภาวะหลอดเลือดแดงแข็ง ซึ่งเป็นหนึ่งในกลไกทางพยาธิสรีรวิทยาหลักที่ก่อให้เกิดโรคหลอดเลือดในผู้ป่วยเบาหวาน (Aronson, 2008)
ในเนื้อเยื่อหลอดเลือด ความเครียดจากออกซิเดชันจะเร่งการเกิดภาวะหลอดเลือดแดงแข็ง ความเครียดจากออกซิเดชันอาจเกิดจากการผลิตสารอนุมูลอิสระ (ROS) มากเกินไป หรือการลดลงของกลไกการป้องกันสารต้านอนุมูลอิสระ (Wei et al., 2009)
ในโรคเบาหวาน ภาวะน้ำตาลในเลือดสูงจะกระตุ้นวิถีการส่งสัญญาณเมตาบอลิซึมที่เพิ่มความเครียดจากออกซิเดชัน (King และ Loeken, 2004; Pang et al., 2020; Volpe et al., 2018) หนึ่งในวิถีเหล่านี้คือการเกิดออกซิเดชันเอง ซึ่งกลูโคสจะเกิดการเอนอไลซ์ ทำให้โมเลกุลออกซิเจนลดลงและได้อนุมูลซูเปอร์ออกไซด์ (O2-) อนุมูลไฮดรอกซิล (•OH) และไฮโดรเจนเปอร์ออกไซด์ (H2O2) (Wolff และ Dean, 1987; Nishikawa et al., 2000) วิถีที่สองเกี่ยวข้องกับการผลิตผลิตภัณฑ์ขั้นสุดท้ายของการเกิดไกลเคชันขั้นสูง (AGEs) AGEs เป็นกลุ่มของสารประกอบที่เป็นผลิตภัณฑ์ของปฏิกิริยาที่ไม่ใช้เอนไซม์ระหว่างน้ำตาลรีดิวซิงและ โปรตีน ไขมัน หรือกรดนิวคลีอิก (Prasad et al., 2019) AGEs จับกับตัวรับสำหรับผลิตภัณฑ์ขั้นสุดท้ายของการเกิดไกลเคชั่นขั้นสูง (RAGEs) ซึ่งกระตุ้นให้เกิดการผลิต ROS มากเกินไป (Goldin et al, 2006)
เส้นทางที่สามเกี่ยวข้องกับการเพิ่มขึ้นของการผลิต ROS ภายในเซลล์ที่เกิดจากภาวะน้ำตาลในเลือดสูง ผ่านทางห่วงโซ่การขนส่งอิเล็กตรอนของไมโทคอนเดรีย (Nishikawa et al., 2000) เส้นทางที่สี่เกี่ยวข้องกับการสร้างซูเปอร์ออกไซด์ที่เพิ่มขึ้นโดยโมโนไซต์ที่ถูกกระตุ้น หลังจากที่โมโนไซต์เคลื่อนตัวออกจากหลอดเลือดเข้าไปในผนังหลอดเลือด จะเกิดการปล่อยซูเปอร์ออกไซด์ออกมาอย่างรวดเร็วผ่านการกระตุ้นของ NADPH oxidase (NOX) การเพิ่มขึ้นของซูเปอร์ออกไซด์นี้มีส่วนทำให้เกิดภาวะหลอดเลือดแดงแข็ง โดยมีส่วนร่วมในการออกซิเดชันของไลโปโปรตีนความหนาแน่นต่ำ (LDL) ซึ่งนำไปสู่การก่อตัวของเซลล์โฟม และการพัฒนาของภาวะหลอดเลือดแดงแข็ง (Cathcart, 2004) ภาวะน้ำตาลในเลือดสูงยังสามารถเพิ่มความเครียดจากออกซิเดชันได้โดยการลดกิจกรรมการกำจัดกลูตาไธโอนและลดปริมาณ NADPH ในเนื้อเยื่อบุผนังหลอดเลือด (Kashiwagi et al., 1996)
ความเครียดออกซิเดชันที่เพิ่มขึ้นจะกระตุ้นการทำงานของเส้นทางการส่งสัญญาณหลายเส้นทางที่เกี่ยวข้องกับการเกิดโรคของแผลเบาหวาน ซึ่งรวมถึงการกระตุ้นเส้นทางโพลีออล (Pang, 2020) การผลิต AGEs และ RAGEs ที่เพิ่มขึ้นการกระตุ้นระบบโปรตีนไคเนสซี (PKC) (Aronson และ Rayfield, 2002) การทำงานมากเกินไปของเส้นทางเฮกโซซามีน (Aronson, 2008) การปล่อยไซโตไคน์ที่ก่อให้เกิดการอักเสบ (Rask-Madsen และ King, 2013; Thiruvoipati et al., 2015) และการยับยั้งเอนไซม์ต้านหลอดเลือดแข็งตัว เช่น eNOS และพรอสตาไซคลินซินเทส ผ่านกลไกเหล่านี้ ความเครียดจากออกซิเดชันจะลดระดับไนตริกออกไซด์ ทำลายโปรตีนในเซลล์ ส่งเสริมการยึดเกาะของเม็ดเลือดขาวกับเยื่อบุหลอดเลือด และเพิ่มการอักเสบ (Sheetz and King, 2002) การเปลี่ยนแปลงเหล่านี้ส่งเสริมการพัฒนาของหลอดเลือดแดงแข็ง ซึ่งนำไปสู่โรคหลอดเลือดแดงส่วนปลาย (PAD) ภาวะขาดเลือด และในที่สุดก็ทำให้เกิดแผลเบาหวาน
การอักเสบและระบบภูมิคุ้มกันมีบทบาทสำคัญในการพัฒนาของหลอดเลือดแดงแข็ง โดยทั้งระบบภูมิคุ้มกันโดยกำเนิดและระบบภูมิคุ้มกันแบบปรับตัวมีส่วนร่วมการเกิดหลอดเลือดแดงแข็งมีลักษณะเฉพาะคือการสะสมเรื้อรังของโมโนไซต์/แมโครฟาจที่ผลิต ROS และปล่อยไซโตไคน์ที่ก่อให้เกิดการอักเสบภายในผนังหลอดเลือดแดง โมโนไซต์จะเปลี่ยนแปลงในบริเวณนั้นไปเป็นแมโครฟาจที่กิน LDL ที่ถูกออกซิไดซ์ จึงกลายเป็นเซลล์โฟมที่ก่อตัวเป็นคราบพลัค ซึ่งนำไปสู่หลอดเลือดแดงแข็ง (Li et al., 2017)
การตอบสนองทางภูมิคุ้มกันแบบปรับตัวมีส่วนช่วยในการพัฒนาของหลอดเลือดแดงแข็งตัวเมื่อลิมโฟไซต์เคลื่อนตัวผ่านผนังหลอดเลือดแดงซึ่งแมโครฟาจจะนำเสนอส่วนประกอบโปรตีนของอนุภาค LDL ให้กับทีลิมโฟไซต์ ทำให้เกิดการผลิตไซโตไคน์ที่ก่อให้เกิดการอักเสบ นอกจากนี้ เซลล์ B2 ยังผลิตแอนติบอดี IgG ซึ่งส่งเสริมหลอดเลือดแดงแข็งตัวโดยการมีส่วนร่วมในการกระตุ้นเซลล์ T CD4 และกระตุ้นการเพิ่มจำนวนของเซลล์ T ที่ทำหน้าที่ (Li และคณะ, 2017)
โรคเส้นประสาท
ภาวะแทรกซ้อนของหลอดเลือดขนาดเล็กที่พบบ่อยที่สุดในโรคเบาหวานคือโรคเส้นประสาท ประมาณ 50% ของผู้ป่วยโรคเบาหวาน จะมีอาการเส้นประสาทส่วนปลายเสื่อมภายใน 25 ปีหลังจากเริ่มมีอาการ และโรคเส้นประสาทเป็นสาเหตุของแผลเบาหวานที่เท้า 50% (Vincent et al., 2004; Volmer-Thole and Lobmann, 2016) แผลเบาหวานที่เท้าส่วนใหญ่เกิดจากการบาดเจ็บเล็กน้อยในขณะที่มีโรคเส้นประสาทรับความรู้สึก ซึ่งทำให้ความรู้สึกเจ็บปวดลดลง ส่งผลให้การบาดเจ็บอาจไม่ถูกสังเกตเห็นเป็นเวลาหลายสัปดาห์ (McNeely et al., 1995; Volmer-Thole and Lobmann, 2016)
ภาวะเครียดออกซิเดชันมีบทบาทสำคัญในพยาธิสรีรวิทยาของโรคเส้นประสาทเบาหวาน (Feldman, 2003) ภาวะเครียดออกซิเดชันทำให้เกิดความผิดปกติของรูปร่างแอกซอน การเปลี่ยนแปลงการซึมผ่านของเยื่อหุ้มเซลล์ประสาท และการเปลี่ยนแปลงของโปรตีนในเซลล์ต่างๆ (Negi et al., 2011) ภาวะเครียดออกซิเดชันยังเกี่ยวข้องกับการเกิดอะพอพโทซิสในเซลล์ประสาทและเซลล์เกลียที่คอยสนับสนุน (Vincent et al., 2004) การลดระดับน้ำตาลในเลือด ซึ่งช่วยลดภาวะเครียดออกซิเดชัน จะช่วยลดความเสี่ยงของโรคเส้นประสาท (Rask-Madsen and King, 2013)
การทำงานของระบบภูมิคุ้มกันบกพร่องและการอักเสบเพิ่มขึ้น
ภาวะน้ำตาลในเลือดสูงและความเครียดจากออกซิเดชันยังส่งผลต่อแผลเบาหวาน โดยทำให้การทำงานของระบบภูมิคุ้มกันบกพร่องและเพิ่มการอักเสบ ระดับน้ำตาลในเลือด >150 มก./ดล. มีความสัมพันธ์กับการทำงานของระบบภูมิคุ้มกันที่บกพร่อง (Syafril, 2018) กลไกที่ภาวะน้ำตาลในเลือดสูง ทำให้การทำงานของระบบภูมิคุ้มกันบกพร่อง ได้แก่ การทำงานของเม็ดเลือดขาวชนิดโพลีมอร์โฟนิวเคลียร์ (PMN) ที่บกพร่อง เช่น
การเคลื่อนที่ การอพยพ การยึดเกาะ การกลืนกิน และ การฆ่าเชื้อภายในเซลล์ การทำงานของโมโนไซต์และแมโครฟาจที่บกพร่อง และจำนวนลิมโฟไซต์ CD4 T ที่ลดลง ส่งผลให้สัดส่วน CD4/CD8 ลดลง ภาวะน้ำตาลในเลือดสูงยังกระตุ้นให้เกิดการเพิ่มขึ้นของไซโตไคน์ที่ก่อให้เกิดการอักเสบ (McMahon and Bistrian, 1995)
การติดเชื้อ
ในผู้ป่วยเบาหวาน ระดับน้ำตาลในเลือดที่สูงขึ้นมีความสัมพันธ์กับความเสี่ยงต่อการติดเชื้อที่เพิ่มขึ้น ปัจจัยที่ส่งผลต่อความเสี่ยงที่เพิ่มขึ้นนี้ ได้แก่ ภาวะเนื้อเยื่อขาดออกซิเจน และระบบภูมิคุ้มกันของร่างกายที่บกพร่อง (Pozilli และ Leslie, 1994) อย่างหลังเป็นผลมาจากการปล่อยอินเตอร์ลิวคิน-1 (IL-1) จากแมโครฟาจที่บกพร่อง และการทำงานของเม็ดเลือดขาวชนิด PMN ที่บกพร่อง รวมถึงการเคลื่อนที่ที่ลดลง การเคลื่อนที่ตามสารเคมีที่บกพร่อง และกิจกรรมการกลืนกินที่ลดลง (Butler et al., 2005) การติดเชื้อส่งผลให้ระยะเวลาในการสมานแผลเพิ่มขึ้น (Marston, 2006)
การสมานแผลและ ROS
โดยทั่วไปแล้ว การสมานแผลจะถูกมองว่าเกิดขึ้นใน 4 ขั้นตอน ได้แก่ การแข็งตัวของเลือด การอักเสบ การเพิ่มจำนวนเซลล์ และการเจริญเติบโตเต็มที่ ROS มีบทบาทสำคัญในแต่ละขั้นตอนเหล่านี้ สำหรับแผลเบาหวาน กลไกที่ ROS มีอิทธิพลต่อการสมานแผลนั้นได้รับการศึกษามาเป็นอย่างดีแล้ว
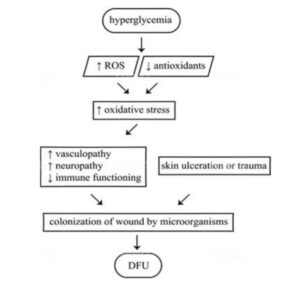
ภาพที่ 1. พยาธิสรีรวิทยาของแผลที่เท้าในผู้ป่วยเบาหวาน
ที่มา: Yosuf/fiverr
ROS ถูกสร้างขึ้นโดยเซลล์หลอดเลือดทุกชนิด แต่แหล่งกำเนิดหลักสองแหล่งในหลอดเลือดคือห่วงโซ่การขนส่งอิเล็กตรอนของไมโทคอนเดรียและนิโคตินาไมด์อะดีนีนไดนิวคลีโอไทด์ฟอสเฟต (NADPH) ออกซิเดส (NOX) NOX สร้างซูเปอร์ออกไซด์โดยการถ่ายโอนอิเล็กตรอนจาก NADPH ไปยังออกซิเจน ไมโทคอนเดรียผลิตซูเปอร์ออกไซด์ผ่านห่วงโซ่การขนส่งอิเล็กตรอน (ETC) และซูเปอร์ออกไซด์จะถูกเปลี่ยนเป็นไฮโดรเจนเปอร์ออกไซด์ (H2O2) โดยเอนไซม์ซูเปอร์ออกไซด์ดิสมิวเทส (SOD2) (ภาพที่ 2)
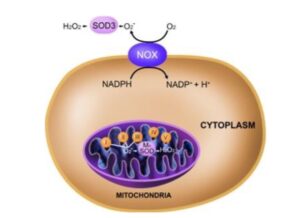
ภาพที่ 2 การสร้างสารออกซิเจนที่ว่องไวต่อปฏิกิริยา
ที่มา: ภาพประกอบโดย Huțanu Alexandru Adrian
การลดความเครียดจากออกซิเดชัน ไม่ว่าจะโดยการลดการผลิตซูเปอร์ออกไซด์ที่มากเกินไป หรือการเพิ่มกิจกรรมของสารต้านอนุมูลอิสระ ได้รับการเสนอแนะว่าเป็นกลยุทธ์ในการลดภาวะแทรกซ้อนของโรคเบาหวาน อย่างไรก็ตาม สารต้านอนุมูลอิสระแบบดั้งเดิมไม่ได้ผลดีในเรื่องนี้ มีการเสนอแนะว่านี่อาจเป็นเพราะสารเหล่านี้กำจัด ROS ในลักษณะที่เป็นสัดส่วน หรืออีกทางหนึ่งอาจเป็นเพราะสารต้านอนุมูลอิสระจากภายนอกอาจถูกทำให้ไม่ทำงานก่อนที่จะไปถึงหลอดเลือด การกระตุ้นระบบต้านอนุมูลอิสระภายในร่างกาย หรือการใช้สารเลียนแบบ SOD หรือ catalase ได้รับการเสนอแนะว่าอาจมีประสิทธิภาพมากกว่าการให้สารต้านอนุมูลอิสระจากภายนอก (Brownlee, 2001; Wassmann et al., 2004)
ในโรคเบาหวาน ระดับกลูโคสในเลือดที่สูงขึ้นจะเพิ่มการผลิตซูเปอร์ออกไซด์ในไมโทคอนเดรีย (บราวน์ลี, 2001) การเพิ่มขึ้นของซูเปอร์ออกไซด์จะทำให้การสมานแผลช้าลง ในขณะที่การลดซูเปอร์ออกไซด์จะช่วยเร่งการสมานแผล (ลั่วและคณะ, 2004) กลยุทธ์หนึ่งที่แนะนำเพื่อลดระดับซูเปอร์ออกไซด์คือการเพิ่มการเปลี่ยนซูเปอร์ออกไซด์เป็นไฮโดรเจนเปอร์ออกไซด์โดยการเพิ่มกิจกรรมของเอนไซม์ซูเปอร์ออกไซด์ดิสมิวเทส (SOD) (บราวน์ลี, 2001)
ไฮโดรเจนเปอร์ออกไซด์มีอิทธิพลต่อการสมานแผลผ่านกลไกหลายประการ ซึ่งรวมถึงการเปลี่ยนแปลงการสร้างหลอดเลือดใหม่ การแทรกซึมของนิวโทรฟิล การเคลื่อนที่ของไฟโบรบลาสต์ และการกระตุ้นไมโอไฟโบรบลาสต์ (Fujiwara et al., 2013) ผลกระทบของไฮโดรเจนเปอร์ออกไซด์ต่อการสมานแผลบางส่วนขึ้นอยู่กับความเข้มข้น ตัวอย่างเช่น ความเข้มข้นต่ำ (0.1-10 μM) ส่งเสริมการสร้างหลอดเลือดใหม่ ในขณะที่ความเข้มข้นสูง (>125 μM) ยับยั้งการสร้างหลอดเลือดใหม่และทำให้เซลล์เยื่อบุหลอดเลือดเสียหาย (Huang and Zheng, 2006; Yasuda et al., 1998) ปัจจัยที่ส่งผลต่อระดับไฮโดรเจนเปอร์ออกไซด์และส่งผลต่อการสร้างหลอดเลือดใหม่แสดงอยู่ในตารางที่ 1
ตารางที่ 1 ปัจจัยที่มีอิทธิพลต่อการสร้างหลอดเลือดใหม่

↑ = เพิ่มขึ้น; ↑↑ = เพิ่มขึ้นมาก; ↓ = ลดลง
ที่มา: Huang Zheng (2006), Yasuda et al. (1998) และ Brownlee (2001)
การกระตุ้นการสร้างหลอดเลือดใหม่โดยไฮโดรเจนเปอร์ออกไซด์ต้องอาศัยปัจจัยส่งเสริมการสร้างหลอดเลือดใหม่ เช่น ปัจจัยการเจริญเติบโตของหลอดเลือด (VEGF) และปัจจัยการเปลี่ยนแปลงการเจริญเติบโต-β-1 (TGF-β-1) (Kim และ Byzofa, 2014) VEGF กระตุ้นการสร้างหลอดเลือดใหม่ ซึ่งช่วยฟื้นฟูการไหลเวียนโลหิตในเนื้อเยื่อและการปล่อยออกซิเจน จึงช่วยปรับปรุงความผิดปกติทางเมตาบอลิซึมของสภาพแวดล้อมบาดแผล (Detmar et al., 1977) TGF-β-1 มีอิทธิพลต่อการทำงานของเซลล์หลายอย่าง รวมถึงการเพิ่มจำนวน การแบ่งตัวการเคลื่อนที่ และการตายของเซลล์ ไซโตไคน์นี้ยังควบคุมการสร้างหลอดเลือดใหม่ เสริมสร้างการซ่อมแซมเนื้อเยื่อที่ได้รับบาดเจ็บ และส่งเสริมการสมานแผล (Chin, 2004)
จากที่ได้กล่าวถึงการอภิปรายก่อนหน้านี้เกี่ยวกับพยาธิสรีรวิทยาของแผลเบาหวาน สารที่เหมาะสมที่สุดในการรักษาแผลเบาหวานคือสารที่ช่วยลดระดับน้ำตาลในเลือด ลดซูเปอร์ออกไซด์ในขณะที่เพิ่มไฮโดรเจนเปอร์ออกไซด์ให้อยู่ในระดับที่ช่วยลดความเครียดจากออกซิเดชัน กระตุ้นการสร้างหลอดเลือดใหม่ ลดอาการทางประสาท ลดการอักเสบ รักษาการติดเชื้อ และฟื้นฟูการทำงานของระบบภูมิคุ้มกันให้เป็นปกติ สารหนึ่งที่ดูมีแนวโน้มที่ดีในด้านนี้คือคลอรีนไดออกไซด์
คลอรีนไดออกไซด์
ประวัติความเป็นมาของคลอรีนไดออกไซด์
คลอรีนไดออกไซด์ (ClO2) เป็นโมเลกุลสังเคราะห์ที่ผลิตขึ้นครั้งแรกในปี ค.ศ. 1802 โดยนักเคมีชาวไอริช ริชาร์ด เชเนวิกซ์ ซึ่งผสมกรดซัลฟิวริกกับโพแทสเซียมคลอเรต (ซิดจ์วิก, 1950) เกือบสิบปีต่อมา เซอร์ ฮัมฟรีย์ เดวี ได้ผสมโพแทสเซียมคลอเรตกับกรดไฮโดรคลอริกและผลิตก๊าซที่เขาเรียกว่า “ยูคลอรีน” ซึ่งประกอบด้วยส่วนผสมของ ClO2 และคลอรีน (เดวี, 1832)
ในช่วงครึ่งหลังของศตวรรษที่ 19 ClO2 ถูกนำมาใช้ในการบำบัดน้ำในยุโรป (Benarde et al., 1965) หลังจากการศึกษาในช่วงทศวรรษ 1940 และ 1950 แสดงให้เห็นว่าประสิทธิภาพในการฆ่าเชื้อโรคในวงกว้างของ ClO2 นั้นอย่างน้อยก็เท่ากับ หรืออาจจะเหนือกว่าคลอรีน การใช้สารนี้จึงขยายตัวมากขึ้น ในช่วงทศวรรษ 1970 โรงบำบัดน้ำมากกว่า 500 แห่งทั่วโลกใช้ ClO2 ในการทำน้ำให้บริสุทธิ์ (Clarke and Berman, 1983)
ปัจจุบัน นอกจากใช้ในการบำบัดน้ำแล้ว ClO2 ยังถูกนำไปใช้เป็นสารกำจัดเม็ดสีสำหรับเยื่อไม้ (Gall, 1978) แป้ง (Fukayama et al., 1986) และสิ่งทอ (Jonnalagadda และ Nadupalli, 2014) สารฆ่าเชื้อในอุตสาหกรรมอาหารและเครื่องดื่ม (Drechsler et al., 1990; Gómez-López และคณะ, 2009) สารฆ่าเชื้อในทางการแพทย์ (Lowe et al., 2013) สารรักษาอาการปากเหม็น (Frascella et al., 2000) และสารดับกลิ่นในห้อง (Ogata และ Shibata, 2009) ClO2 ยังถูกนำมาใช้ในการทำความสะอาดเอกสารโบราณ (Gettens, 1952), ทำลายสารชีวภาพที่ใช้ในการสงคราม (Gordon and Rosenblatt, 2005), ยืดอายุขัยของผึ้ง (Lackett et al., 1972) และเป็นยาที่หาซื้อได้ทั่วไปสำหรับรักษาการติดเชื้อไวรัส แบคทีเรีย และเชื้อรา (Frontier Pharmaceutical, Inc.) นอกจากนี้ ClO2 ยังถูกแนะนำให้ใช้เป็นสารฆ่าเชื้อสำหรับไวรัส SARS-CoV-2 ที่ก่อให้เกิด COVID-19 (Ogata and Miura, 2020) รวมถึงการป้องกันและรักษา COVID-19 (Ogata and Miura 2021; Aparicio-Alonso et al., 2021) เนื่องจากมีความปลอดภัยและมีประสิทธิภาพในวงกว้าง ClO2 จึงถูกขนานนามว่าเป็น “สารฆ่าเชื้อที่เหมาะสมที่สุด” (Simpson et al., 1993)
หนึ่งในการประยุกต์ใช้ ClO2 ที่เกิดขึ้นเมื่อไม่นานมานี้คือการรักษาแผลเบาหวาน บทความนี้จะทบทวนเหตุผลในการใช้ ClO2 ในการรักษาแผลเบาหวาน
เคมีของคลอรีนไดออกไซด์
ClO2 เป็นโมเลกุลสมมาตรที่มีอะตอม 3 อะตอม ประกอบด้วยอะตอมคลอรีน 1 อะตอมและอะตอมออกซิเจน 2 อะตอม ที่อุณหภูมิห้อง ClO2 เป็นก๊าซสีเหลืองที่ละลายน้ำได้ดีมาก
(PubChem, 2018)
ClO2 จะสลายตัวอย่างรวดเร็วในอุณหภูมิสูงและอาจเกิดการสลายตัวด้วยแสง โดยเฉพาะอย่างยิ่งด้วยแสงอัลตราไวโอเลต ในอากาศ โมเลกุลนี้จะสลายตัวเป็นก๊าซคลอรีนและออกซิเจน ในขณะที่ในน้ำจะค่อนข้างเสถียรอย่างไรก็ตาม ที่ค่า pH สูงกว่า 9 ถึง 10 ClO2 ในน้ำจะเกิดปฏิกิริยาไม่สมดุลเพื่อผลิตไอออนคลอไรต์ (ClO2-) และคลอเรต (ClO3-) (กระทรวงสาธารณสุขและบริการมนุษย์แห่งสหรัฐอเมริกา, 2004)
ClO2 มีจำนวนอิเล็กตรอนเป็นเลขคี่ โดยมีอิเล็กตรอนวาเลนซ์ 19 ตัว อิเล็กตรอนเพียงตัวเดียวครอบครองออร์บิทัลโมเลกุลสูงสุด และอิเล็กตรอนที่ไม่มีคู่ตัวนี้ถูกแบ่งปันระหว่างอะตอมทั้งสามอะตอม ความหนาแน่นของอิเล็กตรอนเดี่ยวส่วนใหญ่จะอยู่ที่อะตอมออกซิเจนอะตอมใดอะตอมหนึ่ง การจัดเรียงตัวที่เป็นเอกลักษณ์นี้ทำให้ ClO2 มีอิเล็กตรอนที่ไม่มีคู่เพียงตัวเดียว และมีศูนย์กลางปฏิกิริยาสองแห่ง (ออกซิเจนและคลอรีน) ที่สามารถทำปฏิกิริยาได้ อิเล็กตรอนที่ไม่มีคู่เพียงตัวเดียวทำให้โมเลกุลเป็นอนุมูลอิสระ ซึ่งช่วยอธิบายธรรมชาติที่ว่องไวต่อปฏิกิริยาของมัน (Flesch et al., 2006) ClO2 ยังเป็นสารออกซิไดซ์ที่มีปฏิกิริยาสูง ซึ่งหมายความว่ามันสามารถรับอิเล็กตรอนผ่านปฏิกิริยาออกซิเดชัน-รีดักชันได้
ClO2 เกิดปฏิกิริยาถ่ายโอนอิเล็กตรอนหนึ่งตัวก่อให้เกิดคลอไรต์ (ClO2-) และจึงทำปฏิกิริยาผ่านการออกซิเดชันแทนที่จะเป็นการเติมหรือการแทนที่ ClO2 ทำปฏิกิริยากับสารอินทรีย์ในขอบเขตที่ค่อนข้างแคบ ได้แก่
ไทออล ฟีนอล สารประกอบเฮเทอโรไซคลิกที่มีไนโตรเจน และเอมีนตติยภูมิแบบอะลิฟาติก ClO2 ทำปฏิกิริยากับกรดอะมิโนอิสระได้ง่าย เช่น ซิสเทอีน ไทโรซีน และทริปโตเฟน ในขณะที่กรดอะมิโนอื่นๆ ทำปฏิกิริยาในอัตราที่ช้ากว่ามาก คุณสมบัติเหล่านี้ทำให้ ClO2 สามารถเกิดปฏิกิริยาออกซิเดชันของโมเลกุลอินทรีย์ได้อย่างเฉพาะเจาะจงและค่อนข้างเลือกได้
หลังจากรับอิเล็กตรอนหนึ่งตัว ClO2 จะถูกเปลี่ยนเป็น ClO2- (คลอไรต์) ซึ่งเกิดขึ้นหลังจากการรับประทาน ClO2 เข้าไป คลอไรต์มีอยู่ในยาหลายชนิดในปัจจุบัน รวมถึงสารประกอบเตตระคลอโรเดคาออกซิเจน (TCDO), WF10, OXO-K993, Ryoxon® และ Oxoferin® TCDO เป็นผลิตภัณฑ์จากปฏิกิริยาคลอไรต์-ออกซิเจน ซึ่งประกอบด้วยคลอไรต์ (ClO2-) (4.25%), คลอไรด์ (Cl-) (1.9%), คลอเรต (ClO3-) (1.5%), ซัลเฟต (SO42-) (0.7%) และแอนไอออนโซเดียม (Na+) (Ennen et al., 1993) ไอออนคลอไรต์ ซึ่งได้รับการพิสูจน์แล้วว่าเป็นสารออกฤทธิ์ในยาเหล่านี้ จะถูกเผาผลาญในร่างกายให้กลายเป็นผลิตภัณฑ์ที่ไม่เป็นพิษ (นั่นคือ คลอไรด์ ออกซิเจน และน้ำ) (Schempp และคณะ, 2001)
TCDO ถูกสังเคราะห์ขึ้นครั้งแรกโดย F. W. Kühne เพื่อรักษาแผลเรื้อรังจากหลอดเลือดดำโดยไม่ต้องใช้ยาต้านการติดเชื้อเพิ่มเติม (Hinz et al., 1984a; Tissot et al., 1990) การศึกษาทางคลินิกพบว่า TCDO กระตุ้นการสร้างเนื้อเยื่อแกรนูเลชันและส่งเสริมการสมานแผล (Hinz et al., 1984b) การศึกษาเพิ่มเติมพบว่า TCDO ช่วยเพิ่มการกลืนกินของแมโครฟาจ (Woerly et al., 1986) แสดงคุณสมบัติต้านการอักเสบ (Tissot et al., 1990) ควบคุมภูมิคุ้มกันของเซลล์และสารน้ำ (Gillissen et al., 1986) และกระตุ้นการปล่อย O2 ในสารละลายที่มีฮีโมโกลบิน (Mueller-Klieser and Vaupel, 1987) ยา WF10 (อิมมูโนไคน์) เป็นสารละลายในน้ำของ TCDO ที่ใช้สำหรับการให้ทางหลอดเลือดดำ คลอไรต์เป็นสารออกฤทธิ์ในสารละลายนี้ซึ่งมีคลอไรต์ 63 มิลลิโมล/ลิตร ปฏิกิริยาของ WF10 กับฮีโมโปรตีนได้รับการเสนอแนะว่าเป็นขั้นตอนสำคัญในการกระตุ้นยา (Schempp et al., 2001) ออกโซเฟอรินได้รับการอนุมัติในปี 1983
ในประเทศเยอรมนีสำหรับการใช้เฉพาะที่เพื่อส่งเสริมการรักษาบาดแผลเรื้อรัง เช่น แผลเบาหวานที่เท้า (Hinz et al., 1986; Schempp et al., 2001) OXO-K993 ได้รับการอนุมัติในประเทศไทยเป็นการบำบัดด้วยการให้ยาทางหลอดเลือดดำสำหรับกลุ่มอาการหลังการฉายรังสีและสำหรับการดูแลประคับประคองในผู้ป่วยที่ได้รับการรักษาโรคมะเร็ง (Schempp et al., 2001) เมื่อเกือบ 25 ปีก่อน พบว่า WF10 ช่วยลดอัตราการเข้ารักษาในโรงพยาบาลและอัตราการเสียชีวิตในผู้ป่วยโรคเอดส์ (Raffanti et al., 1998)
ยาอีกชนิดหนึ่งที่เกี่ยวข้องกับหัวข้อนี้คือโซเดียมคลอไรต์ (NaClO2) หรือที่รู้จักกันในชื่อ NP001 โมเลกุลนี้ทำหน้าที่เป็นทั้งสารตั้งต้นสำหรับการผลิต ClO2 และทำหน้าที่เป็นยาที่กำลังได้รับการศึกษาเพื่อรักษาโรคทางระบบประสาทเสื่อม เช่น โรคกล้ามเนื้ออ่อนแรง (ALS) (Miller et al., 2014, 2015)
แม้ว่าจะมีการใช้วิธีการหลายวิธีในการสังเคราะห์ ClO2 แต่หนึ่งในวิธีที่พบมากที่สุดคือการผสมโซเดียมคลอไรต์ (NaClO2) กับกรด เช่น กรดฟอสฟอริก (H3PO4) หรือกรดไฮโดรคลอริก (HCl) (American Chemistry
Council, 2023) NaClO2 เป็นโมเลกุลที่มีโครงสร้างทางเคมี เกี่ยวข้องกับทั้งเกลือแกง (NaCl) และสารฟอกขาว (NaClO)
จลนศาสตร์ของคลอรีนไดออกไซด์และคลอไรต์
การศึกษาเภสัชจลนศาสตร์ของคลอรีนไดออกไซด์และคลอไรต์ในมนุษย์มีน้อยมาก การศึกษาจลนศาสตร์ส่วนใหญ่ดำเนินการในแบบจำลองสัตว์ โดยส่วนใหญ่ในหนู การศึกษาหลายชุดที่ดำเนินการในช่วงทศวรรษ 1970 และ 1980 ได้ตรวจสอบจลนศาสตร์ของ ClO2 ในหนูและไก่โดยใช้สารติดตามกัมมันตรังสี 36ClO2 นักวิจัยพบว่าหลังจากการให้ 36ClO2 ทางปากในหนู กัมมันตภาพรังสีจะถูกดูดซึมอย่างรวดเร็วจากทางเดินอาหาร จากนั้น ClO2 จะถูกเปลี่ยนเป็นคลอไรด์ (Cl-) คลอไรต์ (ClO2-) และคลอเรต (ClO3-) ที่ 12 และ 24 ชั่วโมงหลังจากการให้ ClO2 อัตราส่วนของ ClO2- ต่อ Cl- คือ 1:5 อย่างไรก็ตาม ที่ 72 ชั่วโมง อัตราส่วนในปัสสาวะและพลาสมาเปลี่ยนเป็น 1:4 ClO3-ตรวจพบเฉพาะในปัสสาวะในช่วง 12-24 ชั่วโมง Cl- มีระดับสูงสุดในพลาสมาครึ่งชั่วโมงหลังจากการรับประทาน 36ClO2
ในขณะที่ ClO2- มีระดับสูงสุดในพลาสมาที่ 2 ชั่วโมง ที่ 72 ชั่วโมงหลังการให้ยา การกระจายตัวของ ClO2-มีระดับสูงสุดในเลือดทั้งหมด เม็ดเลือดแดง พลาสมา กระเพาะอาหาร อัณฑะ ผิวหนัง ปอด ไต ลำไส้เล็กส่วนต้น ซากสัตว์ ม้าม ลำไส้เล็กส่วนปลาย สมอง ไขกระดูก และตับ ในส่วนของการกำจัด พบว่าหลังจากการรับประทาน 36ClO2 75% ของขนาดยาที่ตรวจพบพบในปัสสาวะและ 25% พบในอุจจาระ เมื่อศึกษา ClO2- พบว่า 87% และ 13% ของขนาดยาที่ให้ไปพบในปัสสาวะและอุจจาระตามลำดับ ไม่พบสารประกอบ Cl ในลมหายใจ ครึ่งชีวิตของการกำจัดคือ 43.9+2.3 ชั่วโมงสำหรับ ClO2 และ 35.2+3.0 ชั่วโมงสำหรับ ClO2- (Abdel-Rahman, 1979a, 1979b; Couri et al., 1982)
ความปลอดภัย/ความเป็นพิษ
ความปลอดภัยของคลอรีนไดออกไซด์ขึ้นอยู่กับวิธีการใช้และปริมาณ เมื่อใช้ทาภายนอกในปริมาณต่ำ คลอรีนไดออกไซด์จะไม่เป็นพิษ การศึกษาโดยใช้เซลล์ไฟโบรบลาสต์ของม้าพบว่าคลอรีนไดออกไซด์มีความเป็นพิษน้อยกว่าคลอร์เฮกซิดีน ซึ่งเป็นสารละลายฆ่าเชื้อแผลที่ผิวหนังที่ใช้กันทั่วไป (Redding and Booth, 1991) การศึกษาเกี่ยวกับการใช้คลอรีนไดออกไซด์ 50 ppm เป็นสารล้างแผลในมนุษย์พบว่าสารฆ่าเชื้อนี้ปลอดภัยและไม่เกี่ยวข้องกับผลข้างเคียง (Valente et al., 2014)
ชุดการศึกษาในช่วงทศวรรษ 1980 ได้สำรวจความปลอดภัยของคลอรีนไดออกไซด์และคลอไรต์ที่รับประทานทางปาก พบว่าปริมาณต่ำมีความปลอดภัย แต่ปริมาณสูงทำให้เกิดผลข้างเคียง จากการศึกษาเหล่านี้ สำนักงานคุ้มครองสิ่งแวดล้อมแห่งสหรัฐอเมริกา (EPA) ได้กำหนดระดับที่ไม่พบผลข้างเคียง (NOAEL) ไว้ที่ 3 มก./กก./วัน และระดับที่พบผลข้างเคียงต่ำสุด (LOAEL) ไว้ที่ 5.7 มก./กก./วัน สำหรับ ClO2 (EPA 2000) ไม่กี่ปีต่อมา หน่วยงานด้านสารพิษและโรค (ATSDR) ได้ลดระดับ NOAEL ลงเหลือ 2.9 มก./กก./วัน (กระทรวงสาธารณสุขและบริการมนุษย์แห่งสหรัฐอเมริกา, 2004)
การศึกษาในมนุษย์ไม่พบผลเสียใดๆ ในบุคคลที่ดื่มคลอรีนไดออกไซด์หรือคลอไรต์ในความเข้มข้นต่ำ (0.04-0.34 มก./กก./วัน) ในการศึกษาทดลอง (Lubbers et al., 1981, 1982, 1984a, 1984b) หรือดื่มน้ำที่ฆ่าเชื้อด้วยคลอรีนไดออกไซด์ (Tuthill et al., 1982)
การศึกษาเฟส 1 ที่ตรวจสอบความปลอดภัยและความทนทานของการให้โซเดียมคลอไรต์ทางหลอดเลือดดำแบบเฉียบพลัน พบว่า การเพิ่มขนาดยาจนถึง 3.2 มก./กก./วัน โดยทั่วไปมีความปลอดภัยและผู้ป่วยทนได้ดี (มิลเลอร์และคณะ, 2014) ในการศึกษาเฟส 2 แบบหลายศูนย์ แบบสุ่ม และแบบปกปิดสองทาง ซึ่งดำเนินการในภายหลัง โดยมีผู้ป่วยโรคกล้ามเนื้ออ่อนแรง (ALS) จำนวน 136 ราย โซเดียมคลอไรต์ (NP001) 2 มก./กก./วัน ถูกให้ทางหลอดเลือดดำเป็นขนาดยาเดียวต่อวันเป็นเวลา 6 เดือน ผลการศึกษานี้แสดงให้เห็นหลักฐานระดับ 1 ว่าโซเดียมคลอไรต์โดยทั่วไปมีความปลอดภัยและผู้ป่วยทนได้ดี อาการปวดบริเวณที่ฉีดยาและอาการเวียนศีรษะชั่วคราวเป็นอาการไม่พึงประสงค์ที่สำคัญเพียงอย่างเดียว (มิลเลอร์และคณะ, 2015)
การทดลองแบบสุ่มสองทางขนาดเล็กที่ควบคุมด้วยยาหลอก เปรียบเทียบการรักษาภาวะภูมิคุ้มกันบกพร่องระยะสุดท้าย (เอดส์) ด้วยคลอไรต์ (WF10) ในผู้ป่วย 10 ราย และยาหลอกในผู้ป่วย 9 ราย โดยให้คลอไรต์ทางหลอดเลือดดำในปริมาณ 0.5 มล./กก. เป็นเวลา 5 วัน ทุก 3 สัปดาห์ รวมทั้งหมด 4 รอบ ตลอดระยะเวลา 3 เดือน ในผู้ป่วย 10 ราย ไม่พบเหตุการณ์ไม่พึงประสงค์ร้ายแรงใดๆ (Raffanti et al., 1998)
กลไกการออกฤทธิ์ของคลอรีนไดออกไซด์และคลอไรต์ในการรักษาโรค DFUS
คลอรีนไดออกไซด์/คลอไรต์มีฤทธิ์หลายประการที่อาจช่วยส่งเสริมการสมานแผลเบาหวานได้ ผลดีเหล่านี้ได้แก่ การควบคุมระดับน้ำตาลในเลือดที่ดีขึ้น (Maraprygsavan et al., 2016; Yingsakmongkol et al., 2021), การลดการผลิตไอออนซูเปอร์ออกไซด์ในขณะที่เพิ่มการผลิตไฮโดรเจนเปอร์ออกไซด์ (Tissot et al., 1990), การเพิ่มความดันออกซิเจนในเนื้อเยื่อ (Tissot et al., 1990), การลดการอักเสบ (Giese et al., 2004; Schönberg et al., 2016; Tissot et al., 1990; Yingsakmongkol, 2013), ผลต้านจุลชีพ (Alvarez and O’Brien, 1982; Benarde et al., 1965; Sanekata et al., 2010; Zu et al., 2019) และการสมานแผลที่ดีขึ้น (อัล-บายาตี และอับดุลลา, 2012; Hinz et al., 1986; เคนยอน และคณะ 1986; วิลกินส์ 2014; ยิ่งศักดิ์มงคล และคณะ 2011)
ปรับปรุงการควบคุมระดับน้ำตาลในเลือด
มีการแสดงให้เห็นว่าคลอไรต์ช่วยลดระดับฮีโมโกลบิน A1c ในผู้ป่วยเบาหวานที่มีแผลเบาหวานรุนแรง การศึกษาแบบย้อนหลังในผู้ป่วย 12 รายที่เป็นเบาหวานมาเฉลี่ย 16 ปี ได้ตรวจสอบผลของคลอไรต์ (WF10) ในการรักษาแผลเบาหวาน ผู้ป่วยเหล่านี้มีแผลรุนแรงร่วมกับนิ้วเท้าเน่าและกระดูกอักเสบ 8 รายถูกส่งตัวไปผ่าตัดตัดขาใต้เข่า การศึกษาพบว่า 11 ใน 12 รายนี้ มีการหายของแผลอย่างสมบูรณ์ หรือมีการดีขึ้นอย่างมีนัยสำคัญหลังการรักษาด้วย WF10 ใน 8 ใน 12 ราย พบว่าแผลหายสนิท ไม่มีผู้ป่วยรายใดที่ต้องผ่าตัดตัดขาใต้เข่า นอกจากนี้ 11 ใน 12 รายแสดงให้เห็นถึงการลดลงของระดับฮีโมโกลบิน A1c (HbA1c) อย่างมีนัยสำคัญทางสถิติในช่วง 4 ถึง 16 สัปดาห์หลังการรักษา (ตารางที่ 2) พบว่าค่าฮีมาโตคริตลดลงในผู้ป่วยบางราย แต่ภาวะนี้หายไปได้ด้วยการถ่ายเลือด ผู้ป่วย 4 ใน 12 รายได้รับการถ่ายเลือด (Maraprygsavan et al., 2016)
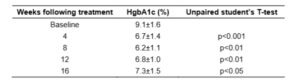
ตารางที่ 2 การลดลงของระดับ Hgb A1c หลังการรักษาด้วยคลอไรต์ (WF10)*
*Maraprygsavan et al. (2016).
การศึกษาวิจัยเชิงคาดการณ์แบบไม่ควบคุมโดยใช้คลอไรต์ (WF10) เป็นการรักษาเสริมสำหรับแผลเบาหวานพบว่าการรักษานี้ช่วยลดค่า HbA1c ได้มากกว่า 2% ลดระดับน้ำตาลในเลือดขณะอดอาหาร (FBG) และเร่งการหายของแผลเบาหวาน โดยแสดงให้เห็นจากการลดลงของคะแนนความรุนแรงของแผลจาก 8.0 เหลือ 1.4 หลังจาก 12 สัปดาห์ (Yingsakmongkol et al., 2021)
ลดระดับซูเปอร์ออกไซด์และเพิ่มไฮโดรเจนเปอร์ออกไซด์
ผลกระทบของคลอไรต์ต่อการผลิต ROS นั้นแตกต่างกันไปตามชนิดของสิ่งมีชีวิต ตัวอย่างเช่น โซเดียมคลอไรต์ (TCDO) ที่ฉีดเข้าไปในหนูทดลองช่วยลดการสร้างซูเปอร์ออกไซด์ได้อย่างมีนัยสำคัญ ในขณะเดียวกันก็เพิ่มระดับไฮโดรเจนเปอร์ออกไซด์ (Tissot et al., 1990) สิ่งนี้อาจเกิดขึ้นเนื่องจากกิจกรรมของ SOD เพิ่มขึ้น (ซึ่งเพิ่มการเปลี่ยนซูเปอร์ออกไซด์เป็นไฮโดรเจนเปอร์ออกไซด์) และการทำงานของไมอีโลเปอร์ออกซิเดสบกพร่อง (ซึ่งเปลี่ยนไฮโดรเจนเปอร์ออกไซด์เป็นกรดไฮโปคลอรัส) (Ali and Mahmood, 2017; Schempp et al., 2001)
การศึกษาล่าสุดจากประเทศอียิปต์ได้สำรวจผลกระทบของเจล ClO2 เฉพาะที่ต่อการรักษาบาดแผลลึกในหนูขาว (Mawas et al., 2022) การศึกษานี้ประกอบด้วย 4 กลุ่ม ได้แก่ กลุ่มควบคุมที่ไม่เป็นเบาหวาน กลุ่มควบคุมที่เป็นเบาหวานแต่ไม่ได้รับการรักษา กลุ่มที่ใช้น้ำมันงา และกลุ่มที่ใช้เจล ClO2 ผลการศึกษาพบว่ากิจกรรมของ SOD สูงกว่าในกลุ่มที่ได้รับการรักษาด้วย ClO2 มากกว่าในกลุ่มที่เป็นเบาหวานแต่ไม่ได้รับการรักษา และการปิดบาดแผลดีกว่าในกลุ่ม ClO2 มากกว่าในทุกกลุ่มอื่น ๆ
เพิ่มระดับความตึงเครียดของออกซิเจนในเนื้อเยื่อ
มีรายงานว่าภาวะขาดออกซิเจนเพิ่มความเสี่ยงต่อการติดเชื้อในเนื้อเยื่อของผู้ป่วยเบาหวานเนื่องจากกลไกการป้องกันของร่างกายบกพร่องและการแสดงออกของยีนเป้าหมายของปัจจัยเหนี่ยวนำภาวะขาดออกซิเจน-1ɑ (HIF-1ɑ) และปัจจัยเหนี่ยวนำภาวะขาดออกซิเจน-1 (HIF-1) ลดลง ส่งผลให้การตอบสนองของเซลล์ต่อภาวะขาดออกซิเจนบกพร่อง (Pozzilli และ Leslie, 1994; Davis et al., 2018) ดังนั้น การเพิ่มความดันออกซิเจนจึงคาดว่าจะช่วยลดความเสี่ยงต่อการติดเชื้อได้
ความพยายามในการเพิ่มปริมาณออกซิเจนในเนื้อเยื่อโดยใช้ออกซิเจนความดันสูงได้ผลลัพธ์ที่หลากหลาย แม้ว่าระดับออกซิเจนในเลือดจะสูงขึ้นอย่างเห็นได้ชัด แต่หลายคนก็ไม่สามารถเพิ่มความดันออกซิเจนในเนื้อเยื่อได้ และบางคนกลับพบว่าความเข้มข้นของออกซิเจนในเนื้อเยื่อลดลงอย่างผิดปกติ ผลกระทบเหล่านี้ถูกตั้งสมมติฐานว่าเกิดขึ้นจากภาวะหลอดเลือดหดตัวอันเนื่องมาจากการผลิต ROS ที่เพิ่มขึ้นและระดับไนตริกออกไซด์ที่ลดลง ในขณะที่ซูเปอร์ออกไซด์และไฮโดรเจนเปอร์ออกไซด์ทำให้หลอดเลือดหดตัว ไนตริกออกไซด์กลับทำให้หลอดเลือดขยายตัว (Efrati et al., 2009)
ผลกระทบของโซเดียมคลอไรต์ต่อการผลิต ROS แสดงให้เห็นผลกระทบที่ขึ้นอยู่กับปริมาณ หนูที่ฉีดด้วยโซเดียมคลอไรต์ (TCDO) 1.5 ไมโครโมล แสดงให้เห็นการลดลงอย่างเห็นได้ชัดของการสร้างซูเปอร์ออกไซด์หลังจาก 4 ชั่วโมง (Tissot et al., 1990) ในขณะที่เม็ดเลือดแดงของมนุษย์ที่บ่มในสารละลายโซเดียมคลอไรต์ 0.1 ถึง 3.0 มิลลิโมลาร์ แสดงให้เห็นการเพิ่มขึ้นของการสร้าง ROS ถึง 3 ถึง 21 เท่า (Ali และ Mahmood, 2017) ดังนั้น ปริมาณคลอไรต์ที่ต่ำกว่าจะคาดว่าจะลดการสร้าง ROS ซึ่งจะลดการหดตัวของหลอดเลือดและปรับปรุงภาวะขาดออกซิเจน ในทางกลับกัน ปริมาณที่สูงกว่าจะเพิ่มระดับ ROS และเพิ่มการหดตัวของหลอดเลือด
ส่งผลให้ภาวะขาดออกซิเจนเพิ่มขึ้น
ลดการอักเสบ
ClO2 และคลอไรต์เปลี่ยนแปลงการตอบสนองของระบบภูมิคุ้มกันผ่านการปรับเปลี่ยนการทำงานของเซลล์ภูมิคุ้มกันหลายชนิด (McGrath et al., 1998) คลอไรต์ออกฤทธิ์ยับยั้งการเพิ่มจำนวนของทีลิมโฟไซต์ในหลอดทดลองโดยขึ้นอยู่กับปริมาณ (Giese et al., 2004) และยับยั้งการฆ่าเซลล์เป้าหมายโดยทีเซลล์ที่เป็นพิษต่อเซลล์ (Wabnitz and Samstag, 2016)
คลอไรต์ยังแสดงคุณสมบัติต้านการอักเสบ เช่น ยับยั้งแมโครฟาจชนิด M1 ที่ก่อให้เกิดการอักเสบ (Schönberg et al., 2016) ยับยั้งการเคลื่อนที่ของเม็ดเลือดขาวชนิดโพลีมอร์โฟนิวเคลียร์ (PMN) (Tissot et al., 1990) เพิ่มกิจกรรมการกลืนกินของแมโครฟาจ (Yingsakmongkol, 2013) และลดการแสดงออกของยีนที่ก่อให้เกิดการอักเสบในโมโนไซต์ (Giese et al., 2004) คลอไรต์ (WF10) ถูกกระตุ้นในปฏิกิริยากับฮีโมโปรตีน โดยเฉพาะอย่างยิ่งไมอีโลเปอร์ออกซิเดส ส่งผลให้เกิดการผลิตทอรีนคลอรามีน (TauCl) ซึ่งเป็นตัวกระตุ้นอะพอพโทซิสที่รุนแรงและยังมีฤทธิ์ต้านการอักเสบด้วย (Giese et al., 2004; Schempp et al., 2001; Yingsakmongkol, 2013) คลอไรต์ยังกระตุ้นความเป็นพิษต่อเซลล์ของเซลล์นักฆ่าตามธรรมชาติ (NK) ด้วย (Kühne et al., 2011)
การศึกษาวิจัยเกี่ยวกับการรักษาโรคเอดส์ด้วยคลอไรต์ (WF10) พบว่าผู้ป่วยแสดงให้เห็นถึงการลดลงอย่างมีนัยสำคัญของเครื่องหมายการกระตุ้นภูมิคุ้มกันของเซลล์ T เช่น CD38, CD28 และ DR รวมถึงการลดลงของ
ลิมโฟไซต์ MO และ B ที่มี DR+ ในกระแสเลือด (McGrath et al., 1998)
โซเดียมคลอไรต์ (NP001) ได้รับการให้ทางหลอดเลือดดำอย่างปลอดภัยแก่ผู้ป่วยโรคกล้ามเนื้ออ่อนแรง (ALS) ในการศึกษาเฟส I และเฟส II ยานี้แสดงให้เห็นว่าสามารถลดตัวบ่งชี้การกระตุ้นภูมิคุ้มกันของโมโนไซต์ในเลือด CD16 และ HLA-DR และชะลอการลุกลามของ ALS ในกลุ่มผู้ป่วยที่มีการอักเสบของระบบประสาทสูง (Miller et al., 2014, 2015) กลไกการออกฤทธิ์ที่แนะนำสำหรับยานี้ในการรักษาโรคความเสื่อมของระบบประสาทคือการเปลี่ยนแมโครฟาจที่ก่อให้เกิดการอักเสบ (M1) ไปเป็นแมโครฟาจที่ไม่ก่อให้เกิดการอักเสบ (M2) (Neuvivo, 2022)
ฤทธิ์ต้านจุลชีพ
มีการแสดงให้เห็นว่า ClO2 มีฤทธิ์ต้านจุลชีพอย่างมีประสิทธิภาพ (Alvarez และ O’Brien, 1982; Benarde et al., 1965; Sanekata et al., 2010; Zhu et al., 2019) คลอไรต์ (TCDO) แสดงฤทธิ์ต้านไวรัสและฆ่าไวรัสต่อไวรัสหลายชนิด รวมถึงไวรัสเริมชนิดที่ 1 (HSV-1), ไวรัสเริมชนิดที่ 2 (HSV-2), ไข้หวัดใหญ่สายพันธุ์ A, โปลิโอสายพันธุ์ที่ 1 (Dargan และ Subek-Sharpe, 1992) และไวรัสภูมิคุ้มกันบกพร่องในมนุษย์ (HIV) (Ennen et al., 1993) คลอไรต์ (TCDO) มีฤทธิ์ต้านแบคทีเรียแบบขึ้นอยู่กับปริมาณและจำเพาะต่อสายพันธุ์ต่อแบคทีเรียแอโรบิกและแบคทีเรียแอนแอโรบิก (Ullmann และ Kühne, 1985)
Gillissen et al. (1986) พบว่าคลอไรต์ (TCDO) ช่วยเพิ่มอัตราการรอดชีวิตในหนูทดลองที่ติดเชื้อ Candida albicans หรือ Peptostreptococcus intermedius ในขณะเดียวกันก็ช่วยเสริมสร้างการตอบสนองทางภูมิคุ้มกันทั้งแบบฮิวโมรัลและเซลลูลาร์ ซึ่งส่วนหนึ่งเกิดขึ้นจากการเพิ่มจำนวนเซลล์ม้ามที่สร้าง IgM และ IgG
การทดลองแบบสุ่มสองทางโดยใช้ยาหลอกควบคุมที่ตรวจสอบคลอไรต์ (WF10) ทางหลอดเลือดดำเป็นวิธีการรักษาแผลเบาหวานในมนุษย์ พบว่าผู้ที่ได้รับการรักษาด้วยคลอไรต์มีแผลรุนแรงน้อยลงเมื่อเทียบกับกลุ่มที่ได้รับยาหลอกหลังจากได้รับการรักษา 9 สัปดาห์ ผลการวิจัยที่มีนัยสำคัญทางสถิติ ได้แก่ การติดเชื้อลดลง (Yingsakmongkol et al., 2011)
ClO2 มีฤทธิ์ต้านแบคทีเรีย ไวรัส และเชื้อราฤทธิ์ต้านจุลชีพเหล่านี้เกิดจากการทำงานของ ClO2 ในฐานะสารออกซิไดซ์ สารออกซิไดซ์คือสารที่รับหรือส่งอิเล็กตรอนจากสารรีดิวซ์ (นั่นคือผู้ให้อิเล็กตรอน) ClO2 ออกซิไดซ์ DNA, RNA และโปรตีนส่งผลให้การสังเคราะห์โปรตีนหยุดชะงัก เยื่อหุ้มเซลล์ถูกทำลาย และเซลล์ตาย (Peredo-Lovillo et al., 2023)
ช่วยให้แผลหายเร็วขึ้น
คลอรีนไดออกไซด์และคลอไรต์ช่วยปรับปรุงการสมานแผลและส่งเสริมการสร้างเนื้อเยื่อแกรนูเลชันในแผลประเภทต่างๆ (Hinz et al., 1986; Kenyon et al., 1986) Wilkins (2014) อธิบายกรณีศึกษา 3 กรณีที่ใช้ ClO2 (Ciderm) เป็นส่วนหนึ่งของโปรแกรมการจัดการดูแลแผลหลังผ่าตัด พวกเขาพบว่า ClO2 สามารถรักษาและป้องกันการติดเชื้อได้อย่างมีประสิทธิภาพ ในขณะเดียวกันก็ช่วยรักษาเนื้อเยื่อที่ยังมีชีวิตอยู่
การศึกษาที่ดำเนินการในมาเลเซียได้สำรวจกิจกรรมการรักษาบาดแผลของเจล ClO2 ในหนูเบาหวานที่เกิดจากการเหนี่ยวนำด้วยสเตรปโตโซซิน (Al-Bayaty และ Abdulla, 2012) ผู้เขียนได้ทำการเหนี่ยวนำให้เกิดบาดแผลจากการตัดเนื้อเยื่อในหนู Sprague Dawley เพศผู้โตเต็มวัย จากนั้นจึงทาเจลคลอรีนไดออกไซด์ลงบนแผลวันละสองครั้ง กลุ่มที่สองได้รับการรักษาด้วยเจลกรดไฮยาลูรอนิก ในขณะที่กลุ่มที่สามได้รับการรักษาด้วยเจล Intrasite กลุ่มควบคุมได้รับการรักษาด้วยน้ำกลั่นปราศจากเชื้อ เก็บเนื้อเยื่อบาดแผลในวันที่ 10 เพื่อวัดกิจกรรมของเอนไซม์ต้านอนุมูลอิสระกลูตาไธโอนเปอร์ออกซิเดส (GPx) และซูเปอร์ออกไซด์ดิสมิวเทส (SOD) หลังจาก 10 วันของการรักษา ขนาดของบาดแผลมีขนาดเล็กกว่าอย่างมีนัยสำคัญในกลุ่มที่ได้รับการรักษาด้วย ClO2 เมื่อเทียบกับกลุ่มควบคุม
นอกจากนี้ เนื้อเยื่อเม็ดจากกลุ่มที่ได้รับการรักษาประกอบด้วยเซลล์อักเสบน้อยลง มีคอลลาเจนมากขึ้น และมีเส้นเลือดฝอยที่เพิ่มจำนวนขึ้นมากกว่าเนื้อเยื่อเม็ดจากกลุ่มควบคุม ยิ่งไปกว่านั้น ระดับกิจกรรมของ GPx และ SOD ยังเพิ่มขึ้นอย่างมีนัยสำคัญในกลุ่ม ClO2 เมื่อเทียบกับกลุ่มควบคุม การทดลองแบบสุ่มควบคุมด้วยยาหลอกแบบปกปิดสองทางที่สำรวจการใช้คลอไรต์ทางหลอดเลือดดำ (WF10) เป็นวิธีการรักษาแผลเบาหวาน พบว่าผู้ป่วยในกลุ่มที่ได้รับการรักษามีความรุนแรงของแผลลดลงเมื่อเทียบกับกลุ่มยาหลอกหลังจากได้รับการรักษา 9 สัปดาห์ ผลการวิจัยที่มีนัยสำคัญทางสถิติ ได้แก่ การติดเชื้อ การอักเสบ และเนื้อเยื่อตายลดลง พร้อมกับการเพิ่มขึ้นของเนื้อเยื่อเม็ด (Yingsakmongkol et al., 2011)
ความท้าทายที่อาจเกิดขึ้นจากการใช้ CLO2 ในการรักษา DFUS
แม้ว่า ClO2 จะมีศักยภาพด้านความปลอดภัยและประสิทธิภาพในการรักษาแผลเบาหวาน แต่ก็ยังมีอุปสรรคที่อาจจำกัดการใช้ ClO2 ในการรักษาแผลเบาหวาน อุปสรรคประการหนึ่งคือต้นทุนของยาชนิดนี้ ปัญหาไม่ได้อยู่ที่ว่า ClO2 มีราคาแพงในการผลิตหรือจัดจำหน่าย ในความเป็นจริงแล้ว ตรงกันข้าม ClO2 มีราคาไม่แพงและไม่สามารถจดสิทธิบัตรได้ ดังนั้นจึงไม่น่าเป็นไปได้ที่บริษัทเภสัชกรรมใด ๆ จะทำการวิจัยเกี่ยวกับยาชนิดนี้ต่อไป เนื่องจากความยากลำบากในการคืนทุนจากการลงทุนจำนวนมากที่จำเป็นในการนำยาชนิดนี้ออกสู่ตลาด

ตารางที่ 3 กลไกการออกฤทธิ์ที่เสนอสำหรับ ClO2/ClO2- ในการรักษาแผลเบาหวาน
ที่มา: Maraprygsavan และคณะ (2016); ยิ่งศักดิ์มงคล และคณะ, 2021; อาลีและมาห์มูด (2017); ทิสโซต์ และคณะ (1990); Giese และคณะ (2004); เชินเบิร์ก และคณะ (2016); อัลวาเรซและโอไบรอัน (1982); เบอร์นาร์เด และคณะ (1965); ซาเนกาตะ และคณะ (2010); ซู และคณะ (2019); อัล-บายาตี และอับดุลลา (2012); ฮินซ์เอตอัล., 1986; เคนยอน และคณะ (1986); วิลกินส์ (2014)
อุปสรรคประการที่สองคือคำวิจารณ์และคำกล่าวที่สร้างความหวาดกลัวของสำนักงานคณะกรรมการอาหารและยาแห่งสหรัฐอเมริกา (FDA) เกี่ยวกับ “ผลิตภัณฑ์โซเดียมคลอไรต์” ในช่วงการระบาดของ COVID-19 FDA ได้เตือนว่าผลิตภัณฑ์โซเดียมคลอไรต์นั้น “อันตราย” และ “อาจทำให้คุณป่วยได้” เว็บไซต์ของ FDA เตือนว่า “โซเดียมคลอไรต์และคลอรีนไดออกไซด์เป็นส่วนประกอบสำคัญในน้ำยาฆ่าเชื้อ และยังมีประโยชน์ในอุตสาหกรรมอื่นๆ อีกด้วย ไม่ควรให้คนกลืนกิน” FDA เปรียบเทียบการดื่มผลิตภัณฑ์โซเดียมคลอไรต์กับการดื่มน้ำยาฟอกขาว (สำนักงานคณะกรรมการอาหารและยาแห่งสหรัฐอเมริกา, 2019)
แม้ว่าจะเป็นความจริงที่ว่าการรับประทานโซเดียมคลอไรต์หรือคลอรีนไดออกไซด์ในปริมาณสูงอาจก่อให้เกิดผลข้างเคียง แต่ก็เป็นความจริงสำหรับยาอื่นๆ ทุกชนิดที่มีอยู่ในปัจจุบันเช่นกัน ดังที่แพทย์และนักเคมีพาราเซลซัสกล่าวไว้เมื่อกว่า 500 ปีแล้วว่า “ปริมาณเท่านั้นที่จะเป็นตัวกำหนดว่าสิ่งนั้นเป็นสารพิษหรือไม่” (Borzelleca, 2000, หน้า 3) ยิ่งไปกว่านั้น คำเตือนขององค์การอาหารและยา (FDA) ยังเพิกเฉยต่อข้อเท็จจริงที่ว่าผู้คนหลายล้านคนทั่วโลกดื่มคลอรีนไดออกไซด์ในปริมาณต่ำในน้ำประปาของเทศบาลทุกวัน และคลอไรต์ก็ได้รับการอนุมัติให้เป็นยาแล้วในเยอรมนีและประเทศไทย ดังนั้น การวิจัยเกี่ยวกับการประยุกต์ใช้คลอรีนไดออกไซด์ในการรักษาจึงต้องเผชิญกับทัศนคติเชิงลบเกี่ยวกับยานี้และการต่อต้านการใช้ยา
การอภิปราย
วัตถุประสงค์ของการทบทวนวรรณกรรมนี้คือเพื่อประเมินความปลอดภัยและประสิทธิภาพของคลอรีนไดออกไซด์ในการรักษาแผลเบาหวาน และเพื่ออธิบายกลไกการออกฤทธิ์ที่เป็นไปได้ซึ่งสารเหล่านี้อาจใช้ในการรักษาแผลเบาหวาน หลังจากทบทวนวรรณกรรมแล้ว พบว่าเมื่อใช้ในปริมาณต่ำ คลอรีนไดออกไซด์และคลอไรต์มีแนวโน้มที่ดีในการรักษาแผลเบาหวานด้วยสารที่มีความปลอดภัยและมีประสิทธิภาพ (ตารางที่ 3)
เราตั้งสมมติฐานว่าคลอรีนไดออกไซด์และคลอไรต์สามารถส่งเสริมการสมานแผลเบาหวานผ่านกลไกหลายประการ รวมถึง:
(1) ปรับปรุงการควบคุมระดับน้ำตาลกลูโคสและลดภาวะน้ำตาลในเลือดสูง จึงช่วยปรับปรุงการทำงานของหลอดเลือด เส้นประสาท และระบบภูมิคุ้มกัน (Maraprygsavan et al., 2016; Yingsakmongkol et al., 2021)
(2) ปรับปรุงภาวะหลอดเลือดผิดปกติโดยการเพิ่มการสร้างหลอดเลือดใหม่และความตึงเครียดของออกซิเจนในเนื้อเยื่อโดยการเพิ่มการเปลี่ยนซูเปอร์ออกไซด์เป็นไฮโดรเจนเปอร์ออกไซด์ผ่านการเพิ่มประสิทธิภาพของ
ซูเปอร์ออกไซด์ดิสมิวเทสพร้อมกับการเพิ่มระดับของไซโตไคน์ VEGF และ TGF-β-1
(3) ชะลอการลุกลามของโรคเส้นประสาทโดยการปรับปรุงการไหลเวียนของเลือดไปยังเซลล์ประสาท
(4) ลดการอักเสบโดยการยับยั้งการอพยพของ PMN (Schönberg et al., 2016) เพิ่มกิจกรรมการกลืนกินของแมโครฟาจ (Yingsakmongkol, 2013) ลดการแสดงออกของยีนที่ก่อให้เกิดการอักเสบในโมโนไซต์ (Giese et al., 2004) เพิ่มการผลิตทอรีนคลอรามีน (Giese et al., 2004; Schempp et al., 2001; Yingsakmongkol, 2013) เพิ่มการเปลี่ยนแมโครฟาจที่ก่อให้เกิดการอักเสบ (M1) ไปเป็นแมโครฟาจที่ไม่ก่อให้เกิดการอักเสบ (M2) (Neuvivo, 2022)
(5) ลดการติดเชื้อด้วยฤทธิ์ต้านจุลชีพ (Alvarez and โอไบรอัน 1982; เบนาร์เด และคณะ 1965; ดาร์แกน & ซูเบค-ชาร์ป 1992; เอนเนน และคณะ 1993; กิลลิสเซ่น และคณะ 1986; ซาเนกาตะ และคณะ 2010; ยิ่งศักดิ์มงคล และคณะ 2554; โจว และคณะ 2019)
(6) ปรับปรุงการสมานแผลให้ดีขึ้นโดยการเพิ่มการสร้างเนื้อเยื่อแกรนูเลชันควบคู่ไปกับการสร้างเนื้อเยื่อที่แข็งแรงขึ้นใหม่ (Al-Bayaty และ Abdulla, 2012; Hinz et al., 1986; Kenyon et al., 1986; Yingsakmongkol et al., 2011)
บทสรุป
แผลเบาหวานมีความเกี่ยวข้องกับความเจ็บป่วยและการเสียชีวิตอย่างมีนัยสำคัญ และเป็นปัญหาสุขภาพระดับโลกที่ร้ายแรง คลอรีนไดออกไซด์และคลอไรต์มีแนวโน้มที่ดีในการรักษาแผลเบาหวานอย่างปลอดภัยและมีประสิทธิภาพ จำเป็นต้องมีการศึกษาแบบสุ่มและควบคุมด้วยยาหลอกเพื่อสำรวจความปลอดภัย ประสิทธิภาพ และช่วงขนาดยาที่เหมาะสมของยาเหล่านี้ นอกจากนี้ยังจำเป็นต้องมีการศึกษาที่ตรวจสอบวิธีการให้ยาที่แตกต่างกัน (เช่น การรับประทาน เทียบกับ การทา เทียบกับ การฉีดเข้าเส้นเลือด เทียบกับ การให้ยาหลายวิธีพร้อมกัน) ผลการทบทวนนี้สนับสนุนการวิจัยดังกล่าวอย่างยิ่ง และเราหวังว่านักวิจัยทั่วโลกจะยังคงสำรวจประโยชน์ที่เป็นไปได้ของคลอรีนไดออกไซด์และคลอไรต์ต่อไป
ความขัดแย้งทางผลประโยชน์
ผู้เขียนไม่มีผลประโยชน์ทับซ้อนใด ๆ ที่ต้องแจ้งให้ทราบ
เอกสารอ้างอิง
Abdel-Rahman MS, Couri D, Bull RJ (1979). จลนศาสตร์ของ Cl02 และผลกระทบของ Cl02, Cl02- และ Cl03- ในน้ำดื่มต่อกลูตาไธโอนในเลือด และการแตกตัวของเม็ดเลือดแดงในหนูและไก่ วารสารสิ่งแวดล้อม
พยาธิวิทยาและพิษวิทยา 3(1-2):431-49.
Abdel-Rahman MS, Couri D, Bull RJ (1984). จลนศาสตร์ของคลอไรต์และคลอเรตในหนู วารสารวิทยาลัยพิษวิทยาแห่งอเมริกา 3(4):261-267.
Al-Bayaty F, Abdulla MA (2012). การเปรียบเทียบอัตราการหายของแผลหลังการรักษาด้วยเจลอะฟทาเมดและคลอรีนไดออกไซด์ในหนูเบาหวานที่เกิดจากการเหนี่ยวนำด้วยสเตรปโตโซซิน การแพทย์เสริมและทางเลือกตามหลักฐานเชิงประจักษ์ https://doi.org/10.1155/2012/468764
Ali SN, Mahmood R (2017). โซเดียมคลอไรต์เพิ่มการผลิตอนุมูลอิสระออกซิเจนที่ทำลายระบบต้านอนุมูลอิสระและทำให้เกิดการเปลี่ยนแปลงทางสัณฐานวิทยาในเม็ดเลือดแดงของมนุษย์ Environmental Toxicology 32(4):1343-1353. https://doi.org/10.1002/tox.22328
Alvarez ME, O’Brien RT (1982). กลไกการยับยั้งไวรัสโปลิโอโดยคลอรีนไดออกไซด์และไอโอดีน Applied and Environmental Microbiology 44(5):1064-1071. https://doi.org/10.1128/aem.
สภาเคมีอเมริกัน (2023). ChemicalSafetyFacts.org. คลอรีน Calliperis et al. 11 ไดออกไซด์. เข้าถึงได้จาก: https://www.chemicalsafetyfacts.org/chemicals/chloine-dioxide/. สืบค้นเมื่อ (6):23
Aparicio-Alonso M, Domínguez-Sánchez C, Banuet-Martínez M (2021). คลอรีนไดออกไซด์เป็นทางเลือกในการรักษา COVID19. วารสารโรคติดเชื้อและการบำบัด 4(8). doi:10.47191/ijmra/v4-i8-02.
Apelqvist J, Larsson J, Agardh C-D (1993). การพยากรณ์โรคในระยะยาวสำหรับผู้ป่วยเบาหวานที่มีแผลที่เท้า. วารสารอายุรศาสตร์ภายใน 233(6):485-491. https://doi.org/10.1111/j.1365- 2796.1993.tb01003.x
Armstrong DG, Wrobel J, Robbins JM (2007). บทบรรณาธิการรับเชิญ: แผลและการตัดอวัยวะที่เกี่ยวข้องกับโรคเบาหวานนั้นร้ายแรงกว่ามะเร็งหรือไม่ วารสารบาดแผลนานาชาติ 4(4):286-287.
Aronson D (2008) ภาวะน้ำตาลในเลือดสูงและพยาธิวิทยาของภาวะแทรกซ้อนจากโรคเบาหวาน วารสารโรคหัวใจและหลอดเลือดที่เกี่ยวข้องกับโรคเบาหวาน: ด้านคลินิก เมตาบอลิซึม และการอักเสบ 45:1-6. https://doi.org/10.1159/000115118
Aronson D, Rayfield EJ (2002). ภาวะน้ำตาลในเลือดสูงส่งเสริมภาวะหลอดเลือดแดงแข็งได้อย่างไร: กลไกระดับโมเลกุล วารสารโรคหัวใจและหลอดเลือดที่เกี่ยวข้องกับโรคเบาหวาน 1(1)1-10. https://doi.org/10.1186/1475-2840-1-1
Benarde MA, Israel BM, Olivieri VP, Granstrom ML (1965). ประสิทธิภาพของคลอรีนไดออกไซด์ในฐานะสารฆ่าเชื้อแบคทีเรีย Applied Microbiology 13(5):776-80. https://doi.org/10.1128/am.13.5.776-780.1965
Borzelleca JF (2000). Paracelsus: ผู้ประกาศข่าวแห่งพิษวิทยาสมัยใหม่ Toxicological Sciences 53(1):2-4. https://doi.org/10.1093/toxsci/
Brownlee M (2001). ชีวเคมีและชีววิทยาของเซลล์ระดับโมเลกุลของภาวะแทรกซ้อนจากโรคเบาหวาน Nature 414(6865):813-820. https://doi.org/10.1038/414813a
Butler SO, Btaiche IF, Alaniz C (2005). ความสัมพันธ์ระหว่างภาวะน้ำตาลในเลือดสูงและการติดเชื้อในผู้ป่วยวิกฤต เภสัชบำบัด: วารสารเภสัชวิทยาและยาบำบัดของมนุษย์ 25(7):963- 976. https://doi.org/10.1592/phco.2005.25.7.963
Cathcart MK (2004). การควบคุมการผลิตซูเปอร์ออกไซด์แอนไอออนโดย NADPH oxidase ในโมโนไซต์/มาโครฟาจ: การมีส่วนร่วมต่อหลอดเลือดแดงแข็งตัว Arteriosclerosis, Thrombosis, and Vascular Biology 24(1):23-28. https://doi.org/10.1161/01.ATV.0000097769.47306.12
Chin D, Boyle GM, Parsons PG, Coman WB (2004).transforming growth factor-beta (TGF-β) คืออะไร? British Journal of Plastic Surgery 57(3):215-221. https://doi.org/10.1016/j.bjps.2003.12.012
Clarke NA, Berman D (1983). การฆ่าเชื้อน้ำดื่ม น้ำในสระว่ายน้ำ และน้ำเสียที่ผ่านการบำบัดแล้ว การฆ่าเชื้อ การทำให้ปลอดเชื้อ และการถนอมอาหาร Seymour S. Block บรรณาธิการ ฟิลาเดลเฟีย: Lea and Febiger
Couri D, Abdel-Rahman MS, Bull, RJ (1982). ผลกระทบทางพิษวิทยาของคลอรีนไดออกไซด์ คลอไรต์ และคลอเรต Environmental Health Perspectives 46:13-17. https://doi.org/10.1289/ehp.824613
Dargan DJ, Subak-Sharpe JH (1992). กิจกรรมต้านไวรัสของเตตระคลอโรเดคาออกไซด์ต่อไวรัสเริมชนิดที่ 1 และผลฆ่าเชื้อไวรัสของยา Antiviral Chemistry and Chemotherapy 3(2):95-105. https://doi.org/10.1177/095632029200300204
Davis FM, Kimball A, Boniakowski A, Gallagher K. (2018). การสมานแผลที่ผิดปกติในแผลเบาหวานที่เท้า: ทางแยกใหม่ Current
Diabetes Reports 18(1):1-8. https://doi.org/10.1007/s11892-018-0970-z
Davy H (1832). “เกี่ยวกับการผสมผสานระหว่างก๊าซออกซิมิวเรียติกและก๊าซออกซิเจน” บทคัดย่อของบทความที่ตีพิมพ์ในวารสาร Philosophical Transactions ของราชสมาคมแห่งลอนดอน ฉบับที่ 1 ลอนดอน: ราชสมาคม https://doi.org/10.1098/rspl.1800.0221
Detmar M, Brown LF, Berse B, Jackman RW, Elicker BM, Dvorak HF, Claffey KP (1997). ภาวะขาดออกซิเจนควบคุมการแสดงออกของปัจจัยการซึมผ่านของหลอดเลือด/ปัจจัยการเจริญเติบโตของเยื่อบุหลอดเลือด (VPF/VEGF) และตัวรับของมันในผิวหนังมนุษย์ วารสาร Journal of Investigative Dermatology 108(3):263-268. https://doi.org/10.1111/1523-1747.ep12286453
Drechsler PA, Wildman EE, Pankey JW (1990). การประเมินน้ำยาจุ่มหัวนมวัวสูตรทดลองที่มีส่วนผสมของกรดคลอรัสและคลอรีนไดออกไซด์ ภายใต้สภาวะการสัมผัสเชื้อแบบจำลองและแบบธรรมชาติ. วารสาร Journal of Dairy Science 73(8):2121-2128. https://doi.org/10.3168/jds.S0022-0302(90)78892-3
Efrati S, Gall N, Bergan J, Fishlev G, Bass A, Berman S, Abu-Hamad R, Feigenzon M, Weissgarten J (2009). ออกซิเจนความดันสูง, ความเครียดจากออกซิเดชั่น, ความพร้อมใช้งานของ NO และการให้ออกซิเจนในแผลในผู้ป่วยเบาหวาน Undersea and Hyperbaric Medicine 36(1):1-12.
Ennen J, Werner K, Kühne FW, Kurth R (1993). การทำให้เชื้อ HIV ไม่ติดเชื้อโดยผลิตภัณฑ์ปฏิกิริยาคลอไรต์-ออกซิเจน tetrachlorodecaoxygen. AIDS (London, England) 7(9):1205-1212.
Environmental Protection Agency (2000). การทบทวนทางพิษวิทยาของคลอรีนไดออกไซด์และคลอไรต์ เข้าถึงได้ที่: https://cfpub.epa.gov/ncea/iris2/chemicalLanding.cfm?substance_nmbr=496 สืบค้นเมื่อ 23 มิถุนายน 2023
Fard AS, Esmaelzadeh M, Larijani B (2007). การประเมินและการรักษาแผลที่เท้าจากโรคเบาหวาน วารสารนานาชาติว่าด้วยการปฏิบัติทางคลินิก 61(11):1931-1938.
Feldman EL (2003). ความเครียดจากออกซิเดชันและโรคเส้นประสาทจากโรคเบาหวาน: ความเข้าใจใหม่เกี่ยวกับปัญหาเก่า วารสารการวิจัยทางคลินิก 111(4):431-433.https://doi.org/10.1172/JCI17862
Flesch R, Plenge J, Rühl, E. (2006). การกระตุ้นระดับแกนกลางและการแตกตัวของคลอรีนไดออกไซด์ วารสารนานาชาติว่าด้วยมวลสารสเปกโทรเมตรี 249:68-76. https://doi.org/10.1016/j.ijms.2005.12.046
Frascella J, Gilbert RD, Fernandez P, Hendler J. (2000). ประสิทธิภาพของน้ำยาบ้วนปากที่มีคลอรีนไดออกไซด์ในการลดกลิ่นปาก Compendium ของการศึกษาต่อเนื่องทางทันตกรรม (Jamesburg, NJ: 1995) 21(3):241-244.
Frontier Pharmaceutical, Inc (2022) ผู้จำหน่ายคลอรีนไดออกไซด์ออนไลน์ เข้าถึงได้ที่: https://frontierpharm.com/ เข้าถึงเมื่อวันที่ 8 สิงหาคม 2022
Fujiwara T, Kubo T, Kanazawa S, Shingaki K, Taniguchi M, Matsuzaki S, Gurtner GC, Tohyama M, Hosokawa K (2013). การสัมผัสโดยตรงของไฟโบรบลาสต์กับกระบวนการของเซลล์ประสาทส่งเสริมการแยกตัวเป็นไมโอไฟโบรบลาสต์และกระตุ้นการหดตัวของเมทริกซ์คอลลาเจนในหลอดทดลอง Wound Repair Regen 21:588-594. doi: 10.1111/wrr.12059.
Fukayama MY, Tan H, Wheeler WB, Wei CI (1986). Reactions of aqueous chlorine and chlorine dioxide with model food compounds. Environmental Health Perspectives (69):267-274.https://doi.org/10.1289/ehp.8669267
Gall RJ (1978). คลอรีนไดออกไซด์ ภาพรวมของการเตรียม คุณสมบัติ และการใช้งาน ผลิตภัณฑ์ออกซิเดชันของโอโซนและคลอรีนไดออกไซด์ของวัสดุอินทรีย์ (RG Rice และ JA Cotruvo บรรณาธิการ) สถาบันโอโซนระหว่างประเทศ คลีฟแลนด์ โอไฮโอ
Gettens RJ (1952). การฟอกสีภาพที่เปื้อนและเปลี่ยนสีบนกระดาษด้วยโซเดียมคลอไรต์และคลอรีนไดออกไซด์ Museum International 5(2):116-130. https://doi.org/10.1111/j.1468-0033.1952.tb00180.x
Giese T, McGrath MS, Stumm S, Schempp H, Elstner E, Meuer SC (2004). ผลกระทบที่แตกต่างกันต่อการตอบสนองภูมิคุ้มกันโดยกำเนิดเทียบกับภูมิคุ้มกันแบบปรับตัวโดย WF10 Cellular Immunology 229(2):149-158. https://doi.org/10.1016/j.cellimm.2004.08.001
Gillissen G, Kühne FW, Breuer-Werle M, Melzer B, Ostendorp H (1986). ความต้านทานที่เพิ่มขึ้นต่อการติดเชื้อทดลองในระบบสองชนิด โดยสารประกอบแอนไอออนเตตระคลอโรเดคาออกซิเจน ผลกระทบที่เป็นไปได้ของภูมิคุ้มกันของเซลล์และภูมิคุ้มกันของเหลว Arzneimittel-forschung 36(12):1778-1782.
Goldin A, Beckman JA, Schmidt AM, Creager MA (2006). ผลิตภัณฑ์ปลายทางไกลเคชั่นขั้นสูง: กระตุ้นการพัฒนาของการบาดเจ็บของหลอดเลือดในผู้ป่วยเบาหวาน Circulation 114(6):597-605. https://doi.org/10.1161/CIRCULATIONAHA.106.621854
Gómez-López VM, Rajkovic A, Ragaert P, Smigic N, Devlieghere F (2009). คลอรีนไดออกไซด์สำหรับการถนอมอาหารแปรรูปขั้นต่ำ: บทวิจารณ์ แนวโน้มวิทยาศาสตร์และเทคโนโลยีอาหาร 20(1):17-26. https://doi.org/10.1016/j.tifs.2008.09.005
Gordon G, Rosenblatt AA (2005). คลอรีนไดออกไซด์: สถานะปัจจุบันของศิลปะ โอโซน: วิทยาศาสตร์และวิศวกรรม 27(3):203-207. https://doi.org/10.1080/01919510590945741
Hinz J, Hantzinger H, Helling J, Shirren G, ขาย G, Stahl KW, Kühne เอฟดับบลิว. (1984) การกระตุ้น Wundheilung durch TCDO: Ergebnisse โดยการสุ่มตัวอย่าง Doppelblindstudie ฟอร์ชริตเทอ เดอร์ เมดิซิน 18:523-528.
Hinz J, Kuhne F.-W, สตาห์ล, K-W. (1984) เตตระคลอโรเดแคออกไซด์ในท้องถิ่น การบำบัดเพื่อเพิ่มปริมาณออกซิเจนให้กับบาดแผลที่ไม่สมานตัว ที่มีดหมอ 324(8403):630. https://doi.org/10.1016/S0140-
6736(84)90610-X
Hinz J, Hautzinger H, Stahl K-W (1986) เหตุผลและผลลัพธ์จากการทดลองแบบสุ่มและปกปิดสองทางของสารประกอบเตตระคลอโรเดคาออกซิเจนแอนไอออนในการรักษาบาดแผล The Lancet 327(8485):825-828. https://doi.org/10.1016/S0140-6736(86)90939-6
Huang SS, Zheng RL (2006). การควบคุมแบบสองเฟสของการสร้างหลอดเลือดใหม่โดยสารออกซิเจนที่ออกฤทธิ์ Die Pharmazie-An International Journal of Pharmaceutical Sciences 61(3):223-229.
Jonnalagadda SB, Nadupalli S (2014). คลอรีนไดออกไซด์สำหรับการฟอกขาว การใช้งานในอุตสาหกรรมและการบำบัดน้ำ Indian Chemical Engineer56(2):123-136. https://doi.org/10.1080/00194506.2014.881032
Jupiter DC, Thorud JC, Buckley CJ, Shibuya N (2016). ผลกระทบของแผลที่เท้าและการตัดอวัยวะต่ออัตราการเสียชีวิตในผู้ป่วยเบาหวาน I: จากแผลสู่ความตาย การทบทวนอย่างเป็นระบบ International WoundJournal 13(5):892-903. https://doi.org/10.1111/iwj.12404
Kashiwagi A, Asahina T, Nishio Y, Ikebuchi M, Tanaka Y, Kikkawa R, Shigeta Y (1996). ไกลเคชั่น ความเครียดออกซิเดชั่น และกิจกรรมการกำจัดอนุมูลอิสระ: การเผาผลาญกลูโคสและการทำงานผิดปกติของตัวกำจัดอนุมูลอิสระในเซลล์เยื่อบุผนังหลอดเลือด Diabetes 45(Supplement 3):S84-S86. https://doi.org/10.2337/diab.45.3.S84
Kenyon AJ, Hamilton SG, Douglas DM (1986). การซ่อมแซมบาดแผลแบบควบคุมในหนูตะเภา โดยใช้ยาต้านจุลชีพที่เปลี่ยนแปลงการสร้างเนื้อเยื่อเกี่ยวพัน AmericanJournal of Veterinary Research 47(1):96-101.
Kim Y-W, Byzova TV (2014). ความเครียดออกซิเดชั่นในการสร้างหลอดเลือดและโรคหลอดเลือด Blood, the Journal of the American Society of Hematology 123(5):625-631. https://doi.org/10.1182/blood-2013-09-512749
King GL, Loeken MR (2004). ความเครียดออกซิเดชันที่เกิดจากภาวะน้ำตาลในเลือดสูงในภาวะแทรกซ้อนของโรคเบาหวาน Histochemistry and Cell Biology 122(4):333-338. https://doi.org/10.1007/s00418-004-0678-9
Kruse I, Edelman S (2006). การประเมินและการรักษาแผลที่เท้าจากโรคเบาหวาน Clinical Diabetes 24(2):91-93.
Kühne L, Konstandin M, Samstag Y, Meuer S, Giese T, Watzl C (2011). WF10 กระตุ้นความเป็นพิษของเซลล์ NK โดยการเพิ่มการยึดเกาะกับเซลล์มะเร็งผ่าน LFA-1 วารสารชีวการแพทย์และเทคโนโลยีชีวภาพ
(2011). https://doi.org/10.1155/2011/436587
Lackett JJ, Burkhardt CC, Hitchcock JD (1972). Oxodene: อายุยืนยาวของผึ้ง. Journal of Economic Entomology 65(1):19-20. https://doi.org/10.1093/jee/65.1.19
Li B, Li W, Li X, Zhou H (2017). การอักเสบ: เป้าหมาย/ทิศทางการรักษาแบบใหม่ในโรคหลอดเลือดแดงแข็ง. Current Pharmaceutical Design 23(8):1216-1227.
Lim JZ, Ng NS, Thomas C (2017). การป้องกันและการรักษาแผลที่เท้าจากโรคเบาหวาน. Journal of the Royal Society of Medicine 110(3):104-109. https://doi.org/10.1177/0141076816688346
Lipsky BA, Berendt AR, Cornia PB, Pile JC, Peters EJ, Armstrong DG, Deery HG, Embil JM, Joseph WS, Karchmer AW, Pinzur MS (2012). แนวทางปฏิบัติทางคลินิกของสมาคมโรคติดเชื้อแห่งอเมริกา ปี 2012 สำหรับการวินิจฉัยและการรักษาการติดเชื้อที่เท้าของผู้ป่วยเบาหวานโรคติดเชื้อทางคลินิก 54(12):e132-e173. https://doi.org/10.1177/0141076816688346
Lowe JJ, Gibbs SG, Iwen PC, Smith PW, Hewlett AL (2013). ผลกระทบของการฆ่าเชื้อด้วยก๊าซคลอรีนไดออกไซด์ต่อความมีชีวิตของจุลินทรีย์ที่ก่อให้เกิดโรคในโรงพยาบาลในห้องผู้ป่วยในโรงพยาบาล วารสารวิจัยสิ่งแวดล้อมระหว่างประเทศและสาธารณสุข 10(6):2596-2605. https://doi.org/10.3390/ijerph10062596
Lubbers JR, Chauhan S, Bianchine JR (1981). การประเมินทางคลินิกแบบควบคุมของคลอรีนไดออกไซด์ คลอไรต์ และคลอเรตในมนุษย์พิษวิทยาพื้นฐานและประยุกต์ 1(4):334-338. https://doi.org/10.1289/ehp.824657
Lubbers, JR, Chauan S, Bianchine JR (1982). การประเมินทางคลินิกแบบควบคุมของคลอรีนไดออกไซด์ คลอไรต์ และคลอเรตในมนุษย์มุมมองด้านสุขภาพสิ่งแวดล้อม 46:57-62. https://doi.org/10.1289/ehp.824657
Lubbers JR, Bianchine JR (1984a). ผลกระทบของการให้คลอรีนไดออกไซด์ คลอเรต และคลอไรต์ในปริมาณที่เพิ่มขึ้นอย่างเฉียบพลันต่ออาสาสมัครชายวัยผู้ใหญ่ที่มีสุขภาพดี วารสารพยาธิวิทยา พิษวิทยา และมะเร็งวิทยา 5(4-5):215-228.
Lubbers JR, Chauhan SU, Miller JK, Bianchine JR (1984b). ผลกระทบของการให้คลอรีนไดออกไซด์ คลอไรต์ และคลอเรตเรื้อรังต่ออาสาสมัครชายวัยผู้ใหญ่ที่มีสุขภาพดี วารสารพยาธิวิทยา พิษวิทยา และมะเร็งวิทยา 5(4-5):229-238.
Luo JD, Wang YY, Fu WL, Wu J, Chen AF (2004). การบำบัดด้วยยีนของเอนโดธีเลียลไนตริกออกไซด์ซินเทสและแมงกานีสซูเปอร์ออกไซด์ดิสมิวเทส ช่วยฟื้นฟูการสมานแผลที่ล่าช้าในหนูเบาหวานประเภท 1
Circulation 110(16):2484-2493
Maraprygsavan P, Mongkolsuk J, Arnhold J, Kuehne FW (2016). ยา WF10 ที่มีคลอไรต์เป็นส่วนประกอบ ช่วยลดค่าฮีโมโกลบิน A1c อย่างต่อเนื่อง และปรับปรุงการควบคุมระดับน้ำตาลในผู้ป่วยเบาหวานที่มีภาวะเท้าบวมรุนแรง วารสาร Clinical and Translational Endocrinology 4:53-58. https://doi.org/10.1016/j.jcte.2016.05.001
Markuson M, Hanson D, Anderson J, Langemo D, Hunter S, Thompson P, Paulson R, Rustvang D (2009). ความสัมพันธ์ระหว่างค่าฮีโมโกลบิน A1c และระยะเวลาการหายของแผลที่ขาในผู้ป่วยโรคเบาหวาน Advances in Skin and Wound Care 22(8):365-372. 10.1097/01.ASW.0000358639.45784.cd
Marston WA (2006). ปัจจัยเสี่ยงที่เกี่ยวข้องกับการหายของแผลเรื้อรังแผลเบาหวานที่เท้า: ความสำคัญของภาวะน้ำตาลในเลือดสูง Ostomy/Wound Management 52(3):26-8.
Mawas AS, Salah S, Khalil AM, Mohi Eldin MM. (2022). การเสริมคุณสมบัติการหายของแผลเบาหวานหลังจากการใช้เจลน้ำมันงา และคลอรีนไดออกไซด์เฉพาะที่ในหนูขาว วารสาร Alexandria สำหรับวิทยาศาสตร์สัตวแพทย์ 73(1). 10.5455/ajvs.76784
McGrath MS, Benike C, Kuehne FW, Engleman E (1998). ผลของ WF10 (TCDO) ต่อการนำเสนอแอนติเจน ใน Transplantation Proceedings Vol. 30(8):4200-4204. Elsevier Science.
McMahon M, Bistrian BR (1995). การป้องกันของโฮสต์และความอ่อนแอต่อการติดเชื้อในผู้ป่วยโรคเบาหวาน Infectious Disease Clinics of North America 9(1):1-9.
McNeely MJ, Boyko EJ, Ahroni JH, Stensel VL, Reiber GE, Smith DG, Pecoraro RE (1995). การมีส่วนร่วมที่เป็นอิสระของโรคเส้นประสาทและหลอดเลือดจากเบาหวานในการเกิดแผลที่เท้า: ความเสี่ยงมีมากเพียงใด Diabetes Care 18(2):216-219.
Miller RG, Block G, Katz JS, Barohn RJ, Gopalakrishnan V, Cudkowicz M, Zhang JR, McGrath MS, Ludington E (2015). การทดลองแบบสุ่มระยะที่ 2 ของ NP001 ซึ่งเป็นตัวควบคุมภูมิคุ้มกันชนิดใหม่: ความปลอดภัยและประสิทธิภาพเบื้องต้นใน ALS Neurology-Neuroimmunology Neuroinflammation 2(3). https://doi.org/10.1212/NXI.0000000000000100
Miller RG, Zhang R, Block G, Katz J, Barohn R, Kasarskis E, Forshew D, Gopalakrishnan V, McGrath MS (2014). การควบคุม NP001 ของตัวบ่งชี้การกระตุ้นของแมโครฟาจใน ALS: การศึกษาทางคลินิกระยะที่ 1 และการศึกษาตัวบ่งชี้ทางชีวภาพ โรคกล้ามเนื้ออ่อนแรง Amyotrophic Lateral Sclerosis และความเสื่อมของสมองส่วนหน้าและส่วนขมับ 15(7-8):601-609. https://doi.org/10.3109/21678421.2014.951940
Mueller-Klieser W, Vaupel P (1987). การปรับปรุงการออกซิเจนของทรงกลมเนื้องอกโดยเตตระคลอโรเดคาออกไซด์ วารสารนานาชาติของรังสีวิทยา* ชีววิทยา* ฟิสิกส์ 13(1):49-54. https://doi.org/10.1016/0360-3016(87)90259-8
Negi G, Kumar A, Joshi RP, Ruby PK, Sharma SS. (2011). ความเครียดจากออกซิเดชันและโรคเส้นประสาทเบาหวาน: สถานะปัจจุบันของสารต้านอนุมูลอิสระ วารสารสถาบันอินทิเกรทีฟโอมิกส์และเทคโนโลยีชีวภาพประยุกต์ 2(6):71-78. Neuvivo. สืบค้นเมื่อจาก Neuvivo.com เข้าถึงเมื่อ 10-1-2022.
Nishikawa T, Edelstein D, Brownlee M (2000) จุดเชื่อมโยงที่หายไป: กลไกเดียวที่รวมภาวะแทรกซ้อนของโรคเบาหวาน Kidney International 58:S26-S30. https://doi.org/10.1046/j.1523-1755.2000.07705.x
Ogata N, Miura T (2020). การยับยั้งการจับตัวของโปรตีนหนามของไวรัสโคโรนา SARS-CoV-2 กับเอนไซม์ angiotensin-converting enzyme 2 ของมนุษย์โดยคลอรีนไดออกไซด์ วารสารเภสัชวิทยาและเภสัชกรรม
5(5):1195.
Ogata N, Miura T (2021). การยับยั้งการจับตัวของโปรตีนหนามของไวรัสโคโรนา SARS-CoV-2 กับตัวรับของมนุษย์โดยคลอรีนไดออกไซด์ วารสารเภสัชวิทยาและเภสัชกรรม 6(1):1199.
Ogata N, Shibata T (2009). ผลของก๊าซคลอรีนไดออกไซด์ที่มีความเข้มข้นต่ำมากต่อการขาดเรียนของเด็กนักเรียน วารสารการแพทย์และวิทยาศาสตร์การแพทย์นานาชาติ 1(7):288-289.
Pang L, Lian X, Liu H, Zhang Y, Li Q, Cai Y, Ma H, Yu X (2020).ทำความเข้าใจเกี่ยวกับโรคเส้นประสาทเบาหวาน: เน้นที่ความเครียดจากออกซิเดชัน Oxidative Medicine and Cellular Longevity 2020:1-13.
https://doi.org/10.1155/2020/9524635
Peredo-Lovillo A, Romero-Luna HE, Juárez-Trujillo N, Jiménez-Fernández M (2023). ประสิทธิภาพในการต้านจุลชีพของคลอรีนไดออกไซด์และศักยภาพในการใช้เป็นสารต้าน SARS-CoV-2: กลไกการออกฤทธิ์ และการมีปฏิสัมพันธ์กับจุลินทรีย์ในลำไส้ Journal of Applied Microbiology 134(7):lxad133.
Pozzilli P, Leslie RDG (1994). การติดเชื้อและโรคเบาหวาน: กลไกและโอกาสในการป้องกัน Diabetic Medicine 11(10):935-941.
Prasad C, Davis KE, Imrhan V, Juma S, Vijayagopal P (2019). ผลิตภัณฑ์ขั้นปลายของการเกิดไกลเคชั่นขั้นสูงและความเสี่ยงต่อโรคเรื้อรัง: การแทรกแซงผ่านการปรับเปลี่ยนวิถีชีวิต วารสารอเมริกันของ
เวชศาสตร์วิถีชีวิต 13(4):384-404.
PubChem (2018). คลอรีนไดออกไซด์ เข้าถึงได้จาก: https://pubchem.ncbi.nlm.nih.gov/source/hsdb/517 เข้าถึงเมื่อ 10-1-2022.
Raffanti SP, Schaffner W, Federspiel CF, Blackwell RB, Ching OA, Kühne FW (1998). การทดลองแบบสุ่ม แบบปกปิดสองทาง ควบคุมด้วยยาหลอกของตัวปรับภูมิคุ้มกัน WF10 ในผู้ป่วยโรคเอดส์ขั้นรุนแรง
การติดเชื้อ 26(4):202-207. https://doi.org/10.1007/BF02962364
Ramirez-Acuña JM, Cardenas-Cadena SA, Marquez-Salas PA, Garza-Veloz I, Perez-Favila A, Cid-Baez MA, Flores-Morales V, Martinez-Fierro ML (2019). แผลที่เท้าจากโรคเบาหวาน: ความก้าวหน้าในปัจจุบันของการบำบัดด้วยยาต้านจุลชีพและการรักษาที่กำลังเกิดขึ้นใหม่ ยาปฏิชีวนะ 8(4):193. https://doi.org/10.3390/antibiotics8040193
Rask-Madsen C, King GL (2013). ภาวะแทรกซ้อนของหลอดเลือดจากโรคเบาหวาน: กลไกการบาดเจ็บและปัจจัยป้องกัน การเผาผลาญของเซลล์ 17(1):20-33. http://dx.doi.org/10.1016/j.cmet.2012.11.012
Redding WR, Booth LC (1991). ผลของคลอร์เฮกซิดีนกลูโคเนตและกรดคลอรัส-คลอรีนไดออกไซด์ต่อไฟโบรบลาสต์ของม้าและ Staphylococcus aureus ศัลยกรรมสัตวแพทย์ 20(5):306-310. https://doi.org/10.1111/j.1532-950X.1991.tb01272.x
Richard JL, Schuldiner S (2008). ระบาดวิทยาของปัญหาเท้าจากโรคเบาหวาน [Epidemiology of diabetic foot problems]. Revue de Médecine Interne 29(Suppl. 2):S222-S230. https://doi.org/10.1016/S0248-8663(08)73949-3
Saeedi P, Petersohn I, Salpea P, Malanda B, Karuranga S, Unwin N, โคลากิอูรี เอส, กวาริกัวต้า แอล, โมตาล่า เอเอ, โอกูร์ทโซวา เค, ชอว์ เจอี (2019) ประมาณการความชุกของโรคเบาหวานทั่วโลกและระดับภูมิภาคในปี 2562 และการคาดการณ์สำหรับปี 2573 และ 2588: ผลลัพธ์จากนานาชาติสมาพันธ์เบาหวาน Atlas เบาหวาน การวิจัยโรคเบาหวานและคลินิกแบบฝึกหัด 157:107843. https://doi.org/10.1016/j.diabres.2019.107843
ซาเนกาตะ ที, ฟุกุดะ ที, มิอุระ ที, โมริโนะ เอช, ลี ซี, มาเอดะ เคอี, อารากิ เค, โอตาเกะ ที, คาวาฮาตะ ที, ชิบาตะ ที (2010) การประเมินฤทธิ์ต้านไวรัสของคลอรีนไดออกไซด์และโซเดียมไฮโปคลอไรต์ต่อไวรัส
calicivirus ในแมว, ไวรัสไข้หวัดใหญ่ในมนุษย์, ไวรัสโรคหัด, ไวรัสไข้หัดสุนัข, ไวรัสเริมในมนุษย์, ไวรัสอะดีโนในมนุษย์, ไวรัสอะดีโนในสุนัข และไวรัสพาร์โวในสุนัข Biocontrol Science 15(2):45-49.
https://doi.org/10.4265/bio.15.45
Schempp H, Reim M, Dornisch K, Elstner EF (2001). ปฏิสัมพันธ์ระหว่างคลอไรต์กับโปรตีนฮีโมโกลบินเป็นบทบาทสำคัญต่อฤทธิ์ทางเภสัชวิทยาของยา WF10 ที่มีคลอไรต์เป็นส่วนประกอบ Arzneimittelforschung 51(07):554-562.10.1055/s-0031-1300079
Schönberg M, Schlorke D, Arnhold J (2016). ผลกระทบของ WF10 ต่อการซัลเฟตของไกลโคซามิโนไกลแคนในโมโนไซต์และมาโครฟาจที่ก่อให้เกิดการอักเสบ บทที่ 5 ใน Flow Cytometry-Select Topics
IntechOpen http://dx.doi.org/10.5772/60862
Sheetz MJ, King GL (2002). ความเข้าใจเชิงโมเลกุลเกี่ยวกับผลเสียของภาวะน้ำตาลในเลือดสูงต่อภาวะแทรกซ้อนของโรคเบาหวาน วารสารของสมาคมการแพทย์อเมริกัน 288(20):2579-2588 10.1001/jama.288.20.2579
Sidgwick NV (1950). ธาตุเคมีและสารประกอบของพวกมันเล่ม 2 อ็อกซ์ฟอร์ด: Clarendon Press
Simpson GD, Miller RF, Laxton GD, Clements WR (1993). เน้นที่คลอรีนไดออกไซด์: สารฆ่าเชื้อ “ในอุดมคติ” ใน: การกัดกร่อน – การประชุมประจำปีของสมาคมวิศวกรการกัดกร่อนแห่งชาติมีให้ที่:
http://www.clo2.gr/en/pdf/secure/chlorinedioxideidealbiocide.pdf
Singh N, Armstrong DG, Lipsky BA (2005). การป้องกันแผลที่เท้าในผู้ป่วยโรคเบาหวาน วารสารสมาคมการแพทย์อเมริกัน 293(2):217-228.10.1001/jama.293.2.217
Syafril S (2018). พยาธิสรีรวิทยาของแผลที่เท้าจากโรคเบาหวาน IOP Conference Series: Earth and Environmental Science 125(1). IOP Publishing, 2018.10.1088/1755-1315/125/1/012161
Thiruvoipati T, Kielhorn CE, Armstrong EJ (2015). โรคหลอดเลือดแดงส่วนปลายในผู้ป่วยเบาหวาน: ระบาดวิทยา กลไก และผลลัพธ์ World Journal of Diabetes 6(7):961. 10.4239/wjd.v6.i7.961
Tissot M, Roch-Arveiller M, Mathieu J, Giroud JP, Stahl KW (1990) คุณสมบัติต้านการอักเสบของสารรักษาบาดแผลและปรับภูมิคุ้มกันชนิดใหม่ สารประกอบเตตระคลอโรเดคาออกซีเจน (TCDO) Agents and Actions 31(3):368-374.
Tuthill RW, Giusti RA, Moore GS, Calabrese EJ (1982). ผลกระทบต่อสุขภาพในทารกแรกเกิดหลังจากการสัมผัสกับน้ำดื่มที่ฆ่าเชื้อด้วย ClO2 ในช่วงก่อนคลอด Environmental Health Perspectives 46:39-45.
https://doi.org/10.1289/ehp.824639
Ullmann U, Kühne FW (1985). การตรวจสอบในหลอดทดลองเกี่ยวกับฤทธิ์ต้านแบคทีเรียและอิทธิพลต่อการเรืองแสงเคมีของฟาโกไซต์ของ tetrachlorodecaoxide—สารประกอบออกซิเจนที่ไม่ใช่โลหะชนิดใหม่ Infection 13(2):S236-S240. https://doi.org/10.1007/BF01644437
กระทรวงสาธารณสุขและบริการมนุษย์แห่งสหรัฐอเมริกา (2004). ข้อมูลพิษวิทยาสำหรับคลอรีนไดออกไซด์และคลอไรต์ เข้าถึงได้ที่: https://www.atsdr.cdc.gov/toxprofiles/tp160.pdf. เข้าถึงเมื่อ 1 ตุลาคม 2022.
สำนักงานคณะกรรมการอาหารและยาแห่งสหรัฐอเมริกา (2019). อันตราย: อย่าดื่ม Miracle Mineral Solution หรือผลิตภัณฑ์ที่คล้ายคลึงกัน เข้าถึงได้ที่: https://www.fda.gov/consumers/consumer-updates/danger-dontdrink-miracle-mineral-solution-or-similar-products. เข้าถึงเมื่อ 1 ตุลาคม 2022.
Valente JH, Jay GD, Zabbo CP, Reinert SE, Bertsch K (2014). สารละลายคลอรีนไดออกไซด์ที่ออกฤทธิ์สามารถใช้เป็นสารล้างแผลฆ่าเชื้อที่เข้ากันได้ทางชีวภาพได้ ความก้าวหน้าในการดูแลผิวหนังและบาดแผล
27(1):13-19. 10.1097/01.ASW.0000439060.79822.b3
Vincent AM, Russell JW, Low P, Feldman EL (2004). ความเครียดออกซิเดชันในการเกิดโรคของเส้นประสาทเบาหวาน Endocrine Reviews 25(4):612-628. https://doi.org/10.1210/er.2003-0019
Volmer-Thole M, Lobmann R (2016). โรคเส้นประสาทและกลุ่มอาการเท้าเบาหวาน International Journal of Molecular Sciences 17(6):917. https://doi.org/10.3390/ijms17060917
Volpe CM, Villar-Delfino PH, Dos Anjos PM, Nogueira-Machado JA (2018). การตายของเซลล์ สารออกซิเจนที่ว่องไว (ROS) และภาวะแทรกซ้อนของโรคเบาหวานเซลล์ตายและโรค 9(2):1-9. https://doi.org/10.1038/s41419-017-0135-z
Wabnitz GH, Samstag Y (2016). การลดการทำงานของเซลล์ T ที่เกิดจากออกซิเดชัน Cell Death and Disease 7(9):e2373. https://doi.org/10.1038/cddis.2016.273
Wassmann S, Wassmann K, Nickenig G (2004). การปรับเปลี่ยนการแสดงออกและการทำงานของเอนไซม์ออกซิแดนต์ และสารต้านอนุมูลอิสระในเซลล์หลอดเลือด Hypertension 44(4):381-386.
https://doi.org/10.1161/01.HYP.0000142232.29764.a7
Wei W, Liu Q, Tan Y, Liu L, Li X, Cai L (2009). ความเครียดจากออกซิเดชัน โรคเบาหวาน และภาวะแทรกซ้อนจากโรคเบาหวาน Hemoglobin 33(5):370-377. https://doi.org/10.3109/03630260903212175
Wilkins RJ (2014). การจัดการบาดแผลผ่าตัดในสุนัขโดยใช้สารละลายฆ่าเชื้อคลอรีนไดออกไซด์ที่มีความเสถียรและดีขึ้น วารสารสัตวแพทยศาสตร์และการเลี้ยงสัตว์ 1:403. 10.15744/2348-9790.1.403
Woerly G, Lombard Y, Stahl KW, Poindron P (1986). ความสามารถของสารเชิงซ้อนแอนไอออนเตตระคลอโรเดคาออกซีเจนและแบคทีเรียไลโปโพลีแซคคาไรด์ในการเร่งการกลืนกินของเซลล์แมโครฟาจของหนูปกติที่เพาะเลี้ยงย่อย บทคัดย่อ การประชุมนานาชาติว่าด้วยแง่มุมทางชีววิทยาและทางคลินิกของการทำงานของฟาโกไซต์ ปาเวีย อิตาลี
Wolff SP, Dean RT (1987). การออกซิเดชันของกลูโคสและการดัดแปลงโปรตีน บทบาทที่เป็นไปได้ของ ‘การไกลโคซิเลชันแบบออโตออกซิเดชัน’ ในโรคเบาหวาน วารสารชีวเคมี 245(1):243-250 https://doi.org/10.1042/bj2450243
Yasuda M, Ohzeki Y, Shimizu S, Naito S, Ohtsuru A, Yamamoto T, Kuroiwa Y (1998). การกระตุ้นการสร้างหลอดเลือดใหม่ในหลอดทดลองโดยไฮโดรเจนเปอร์ออกไซด์และความสัมพันธ์กับ ETS-1 ในเซลล์เยื่อบุหลอดเลือด Life Sciences 64(4):249-258. https://doi.org/10.1016/S0024-3205(98)00560-8
Yingsakmongkol N, Maraprygsavan P, Sukosit P (2011). ผลของ WF10 (อิมมูโนไคน์) ต่อการรักษาแผลที่เท้าจากโรคเบาหวาน: การทดลองแบบสุ่มสองทาง ควบคุมด้วยยาหลอก The Journal of Foot and Ankle
Surgery 50(6):635-640. https://doi.org/10.1053/j.jfas.2011.05.006
Yingsakmongkol N (2013). ผลลัพธ์ทางคลินิกของการใช้ WF10 ร่วมกับการรักษาแผลที่เท้าจากเบาหวานตามมาตรฐาน วารสารการดูแลแผล 22(3):130-136. https://doi.org/10.12968/jowc.2013.22.3.130
Yingsakmongkol N, Tanunyutthawongse C, Flemmig J, Kuehne F-W (2021). ผลของยา WF10 ที่มีคลอไรต์เป็นส่วนประกอบต่อฮีโมโกลบิน A1c และตัวบ่งชี้ทางโลหิตวิทยาในผู้ป่วยเบาหวานที่ควบคุมระดับน้ำตาลไม่ได้และมีแผลที่เท้าวารสารโรคเบาหวานและการรักษา 6:1086. https://doi.org/10.29011/2574-7568.001086
Zhu Z, Guo Y, Yu P, Wang X, Zhang X, Dong W, Liu X, Guo C (2019). คลอรีนไดออกไซด์ยับยั้งการจำลองแบบของไวรัสโรคระบบสืบพันธุ์และระบบทางเดินหายใจในสุกรโดยการปิดกั้นการเกาะติดของไวรัส การติดเชื้อ, พันธุศาสตร์และวิวัฒนาการ 67:78-87. https://doi.org/10.1016/j.meegid.2018.11.002