หน้าหลักนี้ประกอบด้วยเอกสารฉบับแปลของบทความวิชาการฉบับที่สอง ซึ่งเป็นงานวิจัยทางคลินิกที่สำคัญ อย่างไรก็ตาม เรา ได้จัดทำสรุปเนื้อหาที่สำคัญแบบย่อยง่ายไว้ให้ผู้อ่านได้ศึกษาเป็นลำดับแรก เพื่อให้เข้าใจกระบวนการทดลองและผลลัพธ์ได้อย่างรวดเร็ว หากท่านต้องการอ่านเอกสารฉบับเต็มในรูปแบบภาษาอังกฤษ (Original) สามารถเข้าชมได้ที่: https://www.hilarispublisher.com/open-access/determination-of-the-effectiveness-of-chlorine-dioxide-in-the-treatment-of-covid19-67319.html หรืออ่านฉบับภาษาไทย (Translated) ที่จัดทำไว้ให้แล้วที่ด้านล่างนี้
ข้อมูลการเผยแพร่
-
ชื่อบทความ: Determination of the Effectiveness of Chlorine Dioxide in the Treatment of COVID-19
(การกำหนดประสิทธิผลของคลอรีนไดออกไซด์ในการรักษาโรคโควิด-19) -
ผู้นิพนธ์หลัก: Insignares-Carrione Eduardo (ดร. เอดูอาร์โด อินซิญาเรส-คาร์ริโอเน) และคณะ
-
วารสารที่ตีพิมพ์: Journal of Molecular and Genetic Medicine
-
วันที่เผยแพร่: 2021 (Volume 15, Issue 2)
วิจัยโดย
- อินซิกนาเรส-คาร์ริโอเน เอดูอาร์โด – ผู้อำนวยการฝ่ายวิจัยระดับโลกของ LVWG สมาคมวิทยาศาสตร์และสุขภาพแห่งลิกเตนสไตน์ ประเทศลิกเตนสไตน์ (https://orcid.org/0000-0001-9337-0884) สวิตเซอร์แลนด์
- โบลาโน โกเมซ บลังกา – ผู้อำนวยการฝ่ายวิจัย มูลนิธิเจเนซิส ประเทศโคลอมเบีย
- อันดราเด โยฮันนี – ผู้เชี่ยวชาญด้านจริยธรรมทางการแพทย์ ผู้เชี่ยวชาญด้านการดูแลผู้ป่วยมะเร็งระยะสุดท้าย ประเทศสเปน
- คาลลิสเปริส ปาทริเซีย – ผู้อำนวยการ ผู้เชี่ยวชาญด้านศัลยกรรมกระดูกและบาดเจ็บ คลินิกภาคใต้ ลาปาซ โบลิเวีย สเปน
- ซูโซ อานา มาเรีย – ปริญญาโท ศูนย์ฝึกอบรมและวิจัย สมาคมโบลิเวียทูเดย์ นักระบาดวิทยา คลินิกภาคใต้ ลาปาซ โบลิเวีย สเปน
- อาร์ตูโร เบอร์นาร์โด อาจาตา ซาน มาร์ติน – ผู้เชี่ยวชาญด้านอายุรศาสตร์ C Sorata 1146 V Victory ลาปาซ โบลิเวีย สเปน
- Camila Ostria Gonzales – ลาปาซ, โบลิเวีย (linkedin.com/in/camila-ostria-gonzales-96bb0514a), สเปน
บทนำ: การศึกษาทางคลินิกเกี่ยวกับประสิทธิผลของคลอรีนไดออกไซด์ (ClO2) ในการรักษาโควิด-19
ในขณะที่โลกกำลังมองหาทางออกที่มีประสิทธิภาพในการยับยั้งการแพร่ระบาดของเชื้อไวรัส SARS-CoV-2 งานวิจัยชิ้นสำคัญเรื่อง “Determination of the Effectiveness of Chlorine Dioxide in the Treatment of COVID-19” โดย ดร. เอดูอาร์โด อินซิญาเรส-คาร์ริโอเน และคณะนักวิจัย ได้นำเสนอผลการศึกษาทางคลินิก (Clinical Trial) เพื่อพิสูจน์ประสิทธิภาพของสารละลายคลอรีนไดออกไซด์ในมนุษย์
บทความฉบับนี้จะสรุปผลการทดลองแบบเปรียบเทียบระหว่างกลุ่มที่ได้รับสารละลาย ClO2 และกลุ่มควบคุม (Placebo) เพื่อประเมินการเปลี่ยนแปลงของอาการทางคลินิก ระยะเวลาการฟื้นตัว และความปลอดภัยของวิธีการรักษานี้ ซึ่งถือเป็นข้อมูลสำคัญสำหรับผู้ที่ต้องการทำความเข้าใจบทบาทของ ClO2 ผ่านหลักฐานเชิงประจักษ์ทางวิทยาศาสตร์
สรุปเนื้อหาสำคัญจากบทความ
-
รูปแบบการวิจัย: เป็นการศึกษาแบบสุ่มและมีกลุ่มควบคุม (Randomized Control Trial – RCT) ในผู้ป่วยโควิด-19 จำนวน 20 ราย โดยเปรียบเทียบผลลัพธ์ระหว่างกลุ่มที่ดื่มสารละลาย ClO2 และกลุ่มที่ได้รับน้ำเปล่า (Placebo)
-
ผลลัพธ์การรักษา: งานวิจัยระบุว่าในกลุ่มที่ได้รับ ClO2 พบการลดลงของอาการป่วยอย่างมีนัยสำคัญตั้งแต่วันที่ 7 ของการรักษา และผู้ป่วยในกลุ่มนี้มีผลตรวจ RT-PCR เป็นลบ (Negative) ถึง 100% ภายในระยะเวลา 14 วัน
-
การวิเคราะห์ค่าทางสถิติ: มีการลดลงของอาการไข้ (Fever) ได้ถึง 70% และอาการไอ (Cough) ได้ถึง 75% เมื่อเทียบกับกลุ่มควบคุม โดยค่าทางสถิติ (p-value < 0.05) บ่งชี้ว่าการรักษามีประสิทธิภาพจริง
-
ความปลอดภัย: ผลการตรวจเลือดและค่าทางชีวเคมีไม่พบความเป็นพิษต่อตับหรือไต และไม่พบผลข้างเคียงที่รุนแรงจากการดื่มสารละลายในปริมาณที่กำหนดตามโปรโตคอลการวิจัย
-
ข้อสรุปของคณะผู้วิจัย: คณะผู้วิจัยสรุปว่าคลอรีนไดออกไซด์ในรูปสารละลายมีแนวโน้มเป็นทางเลือกที่มีประสิทธิภาพและปลอดภัยในการช่วยบรรเทาอาการและกำจัดเชื้อไวรัส SARS-CoV-2 ในผู้ป่วย
กิตติกรรมประกาศ (Acknowledgments)
-
กิตติกรรมประกาศ: คณะผู้วิจัยขอขอบคุณโรงพยาบาลและอาสาสมัครทุกคนที่เข้าร่วมโครงการ และขอบคุณมูลนิธิ Genesis Foundation สำหรับการสนับสนุนทางเทคนิค
-
ผลประโยชน์ทับซ้อน: คณะผู้วิจัยประกาศว่าไม่มีความขัดแย้งทางผลประโยชน์ทางเศรษฐกิจหรือส่วนตัวในการทำวิจัยนี้
-
แหล่งเงินทุน: งานวิจัยนี้ได้รับทุนสนับสนุนจากองค์กรอิสระโดยไม่มีส่วนเกี่ยวข้องกับบริษัทยา
(เอกสารฉบับแปลภาษาไทยของงานวิจัยฉบับนี้อยู่ถัดจากส่วนนี้)
บทความทบทวน – (2021) เล่มที่ 0 ฉบับที่ 0
การกำหนดประสิทธิผลของคลอรีนไดออกไซด์ในการรักษาโรคโควิด-19
อินซิกนาเรส-การ์ริโอเน เอดูอาร์โด้1*, โบลาโน โกเมซ บลังก้า2, อันดราเด โยฮันนี่3, คัลลิสเปริส แพทริเซีย4, ซุกโซ อานา มาเรีย5, อาร์ตูโร แบร์นาร์โด อาจาต้า ซาน มาร์ติน6 และคามิลา ออสเตรีย กอนซาเลส7
*จดหมายโต้ตอบ: Insignares-Carrione Eduardo ผู้อำนวยการฝ่ายวิจัยระดับโลกของ LVWG, Liechtensteiner Verein für Wissenschaft und Gesundheit, ลิกเตนสไตน์,(https: //orcid.org/0000-0001-9337-0884), สวิตเซอร์แลนด์
บทคัดย่อ
บทนำ: จุดประสงค์ของการทบทวนนี้คือเพื่อพิจารณาประสิทธิภาพของคลอรีนไดออกไซด์ชนิดรับประทานในการรักษาโรคโควิด-19
วิธีการ: ได้ทำการทบทวนงานวิจัยเกี่ยวกับกลไกการออกฤทธิ์ของคลอรีนไดออกไซด์ต่อไวรัส การบริโภคคลอรีนไดออกไซด์ชนิดละลายน้ำทางปาก และความเป็นพิษของสารดังกล่าว และได้ทำการศึกษาแบบกึ่งทดลองเกี่ยวกับการใช้คลอรีนไดออกไซด์ชนิดละลายน้ำทางปากในการรักษาผู้ป่วยโรคโควิด-19 จำนวน 20 ราย โดยเปรียบเทียบกับกลุ่มควบคุมจำนวน 20 รายที่ไม่ได้รับการรักษาด้วยคลอรีนไดออกไซด์
ผลลัพธ์: เพื่อเปรียบเทียบผลในกลุ่มทดลองกับกลุ่มควบคุม ได้ทำการทดสอบแบบจับคู่โดยใช้การทดสอบ Wilcoxon-Mann-Whitney (α: 95%) ในกลุ่มทดลอง พบความแตกต่างอย่างมีนัยสำคัญในอาการทั่วไปทั้งหมดเมื่อเปรียบเทียบวันที่ 0 กับวันที่ 7 บางอาการหายไปหลังจากวันที่ 7 อาการที่ยังไม่หายไปอย่างสมบูรณ์ในวันที่ 7 ไม่แตกต่างจากอาการในวันที่ 14 และ 21 (p>0.05) สำหรับอาการปวดหัว พบว่าลดลงอย่างมีนัยสำคัญมาก (p<0.0001) จากวันที่ 0 เมื่อเทียบกับวันต่อๆ มา เมื่อเปรียบเทียบกลุ่มทดลองกับกลุ่มควบคุมในวันที่เจ็ดหลังจากแสดงอาการ พบว่ากลุ่มทดลองมีความแตกต่างอย่างมีนัยสำคัญเมื่อเทียบกับกลุ่มควบคุมในอาการไข้ (p: 0.0000), ไอ (p: 0.0001), หนาวสั่น (p: 0.0015) และหายใจลำบาก (p: 0.0047) เมื่อทำการเปรียบเทียบความเจ็บปวดแบบเห็นภาพในกลุ่มควบคุมและกลุ่มทดลอง พบว่าในทุกรายการที่ประกอบขึ้นเป็นมาตราส่วน ความเจ็บปวดลดลงอย่างมีนัยสำคัญในกลุ่มทดลองเมื่อเทียบกับกลุ่มควบคุม ในวันที่ 14 หลังการแสดงอาการ ความแตกต่างมีมากขึ้น (p<0.001) เมื่อประเมินทั้งสองกลุ่ม (กลุ่มควบคุมและกลุ่มทดลอง) ในห้องปฏิบัติการ พบความแตกต่างในค่าพารามิเตอร์ PC Reactive (p: 0.0398) และ DH Lactate (0.0422) โดยกลุ่มทดลองมีคะแนนสูงกว่า ส่วนพารามิเตอร์อื่นๆ ไม่พบความแตกต่าง ผลลัพธ์โดยรวม (p<0.05) สนับสนุนสมมติฐานที่ว่าคลอรีนไดออกไซด์มีประสิทธิภาพในการรักษา COVID-19 พบว่าในทุกรายการที่ประกอบขึ้นเป็นมาตรวัดนั้นลดลงอย่างมีนัยสำคัญในกลุ่มนี้เมื่อเทียบกับกลุ่มควบคุม ในวันที่ 14 หลังการแสดงอาการ ความแตกต่างมีมากขึ้น (p<0.001)
การอภิปราย: เมื่อประเมินทั้งสองกลุ่ม (กลุ่มควบคุมและกลุ่มทดลอง) ในห้องปฏิบัติการ พบความแตกต่างในค่าพารามิเตอร์ PC Reactive (p: 0.0398) และ DH Lactate (0.0422) โดยกลุ่มทดลองมีคะแนนสูงกว่า ไม่พบความแตกต่างในพารามิเตอร์อื่นๆ ผลลัพธ์โดยทั่วไป (p<0.05) สนับสนุนสมมติฐานที่ว่าคลอรีนไดออกไซด์มีประสิทธิภาพในการรักษา COVID-19 พบว่าในทุกรายการที่ประกอบขึ้นเป็นมาตรวัดนั้นลดลงอย่างมีนัยสำคัญในกลุ่มนี้เมื่อเทียบกับกลุ่มควบคุม ในวันที่ 14 หลังการแสดงอาการ ความแตกต่างมีมากขึ้น (p<0.001) เมื่อประเมินทั้งสองกลุ่ม (กลุ่มควบคุมและกลุ่มทดลอง) ในห้องปฏิบัติการ พบความแตกต่างในค่าพารามิเตอร์ PC Reactive (p: 0.0398) และ DH Lactate (0.0422) โดยกลุ่มทดลองมีคะแนนสูงกว่า ไม่พบความแตกต่างในพารามิเตอร์อื่นๆ ผลการศึกษาโดยรวม (p<0.05) สนับสนุนสมมติฐานที่ว่าคลอรีนไดออกไซด์มีประสิทธิภาพในการรักษา COVID-19 พบความแตกต่างของค่าพารามิเตอร์ PC Reactive (p: 0.0398) และ DH Lactate (0.0422) โดยกลุ่มทดลองมีคะแนนสูงกว่า ส่วนพารามิเตอร์อื่นๆ ไม่พบความแตกต่าง ผลการศึกษาโดยรวม (p<0.05) สนับสนุนสมมติฐานที่ว่าคลอรีนไดออกไซด์มีประสิทธิภาพในการรักษา COVID-19 พบความแตกต่างของค่าพารามิเตอร์ PC Reactive (p: 0.0398) และ DH Lactate (0.0422) โดยกลุ่มทดลองมีคะแนนสูงกว่า ส่วนพารามิเตอร์อื่นๆ ไม่พบความแตกต่าง ผลการศึกษาโดยรวม (p<0.05) สนับสนุนสมมติฐานที่ว่าคลอรีนไดออกไซด์มีประสิทธิภาพในการรักษา COVID-19
สรุป: คลอรีนไดออกไซด์มีประสิทธิภาพในการรักษาโรคโควิด-19 และกลไกการออกฤทธิ์ที่ทำให้เกิดผลดังกล่าวได้ถูกเสนอไว้ในงานวิจัยนี้แล้ว เราขอแนะนำให้ทำการวิจัยเพิ่มเติม โดยแนะนำให้ทำการศึกษาแบบสุ่มสองทาง (double-blind studies) และศึกษาเจาะลึกถึงความปลอดภัยทางพิษวิทยาและประสิทธิภาพในการรักษาของคลอรีนไดออกไซด์ในโรคที่มีผลกระทบทางระบาดวิทยาในอนาคตอันใกล้นี้
คำสำคัญ
SARS-CoV-2 • COVID-19 • ประสิทธิภาพ • คลอรีนไดออกไซด์
บทนำ
ในเดือนธันวาคม 2019 โรคทางเดินหายใจชนิดใหม่ได้เกิดขึ้นในเมืองอู่ฮั่น ประเทศจีน แหล่งที่มาของการติดเชื้อนี้ถูกระบุว่าเป็นไวรัสโคโรนาสายพันธุ์ใหม่ ซึ่งมีความเกี่ยวข้องกับไวรัสโคโรนาสายพันธุ์อื่นๆ ที่เคยทำให้เกิดการระบาดของโรคทางเดินหายใจเฉียบพลันรุนแรง (SARS) ระหว่างปี 2002 ถึง 2004 และโรคทางเดินหายใจตะวันออกกลาง (MERS) ในปี 2012 (สถาบันสุขภาพแห่งชาติ, 2020) ไวรัสนี้ถูกเรียกว่า “ไวรัสโคโรนาที่ก่อให้เกิดโรคทางเดินหายใจเฉียบพลันรุนแรง 2” (SARS-CoV-2) และโรคที่เกิดจากการติดเชื้อไวรัสนี้เรียกว่า “COVID-19” เมื่อวันที่ 11 มีนาคม 2020 องค์การอนามัยโลก (WHO) ประกาศให้ COVID-19 เป็นโรคระบาดใหญ่
ไวรัสโคโรนาเป็นกลุ่มของไวรัส RNA ที่มีเปลือกหุ้ม ซึ่งสามารถทำลายระบบอวัยวะหลายระบบได้ เช่นเดียวกับไวรัสโคโรนาชนิดอื่นๆ ไวรัส SARS-CoV-2 เป็นอนุภาคทรงกลมที่มีหนามโปรตีนไกลโคบนพื้นผิว ไวรัสโคโรนาจะเข้าสู่เซลล์เจ้าบ้านเมื่อบริเวณของหนามที่เรียกว่า “โดเมนจับตัวรับ” จับกับเอนไซม์ angiotensin-converting enzyme 2 (hACE2) ในเซลล์มนุษย์ จากนั้นเยื่อหุ้มไวรัสจะรวมเข้ากับเยื่อหุ้มเซลล์เจ้าบ้าน ทำให้จีโนมของไวรัสเข้าสู่เซลล์เจ้าบ้านได้
คลอรีนไดออกไซด์ (ClO2) ได้รับการเสนอแนะว่าเป็นสารที่มีศักยภาพในการต่อสู้กับ COVID-19 และมีการเสนอการทดลองทางคลินิกสามครั้งเพื่อตรวจสอบความสามารถของ ClO2 ในการรักษา COVID-19 อย่างไรก็ตาม สารนี้ยังไม่เป็นที่รู้จัก ไม่เข้าใจ และยังถูกมองในแง่ลบในวงการแพทย์ เราสันนิษฐานว่าเกิดจากความสับสนทางแนวคิดกับโซเดียมไฮโปคลอไรต์ ดังนั้น เราจึงตั้งเป้าที่จะตรวจสอบประสิทธิภาพของการใช้คลอรีนไดออกไซด์ทางปากในการรักษา COVID-19 ผ่านการศึกษาครั้งนี้ โดยทบทวนประวัติของ ClO2 อย่างละเอียด โปรไฟล์ด้านความปลอดภัย/ความเป็นพิษ และการประยุกต์ใช้ที่เป็นไปได้ในการต่อสู้กับ COVID-19 วัตถุประสงค์ของการวิจัยนี้คือเพื่อตรวจสอบว่าคลอรีนไดออกไซด์มีประสิทธิภาพในการจัดการ COVID-19 หรือไม่ [1-65]
คุณสมบัติทางกายภาพและเคมีของคลอรีนไดออกไซด์ (ClO2)
คลอรีนไดออกไซด์ ClO2 เป็นก๊าซภายใต้สภาวะมาตรฐานที่มีมวลโมเลกุล 67.45 กรัม/โมล โดยทั่วไป ก๊าซ ClO2 สามารถสังเคราะห์ได้จากปฏิกิริยาระหว่าง NaClO2 (โซเดียมคลอไรต์) กับ Cl2, NaClO2 กับ HOCl, NaClO2 และกรด เช่น HCl หรือ H3PO4 ละลายน้ำได้ง่ายด้วยความสามารถในการละลาย 3 กรัม/100 มิลลิลิตร https://www.vyphidroasesores.com/
ปฏิกิริยาของคลอรีนไดออกไซด์เกี่ยวข้องกับโครงสร้างและพันธะของมัน คลอรีนไดออกไซด์เป็นโมเลกุลสามอะตอมที่มีสมมาตรแบบโค้งงอ (กลุ่มจุด C2v) โดยมีความยาวพันธะ Cl-O เท่ากับ 147.3 พิโคเมตร และมุมพันธะ 117.6 องศา (รูปที่ 1A) ClO2 มีจำนวนอิเล็กตรอนคี่ โดยมีอิเล็กตรอนวาเลนซ์ 19 ตัว ดังนั้นจึงเป็นอนุมูลพาราแมกเนติก โครงสร้างอิเล็กตรอนของมันทำให้เหล่านักเคมีงงงวยมาเป็นเวลานาน เนื่องจากไม่มีโครงสร้างที่เป็นไปได้ใดๆ และลูอิสก็ไม่น่าพอใจสำหรับคลอรีนไดออกไซด์ [1-10]
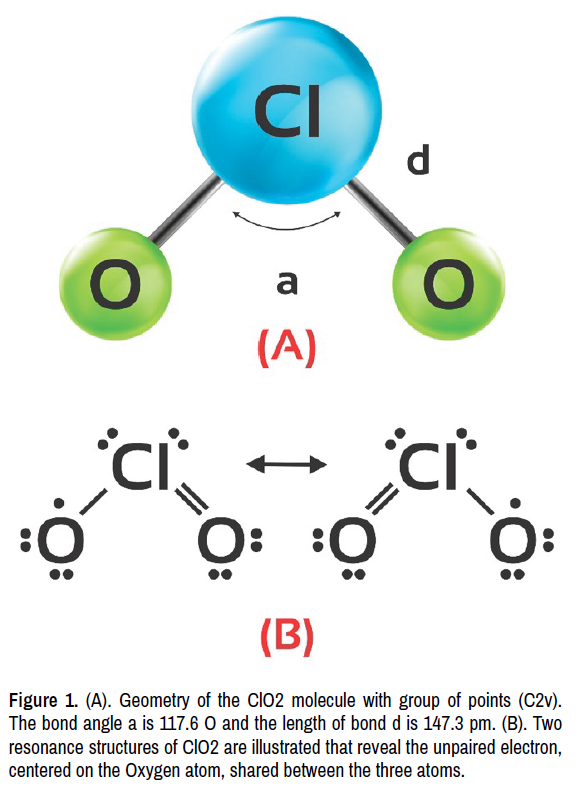
รูปที่ 1. (A). รูปทรงเรขาคณิตของโมเลกุล ClO2 พร้อมกลุ่มจุด (C2v) มุมพันธะ α คือ 117.6° และความยาวพันธะ d คือ 147.3 pm (B). โครงสร้างเรโซแนนซ์สองแบบของ ClO2 แสดงให้เห็นอิเล็กตรอนเดี่ยวที่อยู่ตรงกลางอะตอมออกซิเจน ซึ่งถูกแบ่งปันระหว่างอะตอมทั้งสาม
ทฤษฎีออร์บิทัลโมเลกุลเผยให้เห็นว่าอิเล็กตรอนตัวเดียวจะครอบครองออร์บิทัลโมเลกุลที่ว่างอยู่สูงสุด คือ ออร์บิทัล p* ซึ่งทำให้โมเลกุลเป็นอนุมูลอิสระและอธิบายถึงลักษณะการเกิดปฏิกิริยาของมัน โครงสร้างเรโซแนนซ์สองแบบของ ClO2 แสดงในรูปที่ 1B โครงสร้างเรโซแนนซ์ของอนุมูล ClO2 บ่งชี้ถึงรูปแบบของพันธะคู่ระหว่างอะตอม Cl ตรงกลางกับอะตอม O และพันธะเดี่ยวร่วมกับพันธะ 3 อิเล็กตรอนในพันธะ Cl-O อีกพันธะหนึ่ง อิเล็กตรอนที่ไม่มีคู่จะถูกแบ่งปันระหว่างอะตอมทั้งสามภายในโครงสร้างเรโซแนนซ์ที่แตกต่างกันสองแบบ ความหนาแน่นส่วนใหญ่ของอิเล็กตรอนตัวเดียวจะพบได้ในอะตอม O หนึ่งอะตอม การจัดเรียงที่เป็นเอกลักษณ์นี้ทำให้ ClO2 มีอิเล็กตรอนที่ไม่มีคู่หนึ่งตัวและศูนย์กลางปฏิกิริยาสองแห่ง (O และ Cl) ที่สามารถทำปฏิกิริยาได้
เมื่อคลอรีนไดออกไซด์ละลายในน้ำ ส่วนใหญ่จะไม่เกิดปฏิกิริยาไฮโดรไลซิส แต่จะยังคงเป็นก๊าซที่ละลายอยู่ในสารละลาย ส่วนหนึ่งทำหน้าที่ดังกล่าว และก่อตัวเป็นทั้งไอออนคลอไรต์ (ClO2–) และไอออนคลอเรต (ClO3–) ความสามารถในการละลายของคลอรีนไดออกไซด์ในน้ำที่ระดับน้ำทะเลและที่อุณหภูมิ 25°C อยู่ใกล้เคียงกับ 3 กรัมต่อลิตร (≈ 3000 ppm) ความสามารถในการละลายจะเพิ่มขึ้นที่อุณหภูมิต่ำลง ดังนั้น เมื่อความเข้มข้นมากกว่า 3 กรัมต่อลิตร จึงมักเก็บรักษาไว้ที่อุณหภูมิใกล้เคียง 5°C เมื่อละลายในน้ำบริสุทธิ์ ในภาชนะที่ปิดสนิท ปราศจากแสง และที่อุณหภูมิต่ำ คลอรีนไดออกไซด์จะค่อนข้างเสถียร แม้ว่าจะค่อยๆ สลายตัวเป็นคลอรีนและออกซิเจนก็ตาม คลอไรด์เป็นตัวเร่งปฏิกิริยาในการสลายตัว ในระบบชีวภาพ คาดว่า ClO2 จะมีบทบาทสำคัญในฐานะสารต้านไวรัส/จุลินทรีย์ผ่านปฏิกิริยาเคมีออกซิเดชัน
ฤทธิ์ในการรักษาของคลอรีนไดออกไซด์เกิดจากความสามารถในการเลือกออกฤทธิ์ตามค่า pH หมายความว่าโมเลกุลนี้จะแตกตัวและปล่อยออกซิเจนออกมาเมื่อสัมผัสกับกรดอื่น เมื่อทำปฏิกิริยา มันจะกลายเป็นโซเดียมคลอไรด์ (เกลือแกง) และในขณะเดียวกันก็ปล่อยออกซิเจนออกมา ซึ่งจะไปออกซิไดซ์ (เผาไหม้) เชื้อโรค (จุลินทรีย์ที่เป็นอันตราย) ที่มีค่า pH เป็นกรด เปลี่ยนเชื้อโรคเหล่านั้นให้กลายเป็นออกไซด์ที่เป็นด่าง (“เถ้า”) ดังนั้น เมื่อคลอรีนไดออกไซด์แตกตัว มันจะปล่อยออกซิเจนเข้าสู่กระแสเลือด เช่นเดียวกับเม็ดเลือดแดง โดยใช้หลักการเดียวกัน (ที่รู้จักกันในชื่อปรากฏการณ์โบห์ร) ซึ่งก็คือการเลือกตอบสนองต่อความเป็นกรด เช่นเดียวกับเลือด คลอรีนไดออกไซด์จะปล่อยออกซิเจนออกมาเมื่อพบกับความเป็นกรด ไม่ว่าจะเป็นจากกรดแลคติกหรือจากความเป็นกรดของเชื้อโรค ClO2 เป็นสารต้านจุลชีพที่เลือกขนาดได้
เนื้อเยื่อหลายเซลล์มีความสามารถในการกระจายประจุนี้และไม่ได้รับผลกระทบในลักษณะเดียวกัน คลอรีนไดออกไซด์ ซึ่งเป็นสารฆ่าเชื้อที่แรงเป็นอันดับสองรองจากโอโซน เหมาะสำหรับการใช้ในการรักษามากกว่า เนื่องจากสามารถแทรกซึมและกำจัดไบโอฟิล์มได้ ซึ่งโอโซนทำไม่ได้ ข้อดีอย่างมากของการใช้คลอรีนไดออกไซด์ในการรักษาคือแบคทีเรียไม่สามารถดื้อต่อ ClO2 ได้ แม้ว่าโอโซนจะมีฤทธิ์ฆ่าเชื้อแรงกว่า แต่ศักยภาพในการออกซิเดชั่นสูงถึง 2.07 และครึ่งชีวิตสั้นเพียง 15 นาทีที่อุณหภูมิ 25°C และค่า pH 7.0 ทำให้โอโซนมีประสิทธิภาพน้อยกว่าสำหรับการใช้งานในการรักษาในร่างกาย [11-20]
ประสิทธิภาพในการต้านไวรัสของคลอรีนไดออกไซด์: กลไกการออกฤทธิ์ต้านไวรัสของ ClO2
ClO2 แสดงฤทธิ์ต้านไวรัสผ่านปฏิกิริยาเคมีออกซิเดชัน ไวรัสประกอบด้วยเปลือกนอกหรือเยื่อหุ้ม และแกนกรดนิวคลีอิกภายใน เปลือกหุ้มไวรัสอาจประกอบด้วยโปรตีน ชั้นไขมัน และพอลิแซ็กคาไรด์ และเปลือกหุ้มจะปกป้องแกนกรดนิวคลีอิก นอกเหนือจากการให้การจับแบบเลือกและการจดจำเซลล์ตัวรับ การเปลี่ยนแปลงหรือดัดแปลงเปลือกหุ้มไวรัสหรือแกนกรดนิวคลีอิกจะขัดขวางกลไกการติดเชื้อของไวรัส
ในกรณีของ SARS-CoV-2 เปลือกหุ้มคาร์โบไฮเดรตจะห่อหุ้มและปกป้องมันมากยิ่งขึ้น ทำให้ยากต่อการโจมตีมากกว่าไวรัสชนิดอื่น ประมาณ 70% ของพื้นผิวทั้งหมดของโปรตีนหนามถูกเคลือบด้วยไกลแคน ในกรณีของ SARS-CoV-2 น้ำตาลมีความสำคัญเป็นสองเท่า ประการแรก เนื่องจากสารเหล่านี้ช่วยทำให้หนามโปรตีนคงตัวในโครงสร้างที่ทำให้สามารถจับกับตัวรับ ACE2 บนเซลล์ของเรา ซึ่งเป็นกระบวนการที่เริ่มต้นการติดเชื้อ การกำจัดไกลแคนบางส่วนออกจากพื้นผิวจะทำให้โปรตีนหนามไม่เสถียร และการจับกับตัวรับเหล่านี้ก็จะอ่อนลงด้วย
งานวิจัยชิ้นหนึ่งกำลังพัฒนาโดยผู้เขียนคนหนึ่ง (B. Bolano) เกี่ยวกับกลุ่มอาการหลังติดเชื้อโควิด-19 โดยมุ่งเน้นไปที่ความเป็นไปได้ที่ ClO2 จะออกฤทธิ์ในระดับของอินฟลามาโซมหรือแม้แต่ NETosis ซึ่งอาจเป็นคำอธิบายสำหรับการดีขึ้นของกลุ่มอาการหลังติดเชื้อโควิด-19 ที่พบในแพทย์หลายร้อยคนที่รายงานกรณีศึกษาทั่วโลก ความเกี่ยวข้องและหลักฐานของผลการค้นพบเหล่านี้ต่อกลไกการออกฤทธิ์ต้านการอักเสบของ ClO2 ยังคงไม่ชัดเจนในขณะนี้
เพื่อศึกษาถึงกลไกการออกฤทธิ์อย่างลึกซึ้งยิ่งขึ้น เราได้คัดเลือกบทความที่ตีพิมพ์แล้ว (PubMed, Google Scholar และเครื่องมือค้นหาอื่นๆ) ที่อธิบายถึงการออกฤทธิ์ของ SARS-CoV-2 ในเซลล์ ในการปฏิสัมพันธ์กับ hACE2 และโดยเฉพาะอย่างยิ่ง เราได้ตรวจสอบวิดีโอเสมือนจริงหรือวิดีโอจำลองที่ใช้ซิลิคอน เพื่อแสดงภาพสามมิติของตำแหน่งการออกฤทธิ์ เช่น วิดีโอที่แสดงการจัดการโปรตีนหนามและตัวรับ hACE2 โดยใช้ซอฟต์แวร์เสมือนจริง ChimeraX (UCSF) เป็นต้น
ในทำนองเดียวกัน เราได้ทบทวนโครงสร้างของโปรตีนหนามของไวรัส และอ้างอิงงานวิจัยของ Daniel Wrapp และ Jason S. McLellan จากมหาวิทยาลัยเท็กซัส ภาพสามมิติของไกลโคโปรตีน S ของไวรัส SARS-CoV-2 เบตาโคโรนาไวรัส สามารถมองเห็นได้ด้วยกล้องจุลทรรศน์อิเล็กตรอนแบบแช่แข็งในเวลาอันรวดเร็ว จากภาพที่มีความละเอียด 3.5 Å นี้ ทำให้ยืนยันได้ว่าโปรตีน S นี้จับกับโปรตีน hACE2 ของเซลล์มนุษย์ด้วยความสัมพันธ์ที่สูงกว่าไวรัสโคโรนา SARS-CoV โปรตีน S เป็นเป้าหมายของแอนติบอดีที่สร้างภูมิคุ้มกันให้กับเรา โครงสร้างสามมิติของมันช่วยให้เราเข้าใจว่าเหตุใดแอนติบอดีโมโนโคลนอลที่ตีพิมพ์เพื่อต่อต้าน SARS-CoV จึงไม่มีประสิทธิภาพต่อ SARS-CoV-2
จากข้อมูลนี้ เราได้ทำการศึกษากับแพทย์ด้านชีววิทยาโมเลกุลจากมหาวิทยาลัยสึกุบะ ประเทศญี่ปุ่น โดยมีเป้าหมายเพื่อสร้างสมมติฐานว่าคลอรีนไดออกไซด์ออกฤทธิ์ต่อ SARS-CoV-2 อย่างไร ผลการศึกษาพบว่ามีความสัมพันธ์ที่ดีเยี่ยมระหว่างโครงสร้างและกลไกการแพร่กระจาย รวมถึงการระบุตำแหน่งการออกฤทธิ์ของสารหรือยาที่มีศักยภาพในการรักษา COVID-19 อย่างไรก็ตาม เรายังไม่ได้รับผลลัพธ์ที่คาดหวังในการควบคุมโรคอย่างรวดเร็วด้วยยาที่ทดสอบใดๆ เลย ชีวสารสนเทศศาสตร์เป็นเครื่องมือที่ใช้ข้อมูลทางชีววิทยาในการศึกษาปัญหาทางชีววิทยาในหลากหลายระดับ เช่น วิวัฒนาการ โครงสร้าง หน้าที่ และการควบคุมของกรดนิวคลีอิกและโปรตีน โดยอาศัยวิธีการคำนวณ ในงานของเราที่ประเทศญี่ปุ่น เราทำการวิเคราะห์แบบ in silico ซึ่งเป็นวิธีการเชิงปริมาณที่ครอบคลุม ซึ่งไม่เพียงแต่ให้ข้อมูลเกี่ยวกับพลวัตของกระบวนการภายในเซลล์และภายในโมเลกุลเท่านั้น แต่ยังช่วยให้เราสามารถทำนายพฤติกรรมทางชีววิทยาจากปฏิสัมพันธ์ระดับโมเลกุลได้อีกด้วย ในงานของเรานั้น เรามุ่งเน้นไปที่โดเมนที่อนุรักษ์ไว้ โครงสร้าง หน้าที่ และลักษณะทางชีวเคมี เพื่อทำความเข้าใจกลไกการออกฤทธิ์ของคลอรีนไดออกไซด์ต่อโปรตีนหนามและ RNA ของ SARS-CoV-2 ซึ่งเป็นวิธีการเชิงปริมาณที่สมบูรณ์ที่ให้ข้อมูลเกี่ยวกับพลวัตของกระบวนการภายในเซลล์และภายในโมเลกุลเท่านั้น แต่ยังช่วยให้สามารถทำนายพฤติกรรมทางชีววิทยาจากปฏิสัมพันธ์ระดับโมเลกุลได้อีกด้วย ในงานวิจัยของเรา วิธีการนี้ทำโดยการมุ่งเน้นไปที่โดเมนที่อนุรักษ์ไว้ โครงสร้าง หน้าที่ และลักษณะทางชีวเคมี เพื่อทำความเข้าใจกลไกการออกฤทธิ์ของคลอรีนไดออกไซด์ต่อโปรตีนหนามและ RNA ของ SARS-CoV-2 ซึ่งเป็นวิธีการเชิงปริมาณที่สมบูรณ์แบบ ที่ไม่เพียงแต่ให้ข้อมูลเกี่ยวกับพลวัตของกระบวนการภายในเซลล์และภายในโมเลกุลเท่านั้น แต่ยังช่วยให้สามารถทำนายพฤติกรรมทางชีวภาพจากปฏิสัมพันธ์ระดับโมเลกุลได้อีกด้วย (รูปที่ 2)
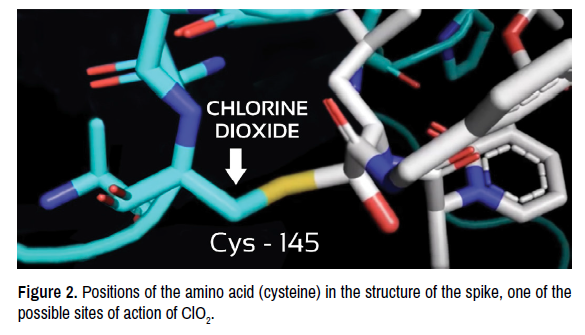
รูปที่ 2 ตำแหน่งของกรดอะมิโน (ซิสเทอีน) ในโครงสร้างของหนามแหลม ซึ่งเป็นหนึ่งในตำแหน่งที่เป็นไปได้ที่ ClO2 จะออกฤทธิ์
การวิเคราะห์ประเภทนี้ไม่เพียงให้ข้อมูลเกี่ยวกับการจำลองแบบ RNA เท่านั้น แต่ยังจำลองพลวัตของความสัมพันธ์ระหว่างโปรตีนหนาม (spike) และตัวรับ hACE2 ด้วย การวิจัยเริ่มต้นด้วยลำดับนิวคลีโอไทด์ของ RNA ของไวรัส โดยกำหนดกรอบการอ่านแบบเปิด (ORF) ซึ่งเมื่อวิเคราะห์แล้ว พบว่ากัวนีนถูกออกซิไดซ์เป็น 8-ออกโซกัวนีน ส่วนเบสอื่นๆ ไม่มีการเปลี่ยนแปลง กรดอะมิโนที่ถูกออกซิไดซ์ด้วยคลอรีนไดออกไซด์พบในโปรตีนหนาม อยู่ในส่วนเกลียว S1, S2, RBD และ hACE2 ซึ่งอาจอธิบายถึงผลการปรับปรุงทางคลินิกที่เกิดขึ้นเกือบจะทันทีจากการใช้ไดออกไซด์
ซิสเทอีน ซึ่งอยู่ในกลุ่มของไทออล เป็นกรดอะมิโนที่มีปฏิกิริยากับระบบจุลินทรีย์ทั้งหมดสูงกว่ากรดอะมิโนอีกสี่ชนิดถึง 50 เท่า ดังนั้นจึงเป็นไปไม่ได้ที่ซิสเทอีนจะสร้างความต้านทานต่อคลอรีนไดออกไซด์ได้
สมมติฐานที่เสนอโดยผู้เขียน Insignares – Carrione และคณะ คือ สาเหตุของฤทธิ์ต้านไวรัสของคลอรีนไดออกไซด์ต่อ SARS-CoV-2 สามารถอธิบายได้จากการออกฤทธิ์ต่อกรดอะมิโนอย่างน้อยห้าชนิด (ซิสเทอีน ทริปโตเฟน ไทโรซีน โพรลีน และไฮดรอกซีโพรลีน)
เภสัชจลนศาสตร์
เภสัชจลนศาสตร์ของ ClO2 แตกต่างกันไปตามวิธีการสัมผัส Scatina และคณะได้ตรวจสอบการดูดซึมทางผิวหนังของสารเตรียม ClO2 ที่ทาลงบนหลังที่โกนขนของหนู การดูดซึม Cl สูงสุดในพลาสมาพบหลังจาก 72 ชั่วโมง และความเข้มข้นในพลาสมาถึง 69.4 ไมโครกรัม% Cl ครึ่งชีวิตของการดูดซึมคำนวณได้เป็น 22.1 ชั่วโมง ซึ่งสอดคล้องกับค่าคงที่อัตรา 0.0314 h-1 (รูปที่ 3)
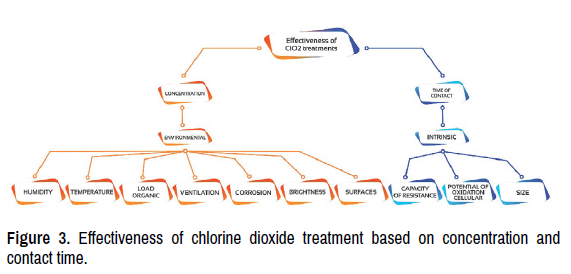
รูปที่ 3 ประสิทธิภาพของการบำบัดด้วยคลอรีนไดออกไซด์โดยพิจารณาจากความเข้มข้นและระยะเวลาสัมผัส
Fridyland และ Kagan ได้วัดระดับการดูดซึม ClO2 ในช่องปากของมนุษย์โดยการล้างปากด้วยน้ำที่มีความเข้มข้นของ ClO2 ตามที่กำหนดไว้ แล้ววัดความเข้มข้นของ ClO2 ที่เหลืออยู่ในน้ำที่ใช้ล้างปาก พวกเขาพบว่า ClO2 ถูกดูดซึมได้มากถึง 30%
ความปลอดภัย/ความเป็นพิษ
ความปลอดภัย/ความเป็นพิษของ ClO2 ขึ้นอยู่กับตัวแปรหลายอย่าง รวมถึงวิธีการใช้ (เช่น การสูดดม การทา หรือการรับประทาน) สถานะของโมเลกุล (เช่น ก๊าซหรือสารละลาย) ความเข้มข้น (โดยปกติจะวัดเป็น mg/L หรือ ppm สำหรับสารละลาย และ ppm หรือ mg/m³ สำหรับก๊าซ) และระยะเวลาการสัมผัส ก๊าซ ClO2 มีความเป็นพิษที่ความเข้มข้นต่ำกว่า ClO2 ในสารละลายมาก ความเป็นพิษยังเพิ่มขึ้นตามระยะเวลาการสัมผัสด้วย ข้อเท็จจริงที่ว่า ClO2 มีความเป็นพิษน้อยกว่าในรูปสารละลาย ทำให้สามารถใช้โมเลกุลนี้เป็นสารฆ่าเชื้อที่ปลอดภัยในน้ำประปาของเทศบาล เป็นสารฆ่าเชื้อสำหรับน้ำดื่ม ณ จุดใช้งาน และเป็นสารฆ่าเชื้ออาหาร รวมถึงการใช้งานอื่นๆ (รูปที่ 4)
ด้านล่างนี้เป็นการทบทวนการศึกษาที่ตรวจสอบความปลอดภัยและความเป็นพิษของ ClO2
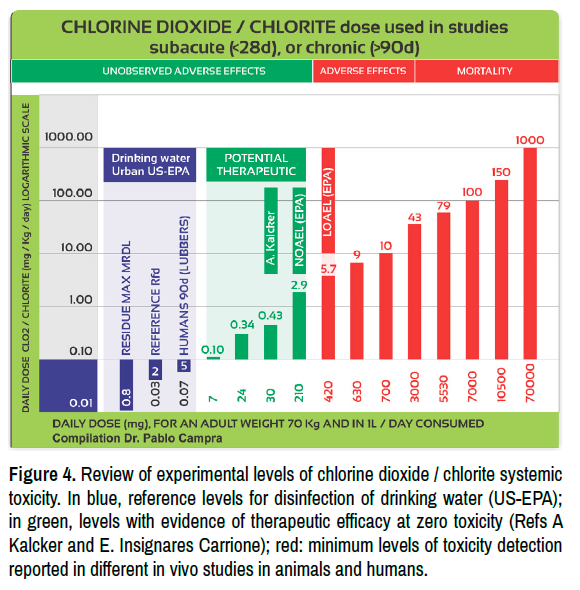
รูปที่ 4 การทบทวนระดับความเป็นพิษของคลอรีนไดออกไซด์/คลอไรต์ในระบบร่างกายจากการทดลอง สีน้ำเงินคือระดับอ้างอิงสำหรับการฆ่าเชื้อในน้ำดื่ม (US-EPA) สีเขียวคือระดับที่มีหลักฐานแสดงถึงประสิทธิภาพในการรักษาที่ระดับความเป็นพิษเป็นศูนย์ (อ้างอิง A Kalcker และ E. Insignares Carrione) สีแดงคือระดับต่ำสุดที่ตรวจพบความเป็นพิษตามรายงานในการศึกษาในร่างกายสัตว์และมนุษย์ต่างๆ
ClO2 ละลายในน้ำ
การศึกษาในหลอดทดลอง: Noszticzius และคณะ ได้ตรวจสอบผลกระทบที่แตกต่างกันของ ClO2 ต่อจุลินทรีย์เทียบกับมนุษย์หรือสัตว์ พวกเขาทำการศึกษาการไหลเวียนโดยใช้เยื่อโปรตีนและพบว่าขนาดของสิ่งมีชีวิตที่สัมผัสกับ ClO2 มีอิทธิพลต่อผลกระทบของสารออกซิแดนต์ พวกเขารายงานว่า ClO2 ที่มีความเข้มข้นต่ำสามารถฆ่าสิ่งมีชีวิตขนาดไมครอนได้อย่างรวดเร็ว ในขณะที่ก่อให้เกิดอันตรายเพียงเล็กน้อยต่อสิ่งมีชีวิตขนาดใหญ่ เช่น มนุษย์ ผู้เขียนแนะนำว่าเหตุผลสำหรับผลกระทบที่แตกต่างกันนี้คือ: (1) ClO2 ไม่สามารถแทรกซึมลึกเข้าไปในเนื้อเยื่อของสิ่งมีชีวิตขนาดใหญ่ได้ และ (2) การไหลเวียนของสิ่งมีชีวิตขนาดใหญ่ให้สารต้านอนุมูลอิสระอย่างต่อเนื่อง ซึ่งให้การป้องกันต่อผลกระทบของสารออกซิแดนต์ ClO2 การศึกษาในหลอดทดลองพบว่าเมทฮีโมโกลบินจะไม่เกิดขึ้นเว้นแต่ความเข้มข้นของกลูตาไธโอนในเซลล์เม็ดเลือดแดงจะลดลงเกือบหมด
การศึกษาในสัตว์ในร่างกาย: Daniel และคณะ การทดลองนี้ได้ทำการทดลองกับหนูโดยให้หนูสัมผัสกับความเข้มข้นของ ClO2 ที่ 0, 25, 50, 100 หรือ 200 มิลลิกรัมต่อลิตร เป็นเวลา 90 วัน ซึ่งเทียบเท่ากับปริมาณ 11.5 มิลลิกรัมต่อกิโลกรัมต่อวันในหนูตัวผู้ และ 14.9 มิลลิกรัมต่อกิโลกรัมต่อวันในหนูตัวเมีย ไม่พบการเสียชีวิตที่เกี่ยวข้องกับการสัมผัสสารดังกล่าว
อับเดล-ราห์มานและคณะ รายงานอัตรา LD50 สำหรับหนูตัวเมียอยู่ที่ 340 ถึง 468 มิลลิกรัมต่อกิโลกรัม และสำหรับหนูตัวผู้อยู่ที่ 292 ถึง 424 มิลลิกรัมต่อกิโลกรัม หลังจากการให้ยาทางปากเพียงครั้งเดียว รายงานเพิ่มเติมเกี่ยวกับ LD50 ในหนู ได้แก่ 94 มิลลิกรัมต่อกิโลกรัม (WHO, 2002), 140 มิลลิกรัมต่อกิโลกรัม, 292 ppm (National Institute for Occupational Safety and Health, 2014) และ > 5,000 มิลลิกรัมต่อกิโลกรัม (US Environmental Protection Agency, 2008) มีรายงานว่าค่า LD50 ในหนูมีค่ามากกว่า 10,000 มก./กก. (Shi et al. 1999)
ในการศึกษาที่ดำเนินการโดยมหาวิทยาลัยเกเรตาโร (เม็กซิโก) ในปี 2020 นักวิจัยได้ท้าทายสมมติฐานที่ว่า ClO2 ช่วยลดปริมาณไวรัสและอัตราการตายที่เกิดจากไวรัสในแบบจำลองสัตว์มีกระดูกสันหลัง เพื่อจุดประสงค์นี้ พวกเขาได้กำหนดปริมาณไวรัส รอยโรคที่เกิดจากไวรัส และอัตราการตายในตัวอ่อนไก่ที่มีอายุ 10 วัน ซึ่งได้รับการฉีดเชื้อไวรัส IBV (avian coronavirus) สายพันธุ์อ่อนฤทธิ์จากแมสซาชูเซตส์และคอนเนตทิคัต ในปริมาณ 104 EID50/มล. การรักษาด้วย ClO2 มีผลกระทบอย่างมากต่อการติดเชื้อ IBV โดยเฉพาะอย่างยิ่ง ปริมาณไวรัสลดลง 2.4 เท่า และอัตราการตายลดลงครึ่งหนึ่งในตัวอ่อนที่ติดเชื้อซึ่งได้รับการรักษาด้วย ClO2 การติดเชื้อทำให้เกิดความผิดปกติในการพัฒนา ไม่ว่าจะได้รับการรักษาหรือไม่ก็ตาม พบรอยโรคที่typical ของการติดเชื้อ IBV ในตัวอ่อนที่ได้รับการฉีดเชื้อทั้งหมด แต่ความรุนแรงมีแนวโน้มลดลงอย่างมีนัยสำคัญในตัวอ่อนที่ได้รับการรักษาด้วย ClO2 พวกเขาไม่พบหลักฐานความเป็นพิษทั้งในระดับมหภาคหรือจุลภาคที่เกิดจาก ClO2 ในปริมาณที่ใช้ในกรณีนี้ การศึกษาจึงสรุปได้ว่า ClO2 อาจเป็นวิธีที่ปลอดภัยและมีประสิทธิภาพในการรักษาและบรรเทาผลกระทบจากการติดเชื้อไวรัสโคโรนาในนก และชี้ให้เห็นถึงความเป็นไปได้ว่าอาจพบผลลัพธ์ที่คล้ายคลึงกันในสิ่งมีชีวิตอื่นๆ
คลอรีนไดออกไซด์ (CDS) ที่ละลายในน้ำ ในการศึกษาในมนุษย์และสัตว์
การศึกษาโดย Lubbers et al. (1982, 1984a) ที่คณะแพทยศาสตร์ มหาวิทยาลัยโอไฮโอสเตท ได้ประเมินความเป็นพิษระยะสั้นของการดื่ม ClO2 ในการศึกษาครั้งแรก (Lubbers et al. 1982) กลุ่มผู้ชายสุขภาพดี 10 คน ดื่ม ClO2 ปริมาณ 1,000 มล. (แบ่งเป็นสองส่วน ส่วนละ 500 มล. ห่างกัน 4 ชั่วโมง) โดยค่อยๆ เพิ่มปริมาณขึ้นเรื่อยๆ การศึกษานี้ประกอบด้วยลำดับการทดลอง 6 ชุด ชุดละ 3 วัน โดยผู้เข้าร่วมการทดลองดื่มสารละลาย ClO2 ที่ความเข้มข้น 0.1, 1.0, 5.0, 10.0, 18.0 และ 24.0 มก./ลิตร (0.34 มก./กก. โดยสมมติน้ำหนักตัวอ้างอิงที่ 70 กก.) ในการศึกษาครั้งที่สอง (Lubbers et al., 1984a) กลุ่มผู้ชายวัยผู้ใหญ่ 10 คนได้รับน้ำกลั่น 500 มล. ที่มี ClO2 ความเข้มข้น 0 หรือ 5 มก./ลิตร (0.04 มก./กก.-วัน โดยสมมติน้ำหนักตัวอ้างอิงที่ 70 กก.) เป็นเวลา 12 สัปดาห์
ในการศึกษาเปรียบเทียบคลอรีนไดออกไซด์บริสุทธิ์สูงกับสารล้างคลองรากฟันอีกสองชนิดเกี่ยวกับความมีชีวิตของเซลล์ต้นกำเนิดเอ็นยึดปริทันต์ (PLDSCs) การทดลองความมีชีวิตของเซลล์แสดงให้เห็นว่าการใช้ ClO2 ไม่ทำให้ความมีชีวิตของ PLDSCs ลดลงอย่างมีนัยสำคัญในความเข้มข้นที่ใช้ในการฆ่าเชื้อจุลินทรีย์ ในทางตรงกันข้าม สารล้างคลองรากฟันแบบดั้งเดิม H2O2 และ CHX มีความเป็นพิษสูงต่อ PLDSCs การแก่ตัวของเซลล์ PLDSC (ระยะที่ 3 เทียบกับระยะที่ 7) มีผลกระทบต่อการตอบสนองต่อสารเหล่านี้ เนื่องจากการแสดงออกของเครื่องหมายเซลล์ต้นกำเนิดมีเซนไคม์ลดลง พวกเขาสรุปว่าถึงแม้ส่วนประกอบสำคัญของน้ำยาบ้วนปาก (H2O2)
การรับประทาน ClO2 ที่ละลายในน้ำทางปาก
การศึกษาเดียวที่ดำเนินการเกี่ยวกับการใช้ ClO2 ที่ละลายในน้ำ (CDS) โดยการรับประทานทางปากคือการศึกษาปัจจุบันของเราซึ่งดำเนินการในรูปแบบการทดลองทางคลินิกหลายศูนย์ในหลายประเทศจากอเมริกากลางและอเมริกาใต้ (https://clinicaltrials.gov/ct2/show/NCT0434374) สถิติของโบลิเวียซึ่งการใช้ ClO2 ที่ละลายในน้ำเพื่อป้องกันและรักษา COVID-19 ได้รับการอนุมัติตามกฎหมายในต้นเดือนสิงหาคม 2020 แสดงให้เห็นถึงการลดลงอย่างเห็นได้ชัดของจำนวนผู้ป่วยและผู้เสียชีวิตในประเทศนั้น จุดสูงสุดที่บันทึกไว้ในโบลิเวียคือสัปดาห์ระบาดวิทยาที่ 29 (10,939 ราย) โดยจำนวนผู้ป่วยลดลงเหลือ 670 รายในสัปดาห์ระบาดวิทยาที่ 45 (คิดเป็นการลดลง 93%) อัตราการเสียชีวิตลดลงจาก 8% เหลือ 4.5% ในสัปดาห์ระบาดวิทยาที่ 36 ซึ่งสอดคล้องกับการใช้ก๊าซคาร์บอนไดออกไซด์ในปริมาณมากในหมู่ประชาชน โดยไม่สามารถยืนยันได้อย่างแน่นอนว่าก๊าซคาร์บอนไดออกไซด์เป็นสาเหตุของการลดลงนี้ (https://snis.minsalud.gob.bo/) จากจำนวนผู้ป่วยรายวันสูงสุด 2,031 รายในวันที่ 20 สิงหาคม 2563 จำนวนผู้ป่วยลดลงเหลือ 147 รายในวันที่ 21 ตุลาคม 2563 คิดเป็นลดลง 93% จำนวนผู้เสียชีวิตรายวันลดลงจากจุดสูงสุด 132 รายในวันที่ 3 กันยายน 2563 เหลือ 24 รายในวันที่ 21 ตุลาคม 2563 คิดเป็นลดลง 82% (https://www.COVID-19.onl/country/bolivia)
แม้ว่าจะมีจำนวนผู้ป่วยเพิ่มขึ้นอีกครั้งในช่วงสัปดาห์ระบาดวิทยาที่ 49 ถึง 53 แต่อัตราการเสียชีวิตยังคงอยู่ในระดับต่ำ แพทย์บางส่วนที่เกี่ยวข้องกับกลุ่มวิจัยของเรา (ในโบลิเวียมีแพทย์มากกว่า 220 คน) ให้ข้อเสนอแนะว่าประชากรลดการบริโภคไดออกไซด์ลง ซึ่งอาจเป็นคำอธิบายที่เป็นไปได้สำหรับจุดสูงสุด และการเพิ่มขึ้นของการบริโภคคลอรีนไดออกไซด์ทำให้จุดสูงสุดลดลงกลับสู่ระดับก่อนหน้า ส่งผลให้อัตราการเสียชีวิตลดลงเมื่อเทียบกับระดับก่อนหน้า (การสื่อสารส่วนตัว) (รูปที่ 5)
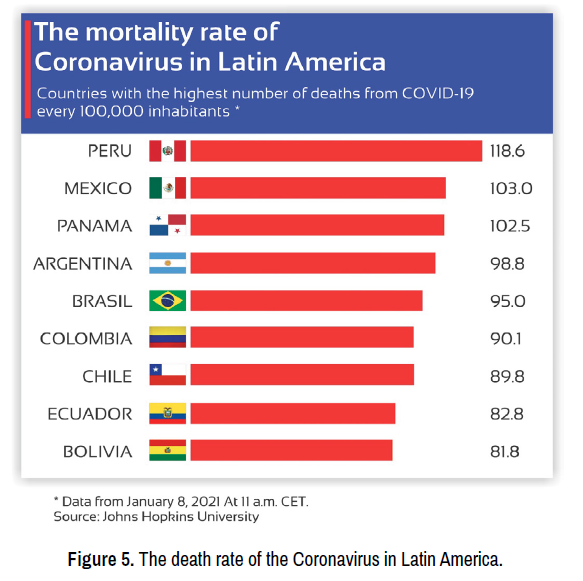
ภาพที่ 5 อัตราการเสียชีวิตจากไวรัสโคโรนาในละตินอเมริกา
โดยสรุปแล้ว ในขณะที่ประเทศอื่นๆ ระดับมลพิษคงที่ แต่ในโบลิเวียกลับลดลง ซึ่งสาเหตุของการลดลงนี้ (ในฐานะคำอธิบายที่เป็นไปได้) อาจมาจากมาตรการป้องกัน การใช้คลอรีนไดออกไซด์ และการใช้ยาแผนโบราณอย่างแพร่หลาย
ปริมาณยา
การศึกษาในหลอดทดลองและในร่างกายแสดงให้เห็นว่า ClO2 ที่ละลายน้ำได้ในปริมาณต่ำ มีฤทธิ์ต้านไวรัสที่ทรงพลังและรวดเร็วต่อไวรัสหลากหลายชนิด ในการศึกษาเกี่ยวกับน้ำดื่มในประเทศเนเธอร์แลนด์ Jin และคณะ พบว่าการบำบัดด้วย ClO2 ที่ความเข้มข้น 0.5 ppm เป็นเวลา 25 นาที หรือ 1.5 ppm เป็นเวลา 10 นาที หรือ 2 ppm เป็นเวลา 5 นาที สามารถลดปริมาณเอนเทอโรไวรัสได้อย่างน้อย 4 log Schijven และคณะ แสดงให้เห็นว่าน้ำดื่มของเทศบาลที่บำบัดด้วย ClO2 (0.1 ppm ในฤดูร้อนและ 0.05 ppm ในฤดูหนาว) ช่วยลดระดับอะดีโนไวรัสลงอย่างมีนัยสำคัญจนถึงระดับที่ถือว่าปลอดภัยสำหรับน้ำดื่ม Alvarez และ O’Brien พบว่าการเติม ClO2 ที่ความเข้มข้น 40 ppm ลงในน้ำเสียที่ปนเปื้อน SARS-CoV สามารถยับยั้ง SARS-CoV ได้อย่างสมบูรณ์ภายใน 30 นาที ปริมาณที่ใช้ในการวิจัยนี้คือ 30 มิลลิกรัมต่อวัน เป็นเวลา 21 วัน ซึ่งต่ำกว่าระดับ NOAEL มาก หรือในกรณีที่แย่ที่สุดก็เท่ากับระดับ NOAEL ที่รายงานไว้ในงานวิจัยก่อนหน้านี้ในสัตว์ทดลอง ดังที่เราได้กล่าวถึงในบรรทัดก่อนหน้านี้
วัสดุและวิธีการ
เพื่อทำการค้นหาข้อมูลทางวิทยาศาสตร์เกี่ยวกับคลอรีนไดออกไซด์อย่างครอบคลุมที่สุด พวกเขาได้ค้นหาใน Google Scholar, PubMed (Medline), LILACS, Cochrane Library, Science, Scielo, MedScape โดยมองหาบทความในภาษาอังกฤษและสเปน ที่มีคำค้นหาว่า chlorine dioxide, virus, SARS-CoV-2, coronavirus, oxidant, water purification, “Chlorine dioxide” หรือ “Chlorine dioxide protocol” หรือ Chlorine dioxide AND virus; Chlorine dioxide AND SARS-COV-2; หรือ “การรักษาด้วยยา COVID-19” หรือ “โปรตีนสไปค์ของไวรัส COVID-19” หรือ “ไวรัสโคโรนาสายพันธุ์ใหม่ที่ก่อให้เกิดโรคทางเดินหายใจเฉียบพลันรุนแรง 2” หรือ “COVID-19” หรือ “2019-nCoV” หรือ “SARS-CoV-2” หรือ “ไวรัสโคโรนาสายพันธุ์ใหม่ 2019” หรือ “โรคติดเชื้อไวรัสโคโรนา 2019” หรือ (ปอดอักเสบ)
นอกจากนี้ ยังได้ทำการค้นหาใน Google โดยใช้คำค้นหาเดียวกันนี้ บทความที่เลือกมาพิจารณาประกอบด้วยบทความที่เกี่ยวข้องกับการใช้ ClO2 ในการป้องกันหรือรักษา COVID-19 รวมถึงประโยชน์และผลข้างเคียงหรือความเป็นพิษของสารดังกล่าว บทความที่ค้นพบทั้งหมดได้รับการคัดกรอง และเลือกบทคัดย่อที่เกี่ยวข้องบางส่วนเพื่อทำการประเมินเพิ่มเติม จากนั้นจึงค้นหาเอกสารอ้างอิงเพิ่มเติมในบรรณานุกรมของบทความเหล่านั้น บทความสุดท้ายที่คัดเลือกเพื่อรวมไว้ในการทบทวนนี้ประกอบด้วยบทความที่ตรวจสอบการใช้งานในอดีต เคมี ความเป็นพิษ ฤทธิ์ต้านจุลชีพและต้านไวรัสของ ClO2 การวิจัยก่อนหน้านี้ในสัตว์ทดลองทั้งในหลอดทดลองและในร่างกาย และการวิจัยในมนุษย์ เราได้ตรวจสอบฐานข้อมูลของ www.clinicaltrials.gov และฐานข้อมูลของ WHO International Clinical Registry Platform (ICTRP) เพื่อระบุการทดลองทางคลินิกที่กำลังดำเนินการอยู่หรือยังไม่ได้ตีพิมพ์
จากผลการค้นหา เราได้เลือกบทความที่กล่าวถึงฤทธิ์ต้านไวรัสของคลอรีนไดออกไซด์ต่อจุลินทรีย์ต่างๆ โดยเฉพาะอย่างยิ่งไวรัส และในจำนวนนั้นรวมถึง SARS-CoV-2 หรือ SARS-CoV ในทางกลับกัน เราได้เลือกบทความที่อธิบายการทำงานของ SARS-CoV-2 ในเซลล์ ในการปฏิสัมพันธ์กับ ACE2 และโดยเฉพาะอย่างยิ่ง เราได้ตรวจสอบวิดีโอเสมือนจริงหรือวิดีโอจำลองที่ใช้ Silico เพื่อการแสดงผลแบบสามมิติ จากแหล่งข้อมูลต่างๆ เช่น วิดีโอที่แสดงการจัดการโปรตีนหนามและตัวรับ ACE2 (37) โดยใช้ซอฟต์แวร์ความเป็นจริงเสริม ChimeraX (UCSF) เป็นต้น ในทำนองเดียวกัน เราได้ทบทวนโครงสร้างของโปรตีนหนามของไวรัสและอ้างอิงงานวิจัยของ Daniel Wrapp และ Jason S. McLellan จากมหาวิทยาลัยเท็กซัส ซึ่งข้อมูลดังกล่าวทำให้เราสามารถตั้งสมมติฐานได้ว่าคลอรีนไดออกไซด์ออกฤทธิ์ต่อ SAR-CoV-2 อย่างไร ในการศึกษาคู่ขนาน
ด้วยข้อมูลที่จำเป็นในการสรุปว่าคลอรีนไดออกไซด์มีประโยชน์และว่าการใช้ในสถานการณ์การระบาดของ COVID-19 นั้นมีความเป็นไปได้สูงในการควบคุมโรคโดยอาศัยพื้นฐานทางวิทยาศาสตร์ที่เปิดเผยในการวิจัยก่อนหน้านี้ และเหนือสิ่งอื่นใดคือไม่มีอันตรายต่อผู้ป่วย เราจึงตัดสินใจดำเนินการวิจัยเพื่อตรวจสอบว่าการรับประทานคลอรีนไดออกไซด์มีประสิทธิภาพในการรักษา COVID-19 หรือไม่
เราตัดสินใจดำเนินการวิจัยระยะที่ IIa เนื่องจากมีความเร่งด่วนในการตรวจสอบวิธีการรักษาที่มีประสิทธิภาพ รวดเร็ว และประหยัด ซึ่งสามารถนำไปใช้ได้ทั่วโลกอย่างรวดเร็ว ด้วยเหตุนี้เราจึงเลือกใช้การทดลองทางคลินิกแบบกึ่งทดลอง (Quasi-Experimental Clinical Trial: ECE) ศูนย์ข้อมูลเทคโนโลยีชีวภาพแห่งชาติ (NCBI) สำหรับฐานข้อมูล Medline และ Pubmed เพิ่งรวมแนวคิดของ ECE (Quasi Experimental Studies) ไว้ภายใต้คำศัพท์ MeSH “Non-Randomized Controlled Trials as Topic” (NCBI, 2015)
เมื่อจัดทำระเบียบวิธีวิจัยเสร็จแล้ว จึงตัดสินใจลงทะเบียนใน clinicaltrials.gov ซึ่งได้รับการอนุมัติเมื่อวันที่ 7 เมษายน 2563 ภายใต้หมายเลข NCT 04343742 การออกแบบการวิจัยเป็นการวิจัยแบบหลายศูนย์นานาชาติ เพื่อให้สามารถเก็บตัวอย่างได้เร็วขึ้น และในอนาคต เพื่อให้ได้ตัวอย่างที่ใหญ่ขึ้นและเป็นตัวแทนมากขึ้น ระเบียบวิธีวิจัยเดียวกันนี้ได้ถูกนำเสนอใน 11 ประเทศในทวีปอเมริกาและในสเปนเพื่อขออนุมัติ น่าเสียดายที่หน่วยงานควบคุมยาในทุกประเทศได้ออกคำเตือนและแม้กระทั่งสั่งห้ามการใช้ยาชนิดนี้เพื่อการบริโภคของมนุษย์ ทำให้คณะกรรมการด้านจริยธรรมอนุมัติข้อตกลงได้ยาก ในประเทศโบลิเวีย
การเก็บรวบรวมและบันทึกข้อมูล
การเก็บรวบรวมและบันทึกข้อมูลดำเนินการโดยการบันทึกข้อมูลด้านประชากรศาสตร์และอาการต่างๆ และโดยใช้มาตรวัดการสังเกตตามมาตรวัดแบบอนาล็อกเชิงภาพ (VAS) และพารามิเตอร์ทางห้องปฏิบัติการที่จัดเรียงตามมาตรวัดแบบลิเคิร์ตเพื่อการประเมินและการเปรียบเทียบที่ดีขึ้น ดังนั้นจึงได้สร้างเครื่องมือหรือแบบฟอร์มขึ้น ซึ่งบันทึกไว้ในซอฟต์แวร์ที่ออกแบบมาเป็นพิเศษสำหรับการวิจัย โดยมีคุณลักษณะดังต่อไปนี้:
แบบฟอร์มอิเล็กทรอนิกส์ในสภาพแวดล้อมเว็บได้รับการออกแบบเป็นพิเศษสำหรับการบันทึกข้อมูลที่จำเป็นในการวิจัยผ่านทางพีซี สมาร์ทโฟน และแท็บเล็ต
แอปพลิเคชันนี้ได้รับการพัฒนาโดยบริษัท SCORPII SAS ในปี 2020 โดยมีฟังก์ชันการทำงานดังต่อไปนี้:
• การบันทึกข้อมูลการติดต่อและประวัติพื้นฐานของแพทย์ผู้ทำการวิจัย ซึ่งระบุที่ตั้งของศูนย์การแพทย์ที่ผู้ป่วยได้รับการรักษาครั้งแรก และบันทึกรายละเอียดการติดต่อและประวัติทางสังคมและวัฒนธรรมของแพทย์
• จัดเก็บจดหมายแสดงความยินยอมโดยแจ้งให้ทราบสำหรับการใช้สารวิจัย ซึ่งลงนามโดยผู้ป่วยแต่ละราย
• การบันทึกข้อมูลเกี่ยวกับประวัติการวินิจฉัยทางคลินิกเบื้องต้นของผู้ป่วย
• บันทึกประวัติการติดตามผลการรักษาของผู้ป่วยที่เกี่ยวข้องกับอาการ ระดับความเจ็บปวด (VAS) และการประเมินด้วยมาตราส่วนลิเคิร์ตของรายงานผลการตรวจทางห้องปฏิบัติการในวันที่ 0, 7, 14 และ 21
• ในส่วนของเงื่อนไขด้านความปลอดภัย ข้อมูลที่บันทึกไว้ไม่มีตัวเลือกให้แพทย์ผู้ทำการวิจัยแก้ไขหรือปรับเปลี่ยนได้ เพื่อรับประกันความถูกต้อง ความสมบูรณ์ และความลับของข้อมูล นักวิจัยแต่ละคนสามารถเข้าถึงแอปพลิเคชันได้โดยการยืนยันตัวตนด้วยอีเมลและรหัสผ่าน ทำให้พวกเขามีความรับผิดชอบแต่เพียงผู้เดียวในการบันทึกข้อมูลของผู้ป่วยแต่ละราย
• การสร้างรายงานการรวบรวมข้อมูลเพื่อการวิเคราะห์ทางสถิติ ซึ่งเป็นฟังก์ชันที่ผู้อำนวยการวิจัยสามารถเข้าถึงได้เท่านั้น โดยไม่มีตัวเลือกในการแก้ไขฐานข้อมูลบันทึกที่จัดทำโดยแพทย์ผู้ทำการวิจัย
กล่าวคือ เครื่องมือนี้ทำให้สามารถรวบรวมและบันทึกผลการตรวจทางอาการทางคลินิกและทางห้องปฏิบัติการในช่วงเริ่มต้นของการรักษาในกลุ่มทดลองและกลุ่มควบคุม รวมถึงหลังจากนั้น 7, 14 และ 21 วัน
นอกเหนือจากข้อมูลทางประชากรศาสตร์แล้ว ยังมีการวัดสิ่งต่อไปนี้: อาการทางคลินิก: ตาแดง มีไข้ ไอ มีเสมหะ อ่อนเพลีย/ไม่มีแรง หนาวสั่น อาเจียน หายใจลำบาก คัดจมูก เกณฑ์ VAS (มาตราส่วนอนาล็อกภาพ หรือ VAS) สำหรับความเจ็บปวด คือเส้นตรงที่ปลายด้านหนึ่งหมายถึงไม่เจ็บปวด และปลายอีกด้านหนึ่งหมายถึงความเจ็บปวดที่รุนแรงที่สุดเท่าที่จะจินตนาการได้ ผู้ป่วยจะทำเครื่องหมายบนเส้นตรงที่ตรงกับระดับความเจ็บปวดที่รู้สึก และตัวแปรที่ตรวจสอบ ได้แก่ เจ็บคอ ปวดหัว เจ็บหน้าอก ปวดกล้ามเนื้อทั่วไป และอาการที่เกิดจากอาการปวดหลังส่วนล่าง เกณฑ์ลิเคิร์ต (มาตราส่วนลิเคิร์ตเป็นมาตราส่วนเชิงลำดับโดยใช้ 5 ระดับ) จัดกลุ่มการตรวจทางคลินิก ตัวแปรที่ตรวจสอบ ได้แก่ ลิมโฟไซต์ เม็ดเลือดขาว เกล็ดเลือด โปรตีนซี-รีแอคทีฟ แลคเตทดีไฮโดรจีเนส AST -D-ไดเมอร์ และแลคเตทในการวัดออกซิเจนในเลือด [36-55]
เครื่องมือดังกล่าวทำให้สามารถเก็บรวบรวมและบันทึกผลลัพธ์จากการตรวจทางอาการ การประเมินอาการปวด (VAS) และการตรวจทางห้องปฏิบัติการ (LIKERT) ในช่วงเริ่มต้นของการรักษา (หรือค่าพื้นฐาน) รวมถึงหลังจากนั้น 7, 14 และ 21 วัน
การวิเคราะห์และการตีความข้อมูล
ดำเนินการตามตัวแปรที่กำหนดไว้ โดยใช้ซอฟต์แวร์สถิติ IBM – SPSS วิเคราะห์ข้อมูลของกลุ่มทดลองและกลุ่มควบคุม วิเคราะห์อาการทั่วไปโดยใช้การทดสอบเปรียบเทียบสัดส่วนและช่วงความเชื่อมั่น และวิเคราะห์เกณฑ์ VAS และ Likert โดยใช้การทดสอบแบบจับคู่โดยใช้การทดสอบ Wilcoxon – Mann – Whitney α: 95% (ตารางที่ 1-3)
| อาการ | กลุ่ม | วันที่ 0 n (%) | ค่า P | วันที่ 7 n (%) | ค่า P | วันที่ 14 n (%) | ค่า P |
| ——————– | —— | ————– | —— | ————– | —— | ————— | —— |
| ไข้ | ควบคุม | 18 (90%) | 0.3160 | 14 (70%) | 0.0000 | 12 (60%) | 0.0000 |
| | ทดลอง | 17 (85%) | | 0 (0%) | | 0 (0%) | |
| ไอ | ควบคุม | 20 (100%) | 0.0680 | 18 (90%) | 0.0000 | 18 (90%) | 0.0000 |
| | ทดลอง | 18 (90%) | | 6 (30%) | | 6 (30%) | |
| อ่อนเพลีย / ไม่มีแรง | ควบคุม | 18 (90%) | 0.1015 | 20 (100%) | 0.0000 | 20 (100%) | NA |
| | ทดลอง | 15 (75%) | | 2 (10%) | | 0 (0%) | |
| มีเสมหะ | ควบคุม | 7 (35%) | 0.1405 | 3 (15%) | 0.0301 | 0 (0%) | NA |
| | ทดลอง | 4 (20%) | | 0 (0%) | | 0 (0%) | |
| หนาวสั่น | ควบคุม | 17 (85%) | 0.0001 | 10 (50%) | 0.0000 | 4 (20%) | 0.0127 |
| | ทดลอง | 7 (35%) | | 0 (0%) | | 0 (0%) | |
| อาเจียน | ควบคุม | 1 (5%) | 0.1524 | 0 (0%) | NA | 0 (0%) | NA |
| | ทดลอง | 0 (0%) | | 0 (0%) | | 0 (0%) | |
| หายใจลำบาก | ควบคุม | 18 (90%) | 0.5000 | 16 (80%) | 0.0006 | 12 (60%) | 0.0005 |
| | ทดลอง | 18 (90%) | | 7 (35%) | | 3 (15%) | |
| คัดจมูก | ควบคุม | 5 (25%) | 0.2438 | 2 (10%) | 0.0680 | 0 (0%) | NA |
| | ทดลอง | 7 (35%) | | 0 (0%) | | 0 (0%) | |